Bruk verktøyet TIMES til å vurdere sår strukturert
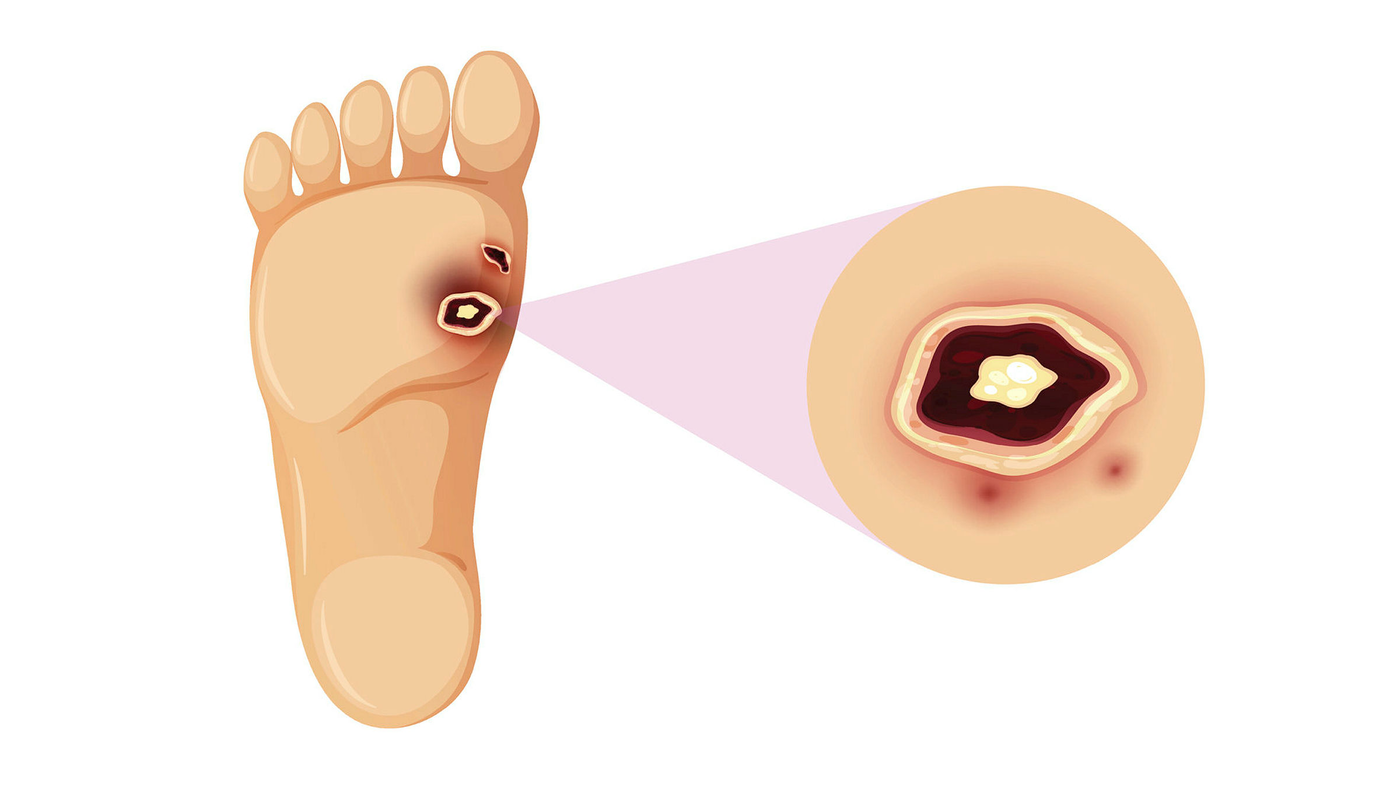
Sår må vurderes før de kan behandles.
Strukturerte vurderinger av sår med TIMES samt vurdering av sårets størrelse, underminering, lokalisasjon, dybde og varighet bør utføres ved hvert bandasjeskift og benyttes av alle som deltar i pasientbehandlingen. Når alt helsepersonell benytter samme struktur, kan vi sammenlikne vurderingene med tidligere funn og avgjøre om behandlingen har effekt.
Sår som oppstår på grunn av skade eller kirurgi, gror som regel i løpet av få dager ved å gå gjennom koagulasjonsfasen, inflammasjonsfasen, proliferasjonsfasen og modningsfasen (1).
Sår som er vanskelige å hele, er de som varer i uker eller måneder og gror dårlig på grunn av grunnlidelser hos pasienten. Andre årsaker kan være hemmende faktorer lokalt i eller omkring såret. De vanligste er venøse leggsår, trykksår, diabetesfotsår og arterielle sår.
Må vurdere såret
Hvis vi skal lykkes med å tilby beste praksis til pasienter med sår, er det viktig at det gjøres en grundig helsevurdering før vi vurderer selve såret og huden omkring. Det første vi må gjøre i all sårbehandling, er derfor å identifisere årsaken til at såret har oppstått, og korrigere de utløsende årsakene (2).
Deretter må vi vurdere og om mulig korrigere systemiske forhold hos pasienten, for eksempel dårlig regulert diabetes eller mangelfull arteriell sirkulasjon, før vi strukturert vurderer såret med TIMES (2, 3). (Se figur 3 senere i artikkelen.)
Denne helhetstenkningen, med oppmerksomhet på både pasientens helsetilstand og lokale forhold i såret, omtales som sårbunnsoptimalisering. Den har til hensikt å få kroppens egne prosesser til å virke positivt inn på sårhelingen (1).
Hjelpemiddel
Akronymet TIMES er utviklet for å gi klinikere hjelp til å strukturere vurderingen og behandlingen av vanskelig helende sår (2), men kan også benyttes for akutte sår. TIMES bør for øvrig brukes sammen med en vurdering av sårets størrelse, underminering (hulrom), lokalisasjon, dybde og varighet (2). (LES: Hva er en sårdiagnose, og hvorfor trenger vi det?) Sår bør vurderes ved hvert bandasjeskift og sammenliknes med tidligere funn for å avgjøre om såret heler (4).
TIMES er enkelt å bruke og kan integreres i de fleste dokumentasjonssystemer (2). Bruk av TIMES kan dermed legge til rette for kontinuitet, oppdaterte behandlingsplaner og redusert helingstid, ikke minst for de pasientene som får behandling fra både spesialisthelsetjenesten og kommunehelsetjenesten samt oppfølging av fastlegen.
Denne artikkelen begrenser seg til å omtale strukturert vurdering med bokstavordet TIMES av selve såret og huden omkring, sårstørrelsen og underminering. Likevel må hovedprinsippet i møte med pasienter med sår alltid være en helhetlig tilnærming til og forståelse av pasientbehandlingen.
Dette er TIMES
Bokstavene i akronymet TIMES har hver sin betydning. T står for «tissue», altså type vev i sårbunnen. I klargjør om det er inflammasjon eller infeksjon i såret. M står for «moisture» og beskriver sårvæsken. E står for «edge», altså sårkantene, og S står for «surrounding skin», altså huden omkring såret.
Ved å benytte TIMES kan helsepersonell ta avgjørelser om behandlingen og avgjøre om de må fjerne dødt vev, hvordan sårvæsken skal håndteres, og hvilke tiltak som kan iverksettes for å behandle eller forebygge eventuelle sårinfeksjoner. I tillegg kan de avgjøre hvordan de kan øke utbredelsen av frisk vev, og hvordan huden omkring såret må beskyttes eller behandles (2) (figur 3) (LES: Slik velger du riktig bandasje)
T – tissue
Hvilken type vev er det i sårbunnen? Vevet i sårbunnen kan beskrives ved å gjengi farger, beskrive strukturen i sårbunnen og forklare hvor stor andel i prosent det er av de ulike vevstypene (2, 5).
Som oftest kan friskt og dødt vev beskrives med fargene svart, grå, gul, hvit, rød og rosa (5). Friskt granulasjonsvev er rødt, mens svart, gult og grått vev indikerer at det er dødt vev i sårbunnen (5). Dødt vev i sårbunnen kan forsinke sårhelingen og gi grobunn for bakterievekst og sårinfeksjon (6). Derfor bør dette vevet fjernes av kvalifisert personell.
Lys rød eller burgunderrød sårbunn som blør lett, kan være tegn på infeksjon eller iskemi (5, 8). Hypergranulert vev er ofte rødt, opphøyd, blankt og blør lett. Det kan også være tegn på infeksjon (7). Lys rosa vev representerer epitelceller, friskt vev, og forekommer når såret er i ferd med å gro (5).
Epitelceller kan vokse fra sårkanten eller som «øyer» i sårbunnen og må ikke mistolkes som oppbløtt hud. Hvis det er mye sekresjon i såret, kan det være vanskelig å oppdage epitelcellene i sårbunnen (5).
I enkelte sår kan knokler (beinvev), ledd og sener være synlige, og det er viktig at funn av synlige bein og sener dokumenteres (3, 5). I de tilfellene der sår er dype og mest sannsynlig går inn mot bein, ledd og sener, er det viktig å vite hva man ser og unngå å feiltolke sener og bein som annen type vev. Feiltolkning av vev kan medføre forsinket henvisning til videre utredning og behandling hos spesialister i sårbehandling (7).
Vanskelig helende sår kan befinne seg i flere sårfaser samtidig, for eksempel både inflammasjons- og proliferasjonsfasen, også kalt nydannelsesfasen. Det at sår befinner seg i flere sårfaser samtidig, er med på å forklare hvordan både friskt og dødt vev kan forekomme samtidig i sårbunnen. Generelt kan vi si at sår som heles, endrer farge fra eksempelvis svart eller gult til å bli rødt og rosa før såret lukker seg med lys rosa arrvev (5).
Fargebeskrivelser av vevet alene er ikke nok for å vurdere vev i sår. Derfor bør vi i tillegg vurdere og dokumentere vevenes struktur eller oppbygging. Vevet kan beskrives som fuktig, mykt, læraktig eller hardt (5). Ettersom fuktig, dødt vev som regel behandles ulikt et tørt, dødt vev, er vurderinger av vevets struktur avgjørende for å sikre pasienter med sår beste praksis.
Ved gjentatte vurderinger kan vi følge med på om prosentandelen friskt eller dødt vev øker eller minsker. En økning i prosentandelen friskt granulasjonsvev i forhold til dødt vev kan bety at såret heler.
I – infection
I – er det infeksjon eller inflammasjon? Akutte sår gror som tidligere nevnt i løpet av få dager ved å gjennomgå fire overlappende faser: koagulasjonsfasen, inflammasjonsfasen, proliferasjonsfasen og modningsfasen (1). Inflammasjonsfasen er derfor en naturlig del av sårhelingen fordi den bidrar til å reparere skadet vev, men vanskelig helende sår kan stagnere i inflammasjons- og proliferasjonsfasen.
I inflammasjonsfasen øker blodgjennomstrømmingen til det skadede vevet. Høyere temperatur, ødemer, smerte og moderate til store mengder sårvæske kjennetegner inflammasjonsfasen. Enkelte symptomer i inflammasjonsfasen likner dermed på infeksjonstegn, men det er viktig å klargjøre om såret er i inflammasjonsfasen, eller om det er en sårinfeksjon, fordi behandlingen er ulik.
Sårinfeksjon beskrives ofte som en sammenhengende linje fra kontaminering, kolonisering og sårinfeksjon til systemisk infeksjon og biofilm, som er en slimaktig overflate i såret som består av mikroorganismer (8).
Så godt som alle åpne sår er kontaminerte, enten av egen normalflora (endogen) eller av ytre (eksogen) smitte. Kontaminerte sår er derfor svært vanlige, men mikrobene har ikke forårsaket lokal infeksjon.
Det er flere forhold, både hos pasienten og i såret, som kan gi kolonisering og sårinfeksjon. Vanskelig helende sår er som regel betydelig kolonisert med bakterier på grunn av dårlig blodsirkulasjon og fordi såret har vart over tid (2). Om såret blir infisert, forsinkes sårhelingen (8) (figur 1).
Risikoen for sårinfeksjon øker blant annet ved dårlig regulert diabetes, venøs hypertensjon, hjertesvikt og underernæring (4, 8, 11). Faren for sårinfeksjon øker også når inflammasjonsfasen varer over tid, slik vi ser ved vanskelig helende sår (10).
Hvis vi tar utgangspunkt i sårbunnen og T-en i TIMES, så vet vi at tilstedeværelse av dødt vev, nekrose, kan øke bakteriemengden og dermed også øke risikoen for sårinfeksjon (10). Faren for sårinfeksjon kan derfor altså øke på grunn av systemiske og/eller lokale forhold i såret.
Biofilm er ikke nødvendigvis synlig, og derfor bør man mistenke biofilm i sår som ikke gror til tross for optimal behandling (8) (LES: Dette må du vite om biofilm). Ettersom enkelte mikroorganismer kan skape biofilm og sårinfeksjoner i selv små mengder, kan både typen og mengden bakterier avgjøre sykdomsbildet (8).
Det kan være utfordrende å oppdage sårinfeksjon i vanskelig helende sår fordi de klassiske infeksjonstegnene, slik som varme, rødme, hevelse, lukt og smerte, ikke nødvendigvis er til stede. Noen ganger er tegnene så vage at det kan være vanskelig både for pasienten og helsepersonellet å oppdage sårinfeksjonen, ikke minst hos personer med diabetesfotsår (11).
Sårinfeksjon uten tydelige eller typiske infeksjonstegn øker faren for amputasjoner og systemisk infeksjon. Som helsepersonell er det viktig å være klar over forskjellen på infeksjonstegn i henholdsvis akutte og vanskelig helende sår samt det faktumet at infeksjonstegn kan være vage (figur 1).

M – moisture
Produksjon av sårvæske er en naturlig reaksjon ved vevsskade (12). Det produseres for øvrig ulike mengder sårvæske i de ulike sårfasene. Det produseres mest i inflammasjonsfasen når kapillærene utvider seg og blir mer gjennomtrengelige for ulike stoffer og celler som skal bidra til å reparere vevsskaden.
Generelt avtar mengden sårvæske når såret heles, men i vanskelig helende sår kan det forekomme store mengder sårvæske over tid fordi de er lenge i inflammasjonsfasen (12).
Vurdering av sårvæske eller fuktighet i såret faller inn under M-en i TIMES, og både mengde, farge, konsistens og lukt bør vurderes. Helsepersonell benytter ofte svært subjektive beskrivelser for mengden av sårvæske, for eksempel lite, middels og mye sårvæske. Andre benytter +, ++ og +++ for å angi volumet, men felles for disse kategoriene er at helsepersonell kan ha ulik forståelse av dem.
En metode som antakelig er bedre, er å angi mengden sårvæske basert på hvor ofte bandasjen skiftes, hvor gjennomtrukket bandasjen er når den fjernes, og hvor påvirket huden omkring såret er av sårvæsken når bandasjen fjernes (13). Oppbløtt hud rundt vanskelig helende sår er et av de vanligste hudproblemene vi ser i klinisk praksis (2).
Sårvæskens farge kan være serøs (vannaktig), hvit, gul, grønn, rosa eller lys rød (5). Lys klar eller serøs væske er ikke uvanlig rett etter at såret har oppstått, og er normalt i små mengder. Fargeforandringer kan bety en forverring av sårets tilstand. Grønn sårvæske ser vi typisk ved infeksjoner forårsaket av bakterien Pseudomonas aeruginosa, mens rødlig sårvæske gir mistanke om blod i sårvæsken (13).
Ved blodig sårvæske må man vurdere om bandasjen eller andre faktorer kan ha skadet sårbunnen og forårsaket blødningen. Sårvæskens konsistens påvirkes av mikroorganismer og kroppsceller, og hvis sårvæsken er tykk, bør man mistenke en infeksjon.
Ifølge Schultz og medarbeidere er sårets varighet også av betydning når sårvæsken vurderes fordi sårvæsken i akutte sår fremmer sårhelingen, mens sårvæsken i vanskelig helende sår hemmer sårhelingen (1). Sårets plassering og størrelse kan for øvrig påvirke både mengde og konsistens. Hvis pasienter har store sårflater, for eksempel på en legg der det i tillegg er ødemer, kan det gi betydelige mengder sårvæske.
Fuktig sårbehandling er å anse som standardbehandling til vanskelig helende sår, og derfor må man unngå at sårbunnen tørker ut. En utfordring i sårbehandlingen kan være å sikre balansen mellom å holde sårbunnen tilstrekkelig fuktig for å fremme sårheling, og samtidig unngå at den blir for fuktig (13).
Når vi vurderer sårvæsken, er det viktig å vurdere om sårvæsken kan være påvirket av pågående behandling. Enkelte bandasjer, for eksempel de som inneholder jod eller sølv, kan gi brun eller gråfarget sårvæske (13). Når vi vurderer lukt fra såret, må vi også vurdere om lukten kan være påvirket av pågående behandling og ikke bare selve såret.
E – epitel
Synlige epitelceller i sårkantene indikerer at såret er i heling (2). Det er flere forhold som kan gi tørr hud rundt såret, blant annet iskemi og nevropati. Tørr hud kan forsinke sårhelingen fordi produksjonen av friske epitelceller er hemmet uten fuktighet (2).
Tørr, hard og opphøyd hud, kallus, oppstår ofte rundt diabetesfotsår. Hvis kallus ikke fjernes regelmessig av kyndige klinikere, bidrar det til forsinket heling (11). Ikke sjelden ses ødemer i sårkantene, og en medvirkende årsak er inflammatoriske faktorer.
Oppbløtt hud rundt såret er som tidligere nevnt et av de viktigste problemene i sårkantene. Også slike forhold hemmer sårtilhelingen.
S – surrounding skin
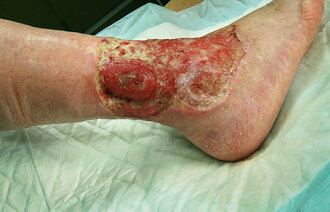
Hudproblemer følger ofte vanskelig helende sår, og huden kan være tørr, oppbløtt, oppskrapet, inflammert, ødematøs eller ha eksem (2). Flere forhold kan være til stede samtidig i huden, og i tillegg kan vi ofte se fargeforandringer, hyperpigmentering, hos personer med venøse leggsår. Ødemer ses ofte hos personer med leggsår, og ødemene kan virke negativt inn på sårhelingen.
Sårvæsken kan skade huden slik at den blir irritert og inflammert, og kontaktdermatitt er ikke uvanlig (6). Inflammasjon i huden kan også oppstå på grunn av allergi mot bandasjer, kompresjonsbind, kremer og salver.
Eksem i huden kan oppstå hos enkelte pasienter, spesielt hos dem med venøse leggsår. Ettersom oppbløtt eller oppskrapet hud, kontaktdermatitt, allergisk dermatitt, tørr hud og eksem krever ulike behandlinger, er det viktig å avklare hudens tilstand når vi vurderer vanskelig helende sår.
Underminering og dybde
Underminering innebærer at det er hulrom, tunneler eller ganger under huden. I praksis betyr det at huden over hulrommet ikke er festet til underliggende vev (5, 14). Årsaken til underminering er stort sett oppvekst av bakterier og/eller infeksjon der fettvevet har gått tapt (5).
Lokalisasjonen av undermineringen kan beskrives ved hjelp av en klokkeskive der vi kan angi hulrom for eksempel mellom klokka 12 og 3 eller 8 og 9 (2, 5, 15) (figur 2). For å angi riktig lokalisasjon av undermineringen kan 12-tallet plasseres mot hodet og 6-tallet mot føttene når vi bruker klokkeskiven.

Omfanget av underminering kan undersøkes med en steril pinne og angis i antall millimeter eller centimeter (14). I sår med underminering kan sårets egentlige omfang eller overflate være betydelig større enn det vi ser på hudoverflaten. Derfor er det klinisk viktig å vurdere underminering (14).
Hvis hulrommet inneholder dødt vev, må vi vurdere om det er sannsynlig at huden vil feste seg til underliggende vev, eller om huden over hulrommet skal fjernes av ansvarlig lege (5).
Når vi vurderer underminering, er det naturlig at vi også vurderer og dokumenterer sårets dybde. Det gjøres ved hjelp av den samme sterile pinnen som vi benytter ved vurdering av underminering (15).
Sårstørrelse
Både lengde, bredde, omkrets og areal kan benyttes for å vurdere sårets størrelse og bør måles ved første konsultasjon og deretter jevnlig (15). En vurdering med TIMES anbefales brukt ved hvert bandasjeskift, men måling av sårstørrelsen kan gjøres hver andre til fjerde uke (15). En reduksjon i sårets størrelse er en indikasjon på at såret heler (5).
Sårets lengde og bredde kan måles ved å benytte en papirlinjal som kan kastes etter bruk. Arealet regnes ut ved å benytte den lengste og bredeste målingen av såret, og det angis i cm². Vi bør imidlertid være klar over at en slik enkel metode kan gi variasjoner i målingene (15).
Alternativt kan vi tegne såret av på gjennomsiktig plast med rutenett, der vi så kan regne ut sårets areal i cm². Tegningen av sårets areal kan fotograferes og kombineres med tekst for å sikre god dokumentasjon. Før vi fotograferer plastfilmen, kan vi tegne prosentandelen av de ulike typene av vev i sårbunnen på plastfilmen, slik at den inngår i dokumentasjonen (15).
Hvis man ønsker å benytte bildedokumentasjon, bør en papirlinjal legges ved siden av såret, slik at det er enklere å vurdere sårets størrelse ut fra bildet. Det finnes ulike digitale løsninger for å måle sårets størrelse, men foreløpig er det få digitale løsninger som benyttes i klinisk praksis.

Avslutning
Ved å vurdere TIMES, sårstørrelse og underminering kan vi ta stilling til hvorvidt behandlingen som er iverksatt, gir bedring. Når en slik strukturert tilnærming benyttes av alt helsepersonell og integreres i dokumentasjonssystemet, kan vi legge til rette for kontinuitet i pasientbehandlingen.
Hvis vi ikke ser bedring i sårets tilstand i løpet av to til fire uker etter at optimal behandling er igangsatt, må vi revurdere behandlingen og bedømme om pasienten skal henvises til en eller flere spesialister (16).
Sykepleien har utviklet et digitalt verktøy for sårvurdering basert på TIMES – prøv det her.





































0 Kommentarer