Sårhelingsprosessen – enkelt forklart

Det er viktig å forstå helingsprosessen, også når et sår ikke gror.
Sårhelingsprosessen er grunnlaget for å forstå hva som skjer når et sår gror, men den er også viktig for å forstå hva som skjer når et sår ikke gror. Prosessen er komplisert og deles inn i ulike faser. Hvordan såret behandles, styres blant annet av hvilken fase såret er i.
På mennesket kan sår og skader hele på to ulike måter, enten ved regenerasjon eller ved reparasjon (1). Regenerasjon betyr at vevet heler til tilstanden det var i før skaden oppsto, mens reparasjon betyr at skaden leges, men det dannes arr.
Dersom skaden kun innebærer skade på epidermis og øvre del av dermis, kan kroppen regenerere skaden. Eksempler på dette er annengrads brannsår, annengrads dekubitus og gnagsår. Er skaden dypere enn dermis, vil skaden bli reparert (1).
Dersom det utføres operasjon på et foster intrauterint, vil skaden uansett regenerere dersom operasjonen er før 22.–24. svangerskapsuke. Etter dette mister fosteret evnen til å regenerere skader dypere enn dermis (2).
Sårhelingsprosessen
Det er vanlig å dele sårhelingsprosessen inn i ulike faser. En måte å forstå sårheling på, er å dele den inn i to faser: en fase der det primært foregår opprenskning og reparasjon, og en fase der vevet heler (2).
Et sår som blir ikke-helende, stanser i den første fasen og kommer ikke videre. I den opprenskende fasen kan vi som sårbehandlere bidra aktivt med å rengjøre og debridere såret. I helingsfasen, derimot, skal såret ha ro, fuktighet og sjeldne skift. Debridering skal bare unntaksvis gjennomføres.
Det vanligste er imidlertid å dele sårhelingen inn i fire faser. Heretter tar vi derfor utgangspunkt i sårhelingens fire faser (2):
- koagulasjonsfasen
- inflammasjonsfasen (rengjøringsfasen)
- proliferasjonsfasen (nydannelsesfasen)
- modningsfasen
Koagulasjonsfasen
Når skade oppstår, enten på grunn av et planlagt, kirurgisk inngrep eller som et resultat av en skade, vil kroppen umiddelbart forsøke å stanse blødningen. Blodkarene kontraherer, og blodplater strømmer til det skadede stedet for å stanse blødningen. Blodplatene lager en plugg som tetter skadede blodkar.
I det videre forløpet av koagulasjonsprosessen dannes det en mer solid plugg bestående av fibrin. Allerede i denne fasen frigis det vasoaktive stoffer, som histamin, samt vekstfaktorer. Vekstfaktorer er signalmolekyler som styrer og koordinerer reparasjonsprosessen.
Som en konsekvens av skaden på blodkar reduseres blodforsyningen til området. Denne reduksjonen fører til relativ hypoksi i såret og området rundt. Denne hypoksien har en signalfunksjon og informerer kroppen om at det er oppstått skade, og at reparasjonsprosessen må starte (3). Når den relative hypoksien opphører, stopper sårhelingsprosessen opp.
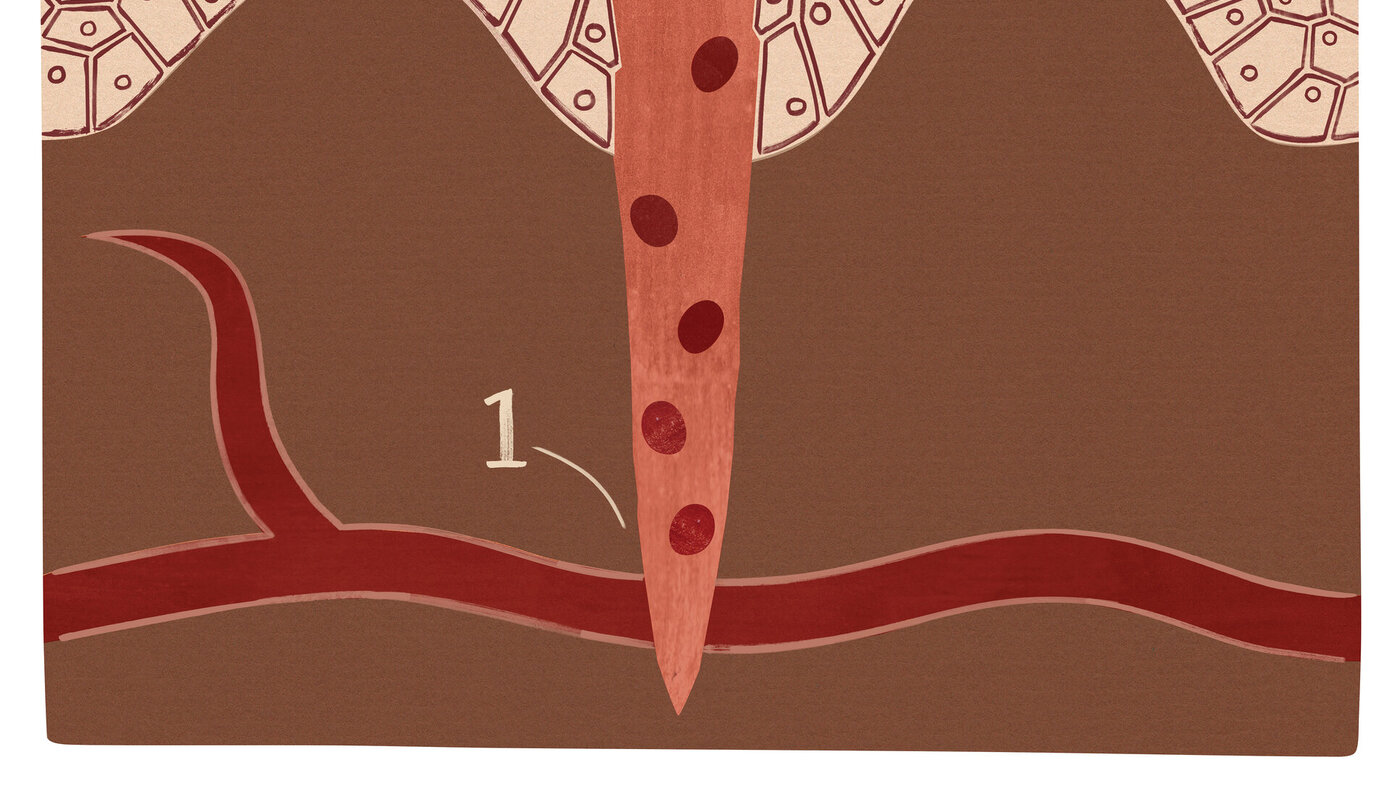
Inflammasjonsfasen
Denne fasen kalles også rengjøringsfasen. Når blødningen er stanset, kan kroppen starte opprenskningen i såret. Da trengs det mer blod. Blodkarene utvider seg og blir utette. Det siver ut væske fra blodkarene (4). Denne endringen i blodkarenes funksjon skjer som følge av økt tilgang på mastceller og dermed også histamin.
Alle som har vært gjennom et kirurgisk inngrep, vet at på den første postoperative dagen blir området rundt suturene rødt og hovent. Det er et signal om at opprenskningen og reparasjonen har startet.
Store mengder hvite blodlegemer kommer til området, særlig granulocytter og makrofager, men også noen lymfocytter. Granulocyttene skal angripe mikrober som befinner seg i sårområdet. Granulocytter gjenkjenner bakterier som inntrengere og dreper mikroorganismene. Makrofagene renser såret for rester etter celleskade og bakteriedrap.
Begge celletypene styrer sårhelingen og produserer vekstfaktorer, cytokiner (signalmolekyler som fremmer inflammasjon) og proteinaser (blant annet MMP, matriks metalloproteinaser) (5). Proteinasene løser opp skadet vev, men også overskytende bindevev som lages under reparasjonsprosessen.
Når dødt vev er løst opp, veksten og utbredelsen av bakterier er under kontroll og det foreligger en ren sårflate, starter første delen av oppbyggingen. Oppbyggingen av vevet forutsetter bedre tilgang på oksygenrikt blod. For å oppnå dette, stimulerer makrofagene, via utskillelse av cytokiner, til dannelse av nye blodkar (angiogenese). Nye blodkar skal erstatte de skadede karene.
Angiogenesen er i tillegg en forutsetning for at det skal dannes granulasjonsvev. Fibroblastene, celler som produserer kollagen og elastiske fibre, danner kollagen type III, som fylles i såret. Dette kollagenet er midlertidig og blir erstattet av mer fullverdig kollagen av type I senere i forløpet (1).


Proliferasjonsfasen
Denne fasen kalles også nydannelsesfasen. I denne fasen skal det skadede sårområdet fylles opp. De nye blodkarene og kollagenet er allerede nevnt, men fibroblastene danner også grunnsubstans, som fyller sårhulen (2).
De nye blodkarene og grunnsubstansen er forberedelse til å danne granulasjonsvev. Grunnsubstans og bindevev er helt avgjørende for dannelsen av epitelvev, som etter hvert skal gro over såret.
Granulasjonsvevet består av forskjellige typer celler, slik som fibroblaster, celler som har evnen til å lage ulike typer vev (blant annet kapillærer, nerver og fettvev), samt immunceller (lymfocytter, makrofager og granulocytter).
Friskt granulasjonsvev uten skader gir god beskyttelse mot bakteriell infeksjon. Derfor er det viktig å behandle dette vevet med forsiktighet. Kompresser som setter seg fast i såret, skader granulasjonsvevet når bandasjene fjernes, noe som gir økt risiko for infeksjon (4).
Når såret er fylt med granulasjonsvev, kan epiteliseringen starte. Keratinocyttene danner hudceller, som vokser inn fra kantene. Når det foreligger en delhudsskade, kan epitel også vokse ut fra rester av sårsekker, talgkjertler og svettekjertler. Forutsetningen for at epitelet skal kunne vokse, er at granulasjonsvevet ikke er for svullent.
Når granulasjonsvev blir for stimulert, dannes det hypergranulasjonsvev (1). Dette er vev som er hovent og lettblødende, og som vokser høyere enn sårkanten. Det er ikke mulig for epitelvevet å vokse inn over det hovne vevet. Hypergranulasjon må derfor behandles før det er mulig å oppnå fullstendig epitelisering av såret.

Modningsfasen
Såret lukkes nå ved hjelp av to mekanismer. Den ene er sammentrekning (kontraksjon) av såret (1). Da trekker sårkantene seg sammen, og arealet som skal fylles med granulasjonsvev og epitel, blir redusert. Myofibroblastene er ansvarlige for denne delen av sårlukkingen.
Den andre mekanismen er arrdannelse. Såret fylles med et tynt lag epitel over den resterende sårflaten. Hud har et høyt innhold av kollagen, og denne typen vev trenger lang tid for å oppnå tilfredsstillende styrke. Vi regner at styrken i dette vevet aldri kommer over 85 prosent av normal styrke, og det tar 6–12 måneder å oppnå denne styrken (2).
Det første kollagenet erstattes da med mer funksjonelt kollagen (kollagen type I), som er med på å bygge styrken i vevet. MMP er involvert i denne prosessen ved å bryte ned overflødig og midlertidig kollagen (6). Det er denne prosessen som tar så lang tid. Mens tarmen, som har lite kollagen, har normal styrke etter ti dager, trenger huden et år på å oppnå tilnærmet opprinnelig styrke.
Over tid vil også arrvevet skrumpe, noe som i de fleste tilfeller er gunstig. Unntaket er blant annet sirkulære sår rundt armen, foten eller på kroppen – da kan arrskrumpningen føre til redusert funksjonalitet. Arrets farge endres også fra rødt til hvitt. Arrvevet er uten talg- og svettekjertler, og det mangler melanocytter, så det danner ikke pigment. Arr skal derfor beskyttes mot sterkt sollys.
Noen ganger slutter ikke kroppen å danne arr; vi får det som kalles et hypertrofisk arr. Arret fortsetter da å vokse en tid etter at såret er lukket. Hypertrofisk arr vil etter hvert minke igjen, og etter et år vil arret være tilnærmet normalt. Det foreligger ikke noen god forklaring på hvorfor det dannes hypertrofiske arr, men vi vet at dype brannsår, infiserte sår med forlenget helingsfase og sår i områder med stort strekk og drag på såret har høyere risiko for å danne hypertrofiske arr (1).
En annen variant er keloide arr. Disse arrene er også hypertrofiske, men de vokser ut over området der det engang var sår. Arret blir større enn det opprinnelige såret (1). Det er ulike mekanismer bak disse to fenomenene. Hudtype 6 (mørk hud) har større risiko for å utvikle keloide arr enn lysere hudtyper.

Referanser
1. Martin M. Physiolgy of wound healing. I: Flanagan M, red. Wound healing and skin integrity. 1 utg. West Sussex: Wiley-Blackwell; 2013.
2. Langøen A, Gürgen M. Sårbehandling, generelle prinsipper. I: Langøen A, red. Sårbehandling og hudpleie. 5 utg. Oslo: Gyldendal Akademisk; 2018.
3. Chambers AC, Leaper DJ. Role of oxygen in wound healing: a review of evidence. J Wound Care. 2011;20(4):160–4.
4. Melby BØ. Sårhelingsprocessen. I: Bermark S, Melby BØ, red. Sår og sårbehandling. København: FADL; 2017.
5. Young A, McNaught C-E. The physiology of wound healing. Surgery (Oxford). 2011;29(10):475–9.
6. Caley MP, Martins VL, O'Toole EA. Metalloproteinases and wound healing. Adv Wound Care (New Rochelle). 2015;4(4):225–34.
Sykepleien har utviklet et digitalt verktøy for sårvurdering basert på TIMES.




































0 Kommentarer