Smerter etter brystkreftbehandling kan vare i årevis
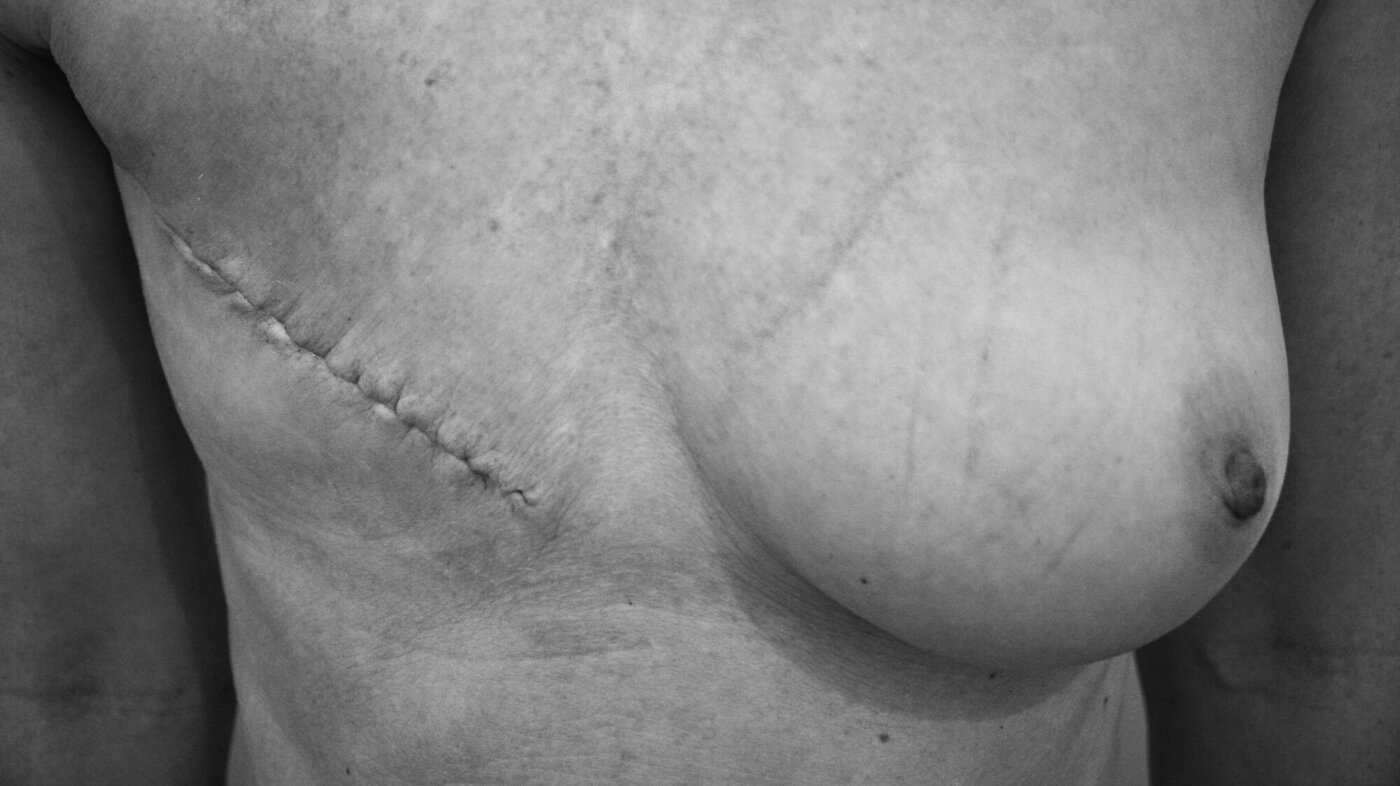
Kvinner opplever at smerter etter brystkreftbehandling varer i måneder eller år. Forebygging og behandling av slike seneffekter er mangelfull.
Kronisk smerte etter brystkreftbehandling er et lite anerkjent helseproblem. 41 prosent av kvinner opplever kronisk smerte etter brystkreftbehandling i Norge. Årsakene er sammensatt for denne pasientgruppen, men smertene er ofte nevropatiske.
De siste tiårene har det vært en økning i forekomsten av brystkreft. I Norge er 90 prosent av pasientene i live fem år etter avsluttet behandling (1). Behandling av brystkreft innebærer operasjon, enten brystbevarende kirurgi eller fjerning av brystet. Fjerning av brystet gjøres med eller uten rekonstruksjon, fjerning av sentinel node og/eller fjerning av fettvevet med lymfeknuter i armhulen.
De aller fleste vil i tillegg til operasjon få en eller flere former for tilleggsbehandling som stråleterapi, cellegift, endokrinbehandling, trastuzumab (antistoffer som reduserer risiko for tilbakefall) eller zoledronsyre (bisfosfonat som reduserer risikoen for utvikling av osteoporose og bedrer prognosen).
Seneffekter etter kirurgi og behandling for brystkreft kan være av både fysisk, psykisk og sosial art, eller en blanding av flere (2). Noen seneffekter kan komme raskt etter behandling, andre seneffekter kan være vanskeligere å tidfeste, mens noen kan komme etter flere år.
Seneffekter som er observert hos kvinner behandlet for brystkreft er smerte, fatigue, menopausale plager, vektøkning, lymfødem, søvnproblemer, seksuelle plager og lavt stoffskifte (hypothyreose). Seneffekter som påvirker hjertets funksjon, er også observert: rytmeforstyrrelse, dysfunksjon i venstre ventrikkel, betennelser (myo- og perikarditt) og annen sykdom i hjertemuskelen (kardiomyopati) og hjertesvikt. Andre seneffekter er kognitiv dysfunksjon, angst og depresjon (3). Denne artikkelen handler om kronisk smerte.
Kronisk smerte
Ifølge International Association for the Study of Pain (IASP) er smerte en ubehagelig sensorisk og emosjonell opplevelse som følge av faktisk eller potensiell vevsødeleggelse. Smerte er alltid subjektiv. IASP skiller mellom akutt og kronisk smerte. Kronisk smerte defineres som smerte med varighet på minst tre til seks måneder eller mer (4).
De fleste kvinner forventer å oppleve en viss grad av smerte etter en brystkreftoperasjon og at den skal gå over etter noen dager eller uker (5). Imidlertid opplever en del at smerten vedvarer i flere måneder eller år, eller at de en stund etter behandlingen får smerter som kommer og går eller vedvarer i flere år. Mye usikkerhet og redsel er knyttet til smerte.
Smerte kan også føre til insomnia, depresjon, fatigue og dårligere seksualitet samt redusert livskvalitet (2). I verste fall kan smerten medføre at kvinnen blir helt eller delvis uføretrygdet. En norsk studie fant at den hyppigste årsaken til uføretrygd hos brystkreftopererte var skulder- og armplager (6).
Prevalensen med kronisk smerte etter brystkreftoperasjon og behandling varierer fra 25 til 60 prosent (7). Den store variasjonen skyldes hovedsakelig ulikheter i hvordan kronisk smerte defineres i studiene, ulik studiedesign, samt hvilke instrumenter som har vært benyttet for å kartlegge smerte.
I en dansk (8) og en norsk (9) studie fant man at prevalensen av kronisk smerte var henholdsvis 47 prosent ett til tre år etter operasjon og 41 prosent to til seks år etter operasjon. Begge studiene hadde brukt en numerisk skala (NRS) (0–10) for å måle intensiteten på smerte. I begge studiene satt man en skår ≥8 som definisjon på sterke smerter. I den danske studien rapporterte 13 prosent av pasientene med smerter at de hadde sterke smerter (8). Til sammenlikning fant forskerne i den norske studien at 8 prosent av pasientene med smerter rapporterte om sterke smerter (9).

Lokalisasjon av smerte
De hyppigste lokalisasjonene for kronisk smerte etter brystkirurgi er smerter i det opererte brystområdet (60–86 prosent), fulgt av smerter i aksillen (48–63 prosent) og arm (29–57 prosent) (8, 9). Andre lokalisasjoner for kronisk smerte kan være skulder, nakke, fingre, tær og ledd (8, 9).
Pasienter som har gjennomgått aksilledisseksjon, er mest utsatt for å få skulder- og armsmerter, i tillegg kan cirka 15–20 prosent få lymfødem, som kan være smertefullt (10). Også blant dem som kun har utført sentinel node-disseksjon, er det rapportert om smerte i skulder og arm hos 8 prosent av pasientene, samt lymfødem i 3,5 prosent av tilfellene etter to år (11).
Taxaner (cellegift) som brukes i behandling av brystkreft hos noen pasienter, gir hyppig perifer nevropati, men dersom nevropatien vedvarer, vil den gradvis bli redusert til et nivå som ikke påvirker pasientens livskvalitet etter tre til tretten år (12). For kvinner med østrogenreseptorpositive svulster anbefales østrogenantagonistbehandling (tamoxifen eller aromatasehemmere, AH) i fem til ti år etter operasjon (13).
Vanlige bivirkninger ved endokrinbehandling er hetetokter, vektøkning, insomnia og tørrhet i vagina, som medfører at samleie oppleves som smertefullt. Leddsmerter og muskelsmerter er mest uttalt hos dem som bruker AH (14). Pasienter som seponerer AH før anbefalt behandlingslengde, oppgir ofte ledd- og/eller muskelsmerter som årsak til at de slutter med AH (14).
Kronisk smerte som skyldes kirurgi, kan være nociceptiv eller nevropatisk. Nociseptive smerter er forårsaket av skade på kroppsvev, for eksempel kuttskader, og går som regel over når skadet vev er tilhelet. Nevropatisk smerte kan vedvare og defineres som smerte som oppstår som en direkte konsekvens av en lesjon eller sykdom som affiserer det sentrale eller perifere somatosensoriske nervesystemet (15). Jung og medarbeidere (16) har klassifisert nevropatisk smerte som kan oppstå etter brystkreftkirurgi, i fire typer:
1. Fantombrystsmerter etter fullstendig fjerning av brystet (radikal mastektomi).
2. Post mastectomy pain syndrom (PMPS) er smerte og sensoriske forandringer i brystveggen, aksillen og proksimalt i overarmen, som har vart i mer enn tre måneder. PMPS kan forekomme hos kvinner som har fått gjort mastektomi eller brystbevarende kirurgi, og forårsakes oftest av skade på nerver som ligger mellom ribbena, og som går ut i armen (interkostale brachialisnerver) (8).
3. Nevromsmerter: Nevromer er primært sammenfiltrede axoner som ikke er i stand til å regenerere. De kan oppstå i arrvev.
4. Andre typer nervesmerter: Disse inkluderer PMPS-liknende smerter uten aksilledisseksjon eller tilstander som er et resultat av kirurgisk skade av nervus thoracicus longus, nervus thoracodorsalis eller pektoralnervene.
Risikofaktorer
Studier som har identifisert hva som kjennetegner brystkreftoverlevere med kronisk smerte, har kommet frem til varierende resultater. Dette kan skyldes ulik definisjon av kronisk smerte, forskjellige instrumenter som ble benyttet til å kartlegge kronisk smerte, studiets design, tidsperspektivet, utvalgets størrelse samt hvilke faktorer som ble vurdert.
Flere studier viser at unge kvinner (<50 år) (7, 8, 9) og kvinner som har gjennomført aksillær lymfeknutedisseksjon (6, 7, 17), har økt risiko for utvikling av kronisk smerte.
Av studiene som tok for seg adjuvant behandling, fant flere at adjuvant strålebehandling, men ikke kjemoterapi, økte risikoen for kronisk smerte (8, 17). To av studiene fant imidlertid at det var kombinasjonen av aksilledisseksjon, strålebehandling og kjemoterapi som økte risikoen for kronisk smerte (9). I studiene som undersøkte om overvekt (BMI > 25) var en risikofaktor for kronisk smerte, fant noen studier en sammenheng (7), mens andre studier ikke fant noen sammenheng mellom høy BMI og kronisk smerte (9).
Preoperativ smerte på grunn av andre smertefulle tilstander, som for eksempel leddgikt, ryggsmerter, fibromyalgi (9, 17) og postoperativ smerte (17), er identifisert som risikofaktorer for utvikling av kronisk smerte. I en befolkningsstudie er de samme variabler som nevnt over også funnet å være risikofaktorer for kronisk smerte etter kirurgi generelt (18), samt i oversiktsartikler om kronisk smerte etter kirurgi (19, 20).
Hvorfor kronisk smerte før kirurgi og sterke smerter etter kirurgi er assosiert med høyere risiko for kronisk smerte, er fortsatt uklart. Det kan kanskje skyldes helsetilstanden før man ble syk, altså en genetisk disposisjon for begge typer smerte. Pasienter som opplever mye angst og depresjon før kirurgi, opplever sterkere smerte etter operasjon enn pasienter med lite angst og depresjon (20). Det er blitt hevdet at angst og depresjon trolig gir økt risiko for utvikling av kronisk smerte (21). Hvorvidt angst eller depresjon er en risikofaktor for utvikling av kronisk smerte etter brystkreftkirurgi, er fortsatt uklart (9).
Smerte opptrer sjelden alene. Flere studier har vist at smerte, fatigue og depresjon utgjør et konsistent «cluster», ofte kombinert med søvnforstyrrelse (22). Nyere forskning viser at symptomene smerte, fatigue og depresjon har felles biologiske markører inkludert genetiske, immunologiske og/eller hormonelle faktorer (23).
Hvordan forhindre smerte?
Inntil år 2000 ble alle pasienter i Norge med brystkreft operert med aksilledisseksjon. Som følge av endrete retningslinjer for hvem som trenger denne operasjonen, er det nå bare cirka 20 prosent av alle med brystkreft som trenger dette inngrepet i aksillen.
I tillegg opereres nå stadig flere med brystbevarende operasjon. Hele 82 prosent av pasienter med svulster under 30 mm fikk brystbevarende operasjon i Norge i 2015 (24). Det er grunn til å tro at mer brystbevarende kirurgi og mindre aksilledisseksjon vil kunne redusere forekomsten av kronisk smerte etter brystkreftoperasjoner.
Videre er det viktig å påse at alle pasienter som har fått gjort en aksilledisseksjon, får rekvisisjon til fysioterapeut og gjøres oppmerksom på egentrening for å unngå skulder- og armsmerter.
God smertelindring postoperativt av nociceptive, inflammatoriske og nevropatiske smerter antas å redusere risikoen for kronisk smerte (19). I tillegg vil god smertelindring i den postoperative fasen redusere smerteindusert immobilisering og muliggjøre raskere mobilisering og rehabilitering av bevegelsesfunksjoner (25).
Ut fra litteraturen om kronisk smerte generelt vet vi at immobilisering øker risikoen for langvarig nevropatisk smerte (19). Pasienter bør oppmuntres til å være fysisk aktive, da det ser ut til at fysisk aktivitet beskytter mot å utvikle smerte gjennom å aktivisere smertereduserende mekanismer (26).
Pasienter bør informeres om betydningen av å være godt smertelindret postoperativt. De bør altså ikke vente til de har veldig vondt før de bruker smertestillende. Alle pasienter bør få en resept på smertestillende medikamenter før operasjon, slik at de har smertestillende medikamenter tilgjengelig når de utskrives fra sykehuset.
Kvinner som opplever smerte ved samleie grunnet tørre slimhinner, kan bruke Replens MD vaginalgel, som er et hormonfritt langtidsvirkende legemiddel som styrker slimhinnen i skjeden.
Pasienter som har blitt behandlet for brystkreft, skal kontrolleres i ti år (27). Det er viktig at helsepersonell etterspør om pasienten har smerter, samt smertens alvorlighetsgrad på rutinekontrollene. Pasienter med alvorlige smerter bør henvises til en smerteklinikk eller smerteekspert.
Konklusjon
41 prosent av kvinner opplever kronisk smerte etter brystkreftbehandling i Norge. Som oftest er smerten nevropatisk. Selv om vi i dag vet mer om årsakene og mekanismene som fører til kronisk smerte, samt hvilke pasienter som er i risikogruppe for å utvikle kronisk smerte, er forbygging og håndtering av smerte mangelfull.
Referanser
1. Kreftregisteret. Cancer in Norway. Cancer incidence, mortality, survival and prevalence in Norway. Oslo: Kreftregisteret; 2016. Tilgjengelig fra: https://www.kreftregisteret.no/globalassets/cancer-in-norway/2016/cin-2106.pdf (nedlastet 02.10.2018).
2. Fosså SD, Loge JH, Dahl AA, red. Kreftoverlevere. Ny kunnskap og nye muligheter i et langtidsperspektiv. Oslo: Gyldendal Akademisk; 2009.
3. Bodai BI, Tuso P. Breast cancer survivors: a comprehensive review of long-term medical issues and lifestyle recommendations. Perm J. 2015;19(2):48–79.
4. Merskey H, Bogduk N. Classification of chronic pain descriptions of chronic pain syndromes and definitions of pain terms. 2nd ed. Seattle: WA: IASP Press; 1994. Tilgjengelig fra: https://pdfs.semanticscholar.org/281f/3f5476d2444bb53553f473ec83634e090ee2.pdf
5. Hovind IL, Bredal IS, Dihle A. Women’s experience of acute and chronic pain following breast cancer surgery. JCN. 2013;22:1044–52.
6. Fisman K, Stanghelle JK. Rehabilitation of women with breast cancer; five year follow-up. Tidsskrift for Den norske legeforening. 2007;127(9):1207–9.
7. Macdonald L, Bruce J, Scott NW, Smith WC, Chambers WA. Long-term follow-up of breast cancer survivors with post-mastectomy pain syndrome. Br J Cancer. 2005;92:225–30.
8. Gartner R, Jensen MB, Nielsen J, Ewertz M, Kroman N, Kehlet H. Prevalence of and factors associated with persistent pain following breast cancer surgery. JAMA. 2009;302:1985–92.
9. Schou Bredal I, Smeby NA, Ottesen S, Warncke T, Schlichting E. Chronic pain in breast cancer survivors: comparison of psychosocial, surgical and medical characteristics between survivors with and without pain. J Pain Symptom Manage. 2014;48(5):852–62.
10. Hidding JT, Beurskens CH, van der Wees PJ, van Laarhoven HW, Nijhuis-van der Sand MW. Treatment related impairments in arm and shoulder in patients with breast cancer: a systematic review. PloS One. 2014;9(5):e96748.
11. Langer I, Guller U, Berclaz G, Koechli OR, Schaer G, Fehr MK, et al. Morbidity of sentinel lymph node biopsy (SLN) alone versus SLN and completion axillary lymph node dissection after breast cancer surgery: a prospective Swiss multicenter study on 659 patients. Ann Surg. 2007;245(3):452–61.
12. Osmani K, Vignes S, Aissi M, Wade F, Milani P, Levy BI, Kubis N. Taxane-indiced peripheral neuropathy has good long-term prognosis: a 1 – to 13-years evaluation. J Neurol. 2012;259:1936–43.
13. Helsedirektoratet. Norsk Bryst Cancer Gruppe (NBCG) Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølgning av pasienter med brystkreft [internett]. Oslo; Helsedirektoratet; 2018 [lesedato; 27.09.18]. Tilgjengelig fra: http://www.helsebiblioteket.no/retningslinjer/brystkreft/adjuvant-systemisk-behandling/adjuvant-hormonbehandling
14. Sestak I, Cuzick J, Sapunar F, Eastell R, Forbes JF, Bianco AR, Buzdar AU; ATAC Trialists Group. Risk factors for joint symptoms in patients enrolled in the ATAC trial: a retrospective, exploratory analysis. Lancet Oncol. 2008;9(9):866–72.
15. Treede RD, Jensen TS, Cambell JN, Cruccu G, Dostrovsky JO, Griffin JW, et al. Neuropathic pain: redefinition and a grading system for clinical and research purposes. Neurology. 2008;78(18):1630–5.
16. Jung BF, Ahrendt GM, Oaklander AL, Dworkin RH. Neuropathic pain following breast cancer surgery: proposed classification and research update. Pain. 2003;104(1–2):1–13.
17. Sheridan D, O’Shea H, Williams L, Colvin L. Long-term follow-up of pain and emotional characteristics of women after surgery for breast cancer. J Pain Symptom Manage. 2012; 44(4):608–14.
18. Johansen A, Romundstad L, Nielsen CS, Schirmer H, Stubhaug A. Persistent postsurgical pain in a general population: prevalence and predictors in the Tromsø study. Pain. 2012; 153:1390–96.
19. Kehlet H, Jensen TS, Woolf C. Persistent postsurgical pain: risk factors and prevention. Lancet. 2006;367(13):1618–25.
20. Nielsen PR, Ridin Å, Werner MU. Prediction of postoperative pain. Curr Anaesth Crit Care. 2007;18:157–65.
21. Wiech K, Tracey I. The influence of negative emotions on pain: behavioral effects and neural mechanisms. Neurolmage 2009;47:987–94.
22. Langford DJ, Paul SM, Cooper B, Kober KM, Mastick J, Melisko M, et al. Comparison of subgroups of breast cancer patients on pain and co-occurring symptoms following chemotherapy. Support Care Cancer. 2016;24(2):605–14.
23. Doong SH, Dhruva A, Dunn LB, West C, Paul SM, Cooper BA, et al. Associations between cytokine genes and a symptom cluster of pain, fatigue, sleep disturbance, and depression in patients prior to breast cancer surgery. Biol Res Nurs. 2014.
24. Kreftregistret. Nasjonalt kvalitetsregister for brystkreft. Oslo: Kreftregistret; 2018. Tilgjengelig fra: https://www.kreftregisteret.no/Registrene/Kvalitetsregistrene/Brystkreftregisteret/ (nedlastet 02.10.2018).
25. Stubhaug A, Breivik H. Can acute pain relief prevent chronic persistent postoperative neuropathic pain? I: Breivik H, Shipley M, red. Aspects of pain from best practice and research in anaesthesiology and rheumatology. London: Elsevier; 2006.
26. Landmark T, Romindstad P, Borchgrevink PC, Kaasa S, Dale O. Associations between recreational exercise and chronic pain in the generel population: evidence from the HUNT 3 study. Pain 2011;152(10):2241–71.
27. Helsedirektoratet. Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølgning av pasienter med brystkreft. Oslo: Helsedirektoratet; 2018. Tilgjengelig fra: https://helsedirektoratet.no/retningslinjer/nasjonalt-handlingsprogram-med-retningslinjer-for-diagnostikk-behandling-og-oppfolging-av-pasienter-med-brystkreft











































0 Kommentarer