Fanger opp forverring tidligere

Dårlige pasienter som ligger på sykehuset, kan observeres mer systematisk med verktøyet MEWS.
Systematiske observasjoner ved bruk av Modified Early Warning Score (MEWS) øker antall målinger av vitale parametere hos pasienter inneliggende i sykehus. Dette øker muligheten til å tidligere identifisere en forverring i pasientens kliniske tilstand.
Antall sengeplasser i norske sykehus har blitt redusert de siste
tiårene. Samtidig øker behovet for behandling i intensivavdelinger.
Det økte presset på intensivplasser kan føre til at pasientenes
kliniske tilstand er mer ustabil enn tidligere når de overflyttes
til sengeposter fra akuttmottak og intensivavdelinger. Dette bidrar
til økt kompetansekrav til helsepersonellet som jobber på
sengeposter (1,2,3).
Forverring i pasientens kliniske tilstand oppstår ofte gradvis
(4). Det er avgjørende å kunne identifisere tegn til endringer på
et tidlig tidspunkt, slik at utvikling av akutt kritisk sykdom kan
forebygges eller begrenses. Forskning viser at inneliggende
pasienter med forverret klinisk tilstand risikerer utilstrekkelig
og forsinket behandling (5,6,7,8,9).
Det er mange grunner til at alvorlig kritisk sykdom hos
pasienter inneliggende i sengepost i sykehus ikke blir identifisert
og forebygget. Dette kan skyldes utilstrekkelig måling av vitale
parametere, feilaktig tolkning av parameterne og forsinket reaksjon
på funnene (10). Flere studier beskriver tverrfaglig kommunikasjon
mellom sykepleiere og lege som problematisk. Sykepleiere lykkes
heller ikke alltid i å formidle hvor alvorlig pasientens situasjon
er til legen (9,11). Dermed kan identifisering og igangsetting av
tiltak ved alvorlig kritisk sykdom bli forsinket. Konsekvensene for
pasienten kan bli alvorlige: behov for behandling i
intensivavdeling eller i verste fall økt risiko for død (12).
Verktøy for å måle og dokumentere
Ulike hjelpemidler for systematisk observasjon av pasienters
vitale parametere er de senere år utviklet til bruk for
helsepersonell. Hensikten er å identifisere forverring i pasienters
kliniske tilstand på et tidlig tidspunkt (8,10,12). Modified Early
Warning Score (MEWS) er ett av mange forskjellige systematiske
scoringsverktøy som i dag brukes til måling og dokumentasjon av
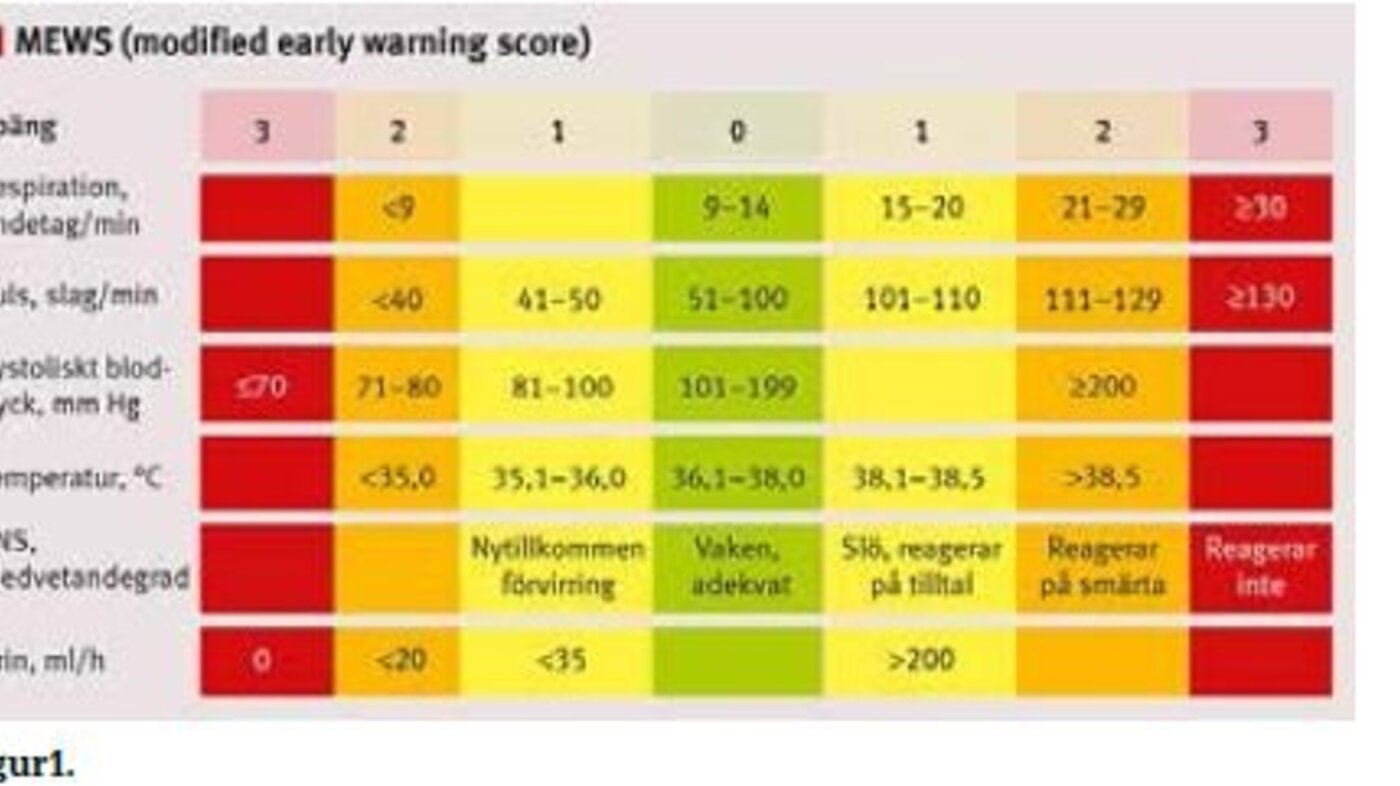
seks vitale parametere: respirasjonsfrekvens, puls, blodtrykk,
temperatur, bevissthetsnivå og urinproduksjon (figur 1) (8).
Avvikende målinger av normalverdiene på vitale parametere
genererer poeng. Hvis skåren øker, skal frekvensen på observasjoner
trappes opp. Ved en sammenlagt skår på tre eller mer skal personell
med høyere kompetansenivå tilkalles for å vurdere pasienten (12).
På sykehus i Sverige og Danmark har de brukt MEWS rutinemessig i mange år, men verktøyet er lite brukt i Norge. Moss var et av de første sykehusene her i landet som implementerte MEWS gjennom et pasientsikkerhetsprosjekt som ble avsluttet i 2010. I tillegg har Rikshospitalet i Oslo brukt verktøyet på noen sengeposter (10,13,14,15). På sykehus i Norge er det økende interesse for bruk av ulike hjelpemidler til systematisk å observere pasienters vitale parametere.
Metode
I dette litteraturstudiet har vi gjennomgått relevant litteratur fra 2004–2014. Litteratursøket er avgrenset til å gjelde voksne pasienter inneliggende på sengeposter. Strukturerte søk er gjort i databasene Medline, Chinal og SveMed+. Søkeord som er brukt er følgende: MEWS, deterioration, prevent, suboptimal care og nurse.
Ga økt antall målinger
Bruk av MEWS fører til økt antall målinger av vitale parametere
hos pasienter inneliggende i sengeposter. Systematiske
observasjoner bidrar til å tydeliggjøre endringer i pasientens
kliniske tilstand og kan forenkle og kvalitetssikre kommunikasjonen
mellom sykepleier og lege.
Flere faktorer må være til stede for å kunne ha nytte av MEWS.
Det er vesentlig at målingene av vitale parametere er
forskriftsmessig og korrekt utført (4). For at pasienter skal
observeres på en tilfredsstillende måte ved bruk av systematiske
hjelpemidler, må vitale parametere måles og dokumenteres minst to
ganger daglig (5).
Flere studier viser en økning i antall målinger av vitale
parametere etter implementering av MEWS. Blodtrykk og puls måles
oftest (5,6,13,15,16). De Meester et al. (16) fant en signifikant
økning i målinger av bevissthet og respirasjonsfrekvens etter at
sykepleierne hadde tatt i bruk MEWS. Likevel er det
respirasjonsfrekvensen som måles og dokumenteres sjeldnest av
sykepleiere (17). Ludikhuize et al. (7) beskriver
respirasjonsfrekvensen som «den glemte vitale parameteren» fordi
respirasjonsfrekvens bare var dokumentert i 23 prosent av
tilfellene. Antall målinger av vitale parametere økte etter
implementering av MEWS, men selv da var respirasjonsfrekvensen
sjelden dokumentert.
Reduserte dødelighet
I 2013 gjorde De Meester et al. (16) en studie som inkluderte
fire kirurgiske avdelinger før og etter at MEWS var implementert.
39 296 målinger av vitale parametere ble undersøkt. Etter
implementeringen av MEWS, var målingene mer nøyaktige og antall
observasjoner steg. Det ble i tillegg funnet en signifikant
reduksjon i dødelighet de første seks dagene postoperativt samt
nedgang i antall reoperasjoner (16).
En studie fra et dansk universitetssykehus innhentet data fra
pasientobservasjoner før implementering og ett og to år etter
implementering av MEWS og mobile intensivteam. Også her var det
flere observasjoner av vitale parametere etter implementering og
færre uventede dødsfall hos inneliggende pasienter.
Implementeringen førte ikke til flere innleggelser i
intensivavdelingen. Funnene kan tyde på bedre oppfølging og
tidligere igangsetting av nødvendige tiltak hos pasientene på
sengepostene (13).
Dokumentasjon viktig
Det er viktig med en nøyaktig dokumentasjon av MEWS for å regne
ut en skår som kan føre til videre tiltak (6). Studien til Hammon
et al. (6) viser at 25 prosent av MEWS-skårene ikke var fullstendig
dokumentert. Også De Meester et al. (5) fant at nesten halvparten
av observasjonene ble ekskludert på grunn av ufullstendig MEWS-skår
der én eller flere vitale målinger manglet.
En retrospektiv studie fra Nederland undersøkte hvilke målinger
som hadde blitt gjort i forkant hos akutt kritisk syke pasienter.
Pasientene hadde klare tegn til forverring med en kalkulert
MEWS-skår på tre eller mer allerede 25 timer før hendelsen. Studien
konkluderer med at dokumentasjon av vitale parametere tydelig
manglet i timene før en alvorlig klinisk forverring oppsto.
Ludikhuize et al. hevder at hvis MEWS hadde vært brukt, kunne disse
pasientene blitt identifisert på et tidligere tidspunkt (7).
Melder for sent om forverringer
Brukeren må også ha tilstrekkelig kunnskap om fysiologi og
patofysiologi (4). De Meester et al. (5) hevder at selv når vitale
parametere blir målt og dokumentert etter fastlagt prosedyre,
forstås ofte ikke risikoen ved endringer. En forverring i
pasientens kliniske tilstand blir kanskje ikke fanget opp tidlig
nok og fører dermed til forsinket behandling. I henhold til
Ludikhuize et al. (18) avventer mange sykepleiere ofte til
legevisitt med å orientere om tegn til klinisk forverring. Kyriacos
et al. (12) sammenfatter at 11,3 prosent av pasientene fikk
forsinket behandling med mer enn én time, og 8,9 prosent av dem
måtte vente i over tre timer på grunn av dette.
I en norsk studie utført av Melby (15) mener flere av
respondentene at bruk av MEWS bidrar til en standardisering av
observasjonene og en systematisk måte å kommunisere på. Denne
bruken kan bidra til trygghet i sykepleieres vurdering og
rapportering av pasientens kliniske tilstand.
Sykepleiere er flinke til å føle og oppleve hvordan pasienten
har det (14), men formidler ikke fysiologiske avvik på en konkret
måte (19). Tydelig kommunikasjon og godt samarbeid mellom
sykepleier og lege er essensielt i behandling av pasienter, men
denne kommunikasjonen beskrives som det svakeste leddet i
forebygging av akutt kritisk sykdom (9). Forskjeller i utdanningen
bidrar til ulikt kommunikasjonsmønster mellom sykepleiere og leger
(20).
Diskusjon 1
Vil bruk av MEWS føre til hyppigere måling av vitale parametere?
Systematiske observasjoner med bruk av MEWS gjør det lettere
å følge utviklingen i pasientens kliniske tilstand over tid (16).
Målingene må være fullstendige og dokumentasjonen god. Ifølge
Ludikhuize et al. (7) kan en kombinasjon av vitale parametere i
større grad identifisere forverring i pasientens kliniske
tilstand framfor å måle enkeltparametere. Hvis noen av parameterne
blir utelatt, kan man risikere å overse endringer hos pasienten
(12). Måling to ganger daglig kan være vanskelig å følge opp i en
travel sykehushverdag. Mange sykepleiere kan synes det er
meningsløst å gjennomføre MEWS etter prosedyre på pasienter som er
oppegående og tilsynelatende i god form. Dette kan være en årsak
til at noen parametere ikke blir målt slik som retningslinjene
sier. Det er svært betenkelig at respirasjonsfrekvensen, som er den
vitale parameteren som mest presis kan forutse alvorlig forverring
innen de neste 24 timer, blir målt minst (7,17,21).
MEWS er altså avhengig av nøyaktig dokumentasjon for å regne ut
en skår som kan føre til videre tiltak. Likevel mener Ludikhuize
et al. (7) at flere pasienter med forverring i klinisk tilstand kan
bli identifisert ved bruk av MEWS enn ved usystematiske målinger av
enkeltparametere.
Diskusjon 2
Vil bruk av MEWS bidra til identifisering og forebygging av
akutt kritisk sykdom?
I sykehus er det primært sykepleierens oppgave å observere
pasienter. Den første som oppdager endringer i pasientens vitale
parametere og avvik fra det forventede sykdomsforløpet, er som
regel en sykepleier. Sykepleieren har ikke myndighet til å
iverksette behandling eller rekvirere diagnostiske undersøkelser og
er dermed avhengig av å formidle pasientens situasjon til legen på
en forståelig måte. Subbe og Welch (9) identifiserer rapportering
om fysiologiske avvik som det svakeste leddet i kjeden for
forebygging av akutt kritisk sykdom. Dette støttes av Smith (4),
som framhever viktigheten av en entydig og godt kjent prosedyre for
hvordan man tilkaller hjelp til å vurdere pasienten.
Sykepleiere bygger ofte sine observasjoner på magefølelse og
klinisk blikk (14). Den tverrfaglige kommunikasjonen kan bli
problematisk hvis sykepleiere ikke er presise nok når de skal
forklare pasientens tilstand. Grunnen til dette kan være manglende
fysiologisk kunnskap eller manglende evne til å uttrykke teoretisk
kunnskap (19). Hierarkisk tenkning og engstelse for å få kritikk er
andre faktorer som bidrar til kommunikasjonsvansker (20).
Behandlingen kan bli alvorlig forsinket hvis sykepleiere venter til
legevisitten med å orientere om tegn til forverring i pasientens
kliniske tilstand (18). Vi gjenkjenner slike
kommunikasjonsutfordringer i egen klinisk praksis. Kommunikasjon om
pasientene må ofte skje på telefon da legene ikke oppholder seg i
avdelingene. Denne kommunikasjonsformen avhenger av at beskjeder
er korte, presise og oppfattes korrekt av mottaker.
Systematiske observasjoner med bruk av MEWS bidrar til en
objektiv og naturvitenskapelig tilnærming til pasientens kliniske
tilstand, noe som kan supplere sykepleierens totale
observasjonskompetanse (15). Når sykepleierne skal rapportere om
pasientens tilstand, ser det ut til at bruk av målbare bevis er
mest effektivt fordi de da raskt kan igangsette nødvendige tiltak
(4). Spesielt nyutdannete sykepleiere kan få hjelp til å utvikle
sitt kliniske blikk og kommunikasjonskompetanse ved å bruke MEWS
(15).
Kritikk til bruk av MEWS
Bruk av systematiske hjelpemidler som MEWS får kritikk siden det
bare er målbare parametere som blir skåret i skjema. Andre
symptomer og tegn, som for eksempel hudfarge, klamhet, smerte,
kvalme og diurese, kan også være svært viktige for å identifisere
en forverring i pasientens kliniske tilstand (12). Noen
MEWS-skjemaer har et underpunkt for generell bekymring for
pasienten og oppfordrer å kontakte lege på grunnlag av dette.
Uansett skal en poengskår ikke være det eneste kriteriet for å få
hjelp med å vurdere pasienten, men må inngå i en totalvurdering
(10).
Det er også usikkert om bruk av slike systematiske hjelpemidler
er i stand til å fange opp de individuelle forskjellene hos
pasientene. Vitale parametere som er normale for én pasient, kan
innebære risiko for en annen (9). I klinisk praksis oppleves man
at pasienter kan stå i fare for å få en forverret klinisk tilstand
til tross for normale vitale parametere, blant annet på grunn av
fysiologiske kompensasjonsmekanismer. Det er derfor viktig å ha
kunnskaper om pasientens normaltilstand samt kroppens ulike
kompensatoriske endringer for å vurdere og individualisere
observasjoner og tiltak (9).
Kritikere hevder også at denne standardiseringen av
observasjoner kan gjøre at sykepleiere mister evnen til å se hver
enkelt pasient ved å bruke klinisk blikk og faglig skjønn i
observasjon og pleie (10). Bruk av MEWS kan derimot være en fordel
fordi det fører til mindre synsing blant helsepersonell, noe som
kan bidra til å redusere innvirkningen av menneskelig svikt (15).
Uansett er det viktig å ta i betraktning at MEWS er et
hjelpemiddel og ikke en erstatning for sykepleierens faglige
vurderinger. Ved å bruke MEWS etter retningslinjene kan
sykepleierne få en indikasjon på hvilke pasienter som bør
observeres nøyere, og hvor ofte de bør observeres, samt når lege
skal kontaktes. Dette kan bidra til økt refleksjon over både
pasientens kliniske tilstand og de ulike tiltakene som iverksettes
(15).
Konklusjon
Det er ikke entydig hvorvidt systematisk observasjon ved bruk av
MEWS vil føre til tidlig identifisering og forebygging av en
forverring av pasientens kliniske tilstand. Når personellet bruker
MEWS på sengeposter, fører det til økt frekvens på målinger av
vitale parametere. For å få nytte av MEWS er man avhengig av god
dokumentasjon, men skjemaet føres ofte ufullstendig, der både én
eller flere målinger av vitale parametere manglet. Likevel
beskriver flere studier at bruk av MEWS gjør det enklere å
gjenkjenne unormale vitale parametere. Dermed øker mulighetene til
å kunne identifisere en forverring i pasientens kliniske tilstand
på et tidlig stadium. Bruk av MEWS bidrar også til å bedre og
tydeliggjøre kommunikasjonen mellom sykepleier og lege om
pasientens tilstand.
MEWS skal være et hjelpemiddel og ikke en erstatning for
faglige vurderinger. Korrekt bruk sammen med tydelig tverrfaglig
kommunikasjon kan gjøre det lettere å identifisere en forverring i
pasientens kliniske tilstand på et tidlig tidspunkt.
Helsepersonellet kan da sette i gang nødvendig behandling av
pasienten raskest mulig og kanskje begrense utviklingen av akutt
kritisk sykdom.
Kirurgisk klinikk ved St. Olavs Hospital i Trondheim startet
våren 2015 et prosjekt med innføring av observasjonsskjema for
tidlig identifisering av klinisk forverring. Det ble besluttet å
bruke National Early Warning Score (NEWS). NEWS er en nyere og
bedre validert versjon av Modified Early Warning Score (MEWS). NEWS
er nå i bruk ved alle sengepostene på Kirurgisk klinikk og det
planlegges implementering på flere klinikker ved St. Olavs
Hospital i løpet av 2016.
Referanser:
1. Aase K. Pasientsikkerhet – teori og
praksis. Oslo: Abstrakt forlag, 2010.
2. Laake JH, Dybvik K, Flaaten HK, Fonneland
IL, Kvåle R, Strand K. Impact of the post-World War 2 generation on
intensive care needs in Norway. Acta Anesthesiol
Scand 2009;11:1-6.
3. Ræder J. Er eldrebølgen på vei inn i
sykehusene? Tidsskr nor legeforen 2012;132:2582.
4. Smith GB. In-hospital cardiac arrest: is
it time for an in-hospital “chain of prevention”?
Resuscitation 2010;81:1209–11.
5. De Meester K, Das T, Hellemans K,
Verbrugghe W, Jorens P, Verpooten G, Van Bogaert P. Impact of a
standardized nurse observation protocol including MEWS after
Intensive Care Unit discharge. Resuscitation 2013a;84:184–8.
6. Hammond NE, Spooner A, J, Barnett A G,
Corley A, Brown P, Fraser J F. The effect of implementing a
modified early warning scoring (MEWS) system on the adequacy of
vital sign documentation. Australian Critical Care
Nursing 2013;26:18–22.
7. Ludikhuize J, Smorenburg SM, De Rooij SE,
De Jonge E. Identification of deteriorating patients on general
wards; measurement of vital parameters and potential effectiveness
of the Modified Early Warning Score. Journal of Critical
Care 2012;27(4): 424.e7–13.
8. Stenhouse C, Coates S, Tivey M, Allsop P,
Parker T. Prospective evaluation of a modified Early Warning Score
to aid earlier detection of patients developing critical illness on
a general surgical ward. British Journal of
Anaesthesia 2000;84:663.
9. Subbe CP, Welch JR. Failure to rescue:
using rapid response systems to improve care of the deteriorating
patient in hospital. Clinical Risk 2013;19:6–11.
10. Fridén T, Andrén-Sandberg Å. Kritisk sjuk
inneliggande patient måste få hjälp i tid.
Läkartidningen 2013;110:29–31.
11. Donohue L A, Endacott R. Track, trigger
and teamwork: Communication of deterioration in acute medical and
surgical wards. Intensive and Critical Care
Nursing 2010;26:10–17.
12. Kyriacos U, Jelsma J, Jordan S.
Monitoring vital signs using early warning scoring systems: a
review of the literature. Journal of nursing
management 2011;19:311–30.
13. Bunkenborg G, Samuelson K, Poulsen I,
Ladelund S, Åkeson J. Lower incidence of unexpected in-hospital
death after interprofessional implementation of a bedside
track-and-trigger system. Resuscitation 2014;85:424–30.
14. Dietrichson S. «Mewsing» gir sikrere
pasientvurdering. Sykepleien forskning 2012;1:86–7.
15. Melby AKI. Bruk av kliniske observasjoner
(MEWS) til å styrke pasientsikkerheten i somatiske sengeposter.
Halden: Høgskolen i Østfold, 2012.
16. De Meester K, Haegdorens F, Monsieurs KG,
Verpooten GA, Holvoet A, Van Bogaert P. Six-day postoperative
impact of a standardized nurse observation and escalation protocol:
A preintervention and postintervention study. Journal of critical
care 2013b;28:1068–74.
17. Cretikos MA, Bellomo R, Hillman K, Chen
J, Finfer S, Flabouris A. Respiratory rate: the neglected vital
sign. Medical Journal of Australia 2008;188:657.
18. Ludikhuize J, De Jonge E, Goossens A.
Measuring adherence among nurses one year after training in
applying the Modified Early Warning Score and
Situation-Background-Assessment-Recommendation instruments.
Resuscitation 2011;82:1428–33.
19. Massey D, Aitken LM, Chaboyer W. What
factors influence suboptimal ward care in the acutely ill ward
patient? Intensive & Critical Care Nursing 2009;25:169–80.
20. Wallin CJ, Thor J. SBAR – modell för
bättre kommunikation mellan vårdpersonal.
Läkartidningen 2008;105:1922–5.
21. Mcgain F, Cretikos MA, Jones D, Van Dyk
S, Buist MD, Opdam H, Pellegrino V, Robertson MS, Bellomo R.
Documentation of clinical review and vital signs after major
surgery. Medical Journal of Australia 2008;189:380–3.






















0 Kommentarer