Forekomst av depressive symptomer og assosierte faktorer hos personer som lever med hiv i Norge. En tverrsnittsstudie
Sammendrag
Bakgrunn: Desom lever med hiv i Norge, har en lovfestet rett til gratis psykisk helsehjelp. Internasjonale og norske faglige retningslinjer for oppfølging og behandling av hiv understreker at det er viktig med søkelys på psykisk helse i hivomsorgen. Det finnes ikke nasjonale data om psykisk helse hos personer med hiv. Vi ønsket derfor å kartlegge hvor ofte depressive symptomer forekommer hos dem med hiv, i hvilken grad de mottok psykisk helsehjelp, og hvilke risikofaktorer for depressive symptomer som finnes i Norges største hivkohort.
Metode: I løpet av ett år gjennomførte vi en tverrsnittsstudie av dem over 18 år som møtte til kontroll for sin hivinfeksjon ved Infeksjonsmedisinsk poliklinikk på Oslo universitetssykehus, Ullevål. Data ble innhentet gjennom strukturert intervju, fra et lokalt hivkvalitetsregister (Medinsight.no) og fra journaler. Alle som deltok, fylte ut Beck Depression Inventory, versjon II (BDI-II). BDI-II > 14 indikerer symptomer på moderat til alvorlig depresjon.
Resultat: Av 486 mulige ble 397 (82 prosent) inkludert. BDI-II > 14 ble funnet hos 76 (19 prosent). Av disse mottok 46 (61 prosent) ingen psykisk helsehjelp. Å bo i kommunal bolig (odds ratio [OR] 4,0, 95 % konfidensintervall [KI] 1,6–10,3), være smittet før introduksjon av proteasehemmere (OR 3,2, 95 % KI 1,1–7,9), opprinnelse fra Asia eller Sør- og Mellom-Amerika (OR 2,9, 95 % KI 1,4–6,0) og rus (OR 2,3, 95 % KI 1,2–4,3) var risikofaktorer for depressive symptomer. Det var redusert risiko for depressive symptomer hos dem med antiretroviral behandling (antiretroviral therapy, ART) basert på ikke-nukleosid revers transkriptasehemmere sammenliknet med dem som brukte integrasehemmere (OR 0,5, 95 % KI 0,2–0,9).
Konklusjon: En av fem hadde depressive symptomer, og andelen uten adekvat psykisk helsehjelp var betydelig. Dette peker på et behov for bedre ivaretakelse av psykisk helse hos dem med hiv. Vi foreslår at de med en eller flere risikofaktorer for depressive symptomer blir kartlagt ved å bruke BDI-II. Enklere screeningspørsmål for å avdekke depressive symptomer og i hvilken grad ART-regimet påvirker depressive symptomer, bør utforskes videre.
Referer til artikkelen
Sørsvang L, Bergersen B, Jenum S. Forekomst av depressive symptomer og assosierte faktorer hos personer som lever med hiv i Norge. En tverrsnittsstudie. Sykepleien Forskning. 2022;17(90566):e-90566. DOI: 10.4220/Sykepleienf.2022.90566
Introduksjon
I Norge lever cirka 6500 personer med hiv, noe som utgjør en prevalens på omtrent 0,12 prosent (1). Med moderne antiretroviral behandling (antiretroviral therapy, ART) er forventet levealder for personer som lever med hiv, tilnærmet lik normalbefolkningen (2, 3).
Fullt virussupprimerte personer som lever med hiv, er ikke lenger ansett som smitteførende (4), og kvinner kan fullføre svangerskap med minimal risiko for å overføre smitten til barnet (5). Hivinfeksjon krever livslang medikamentell behandling og må derfor betraktes som en kronisk sykdom, selv om en velbehandlet infeksjon i seg selv ikke gir symptomer.
Over tid vil både den kroniske infeksjonen og ART gi økt risiko for blant annet kardiovaskulær sykdom, nyresvikt og benskjørhet (6). European Aids Clinical Society (EACS) lister opp en rekke forhold som påvirker den mentale helsen til personer med hiv. Blant annet høy alder, rus og isolasjon på grunn av stigma knyttet til hiv og aids kan være en belastning for mange som lever med hiv. Disse faktorene kan bidra til at 20–40 prosent av dem som lever med hiv, har depresjon sammenliknet med 7 prosent av normalbefolkningen (7).
Økt forekomst av depresjon blant dem som lever med hiv, er også vist i Sverige (8). The Greater Stockholm Hiv Cohort Study hadde til hensikt å se på sammenhengen mellom hiv og blant annet depresjon. I Sverige har man et nasjonalt register hvor alle diagnosekodene på en person blir samlet i ett register (9–11).
Årsaksforholdet mellom hivinfeksjon og depresjon er komplekst, da begge kan påvirke hverandre. Depresjon kan øke risikoen for hivsmitte og ha negativ effekt på etterlevelse av hivbehandling, som i sin tur kan bidra til dårligere behandlingsresultater og økt sykelighet. På den annen side kan depresjon være en konsekvens av hiv, både gjennom biologiske mekanismer og knyttet til praktiske og psykososiale konsekvenser av diagnosen (9–11).
Velbehandlet depresjon er vist å bedre etterlevelsen av ART, hvilket understreker viktigheten av å identifisere og behandle depresjon hos personer med hiv (9, 12). På bakgrunn av dette understreker EACS viktigheten av å fokusere på psykisk helse i sine retningslinjer for oppfølging og behandling av personer som lever med hiv (7). Det samme poengteres i norske retningslinjer (13).
Personer med hiv har lovfestet rett til gratis psykisk helsehjelp i Norge (14). Det er derfor problematisk at det ikke finnes nasjonale data på forekomsten av psykiske helseplager i denne pasientgruppen. Vi mener det er viktig med nasjonale data, da internasjonale data ikke nødvendigvis kan overføres til norske forhold.
Vi ble inspirert av studier om depresjon og depressive symptomer som var gjennomført i danske hivkohorter (15–17). Hensikten med denne studien var derfor å kartlegge 1) forekomsten av depressive symptomer blant personer som lever med hiv, 2) andelen med etablert psykisk helsehjelp, og 3) risikofaktorer assosiert med depressive symptomer for å få et datagrunnlag for kvalitetsutvikling av omsorgen til personer med hiv.
Metode
Studiedesign
Studien er en tverrsnittsstudie av dem med hiv som kom til rutinekontroll ved Infeksjonsmedisinsk poliklinikk på Oslo universitetssykehus (OUS) på Ullevål i perioden 1. februar 2017 til 31. januar 2018. Ved rutinekontroll innkalles de normalt hver sjette måned, vekselvis til lege og sykepleier. De som var ≥ 18 år med forståelse for skriftlig norsk eller engelsk, var inkluderbare, forutsatt at de hadde gitt skriftlig informert samtykke.
Utvalg og rekruttering
Infeksjonsmedisinsk poliklinikk, OUS Ullevål, hadde per 31. desember 2018 en hivkohort som utgjorde 1739 personer. Av disse gikk noen til legekontroll kun hver sjette måned, mens noen gikk vekselvis til lege og sykepleier. Det var pasientansvarlig lege som gjorde denne vurderingen.
De som også gikk til en sykepleier, var fortrinnsvis de med en ukomplisert hivinfeksjon, men også de som hadde behov for hyppig oppfølging. De som ble innkalt til en sykepleier, ble gjort oppmerksom på i innkallingsbrevet at psykisk helse ville være prioritert. Studien ble gjennomført innenfor rammene av ordinær klinisk drift, som begrenset rekrutteringsutvalget.
Datasamling
Etter skriftlig informert samtykke ble informantene intervjuet om opprinnelsesland, sivil status, økonomisk situasjon, boligsituasjon, bruk av andre rusmidler enn alkohol samt oppfølging av psykisk helse. Fra 2016 ble disse variablene registrert i det lokale hivkvalitetsregistret Medinsight.no.
Kjønn, alder, diagnosetidspunkt, smittemåte, ART-regime, grad av immunsuppresjon (CD4-tall) og virusmengde per milliliter blod ble hentet fra det lokale hivkvalitetsregistret og den medisinske journalen.
Kartlegging av depressive symptomer
For å kartlegge symptomer på depresjon valgte vi The Beck Depression Inventory, versjon II (BDI-II) (18). Denne er et lett tilgjengelig skåringsverktøy for helsepersonell gjennom depresjonstesten til Global University (19).
Verktøyet krever ikke omfattende opplæring før bruk (18), har høy validitet og pålitelighet for depressive symptomer (18), er validert i en norsk populasjon (20) og er benyttet i tilsvarende studier i danske hivpopulasjoner (14–16).
Det er et kartleggingsskjema med 21 temaer for å måle forekomsten og dybden av depressive symptomer. Skjemaet inneholder både psykiske dimensjoner, for eksempel tristhet, og fysiske dimensjoner, for eksempel smerte. Hvert tema i BDI-II har en gradert beskrivelse med en skår fra 0–3 poeng, der 0 = «jeg føler meg ikke trist» og 3 = «jeg er så trist eller ulykkelig at jeg ikke holder det ut». Personen velger den uttalelsen som best beskriver tilstanden de to siste ukene. Desto høyere poeng, der 63 er maksimum, desto sterkere er indikasjonen på depressive symptomer.
BDI-II > 14 indikerer moderate til alvorlige depressive symptomer og illustrerer behov for ytterligere utredning. Fordi depressive symptomer opptrer som en del av det kliniske bildet ved flere psykiske lidelser, er det viktig å understreke at BDI-II kartlegger depressive symptomer med høy validitet, vel vitende om at det kreves psykiatrisk kompetanse og andre diagnoseverktøy for å stille en psykiatrisk diagnose.
Deltakerne ble informert om screeningresultatet. Ved BDI-II > 14 ble de tilbudt henvisning til fastlege for videre oppfølging og/eller henvising til en spesialist innen psykiatri.
Statistikk
Vi registrerte dataene i SPSS (IBM Statistics for Windows, versjon 25.0). De ble senere dobbeltsjekket av sykepleieren med hovedansvaret for studien.
BDI-II-skår ble delt i to kategorier rundt den validerte grenseverdien for moderate til alvorlige depressive symptomer, altså BDI-II > 14 eller BDI-II ≤ 14, som indikerer normalt stemningsleie til milde depressive symptomer.
For kategoriske variabler ble referanseverdi definert ut fra majoriteten i studiekohorten eller den vanligste eller mest etablerte statusen i det norske samfunnet. Variabelen tidspunkt for diagnose har vi delt i to etter følgende vurdering:
1) Variabelnavn: Hivdiagnose før proteasehemmere. Da proteasehemmere (PI, protease inhibitors) ble introdusert i 1995, endret det markant hivinfeksjonens betydning for helse og forventet levealder (21, 22).
2) Variabelnavn: Hivdiagnose innen siste året. Nylig hivdiagnose, innen det siste året før studieinklusjon, representerer en stor omveltning for den enkelte og dermed en mulig risikofaktor for depressive symptomer.
Deskriptive analyser ble utført stratifisert for BDI-II-kategori. Vi undersøkte risikofaktorer for BDI-II > 14 med univariat og deretter multivariat logistisk regresjonsanalyse. Følgende uavhengige variabler ble undersøkt: kjønn, alder, hivdiagnose før proteasehemmere, hivdiagnose innen siste året, smittemåte, opprinnelsesland, sivil status, økonomisk situasjon, boligsituasjon, ART, virusmengde (antallet viruskopier per milliliter blod), CD4-tall (mål for T-celle-immunforsvar) og bruk av rusmidler.
Alle uavhengige variabler ble analysert i en blokk, der vi ekskluderte variabler med høy multikolliniaritet (toleranseverdi ≤ 0,2). I den endelige justerte analysen inkluderte vi kjønn, hivdiagnose før proteasehemmere, hivdiagnose innen siste året, opprinnelsesland, sivil status, boligsituasjon, ART, antallet viruskopier og bruk av rusmidler. Resultatet er presentert som odds ratio (OR) med tilhørende 95 prosent konfidensintervall (KI) og tosidig p-verdi med statistisk signifikans definert som p < 0,05.
Etiske vurderinger
Studiens overordnede hensikt var å forbedre kvaliteten i hivomsorgen og var forankret hos ledelsen ved Infeksjonsmedisinsk avdeling på OUS, Ullevål. Avdelingen har et godt og etablert samarbeid med flere brukerorganisasjoner som HIV Norge og Aksept for å sikre en god ivaretakelse av en heterogen pasientgruppe med sårbare individer. Som en forberedelse til studien avholdt vi i desember 2016 et lokalt brukermøte der vi informerte brukere om studien, som ga sin tilslutning til studien.
Regional komité for medisinsk og helsefaglig forskningsetikk, Sør-Øst-Norge (referansenummer 2016/2210C) ga sin tilslutning, og personvernombudet ved OUS har godkjent at vi kan lagre data (referansenummer 2016/18515) og oppbevare de skriftlige informerte samtykkene fra deltakerne i et låsbart skap sammen med personenes studiespesifikke ID-kode.
Resultater
I inklusjonsperioden møtte 486 personer til rutinekontroll hos sykepleier, og 397 (82 prosent) tilfredsstilte inklusjonskriteriene. Årsaker til eksklusjon var språk (10 prosent), ikke ønske om å delta (7 prosent) og ikke-returnerte BDI-II-skjemaer innen inklusjonsperioden (1 prosent) (figur 1).
Deltakerkarakteristika
Av 397 personer var 80 prosent menn, 58 prosent var mellom 31 og 49 år, 68 prosent hadde opprinnelse fra vestlige land, 55 prosent var gift, samboende eller i et forhold, 63 prosent jobbet fulltid, og 60 prosent eide egen bolig. Så mange som 79 prosent rapporterte at de ikke hadde erfaring med rusmidler utover alkohol.
Vedrørende hivspesifikke faktorer fikk 6 prosent hivdiagnosen før introduksjonen av proteasehemmere, mens 6 prosent fikk hivdiagnosen innen det siste året. Majoriteten på 88 prosent fikk altså sin hivdiagnose etter 1995, men før 2016. Menn som har sex med menn (MSM) utgjorde den største gruppen av smittede med 67 prosent.
Med unntak av én person mottok alle 397 ART. Majoriteten av disse, 58 prosent, hadde et regime som inkluderte integrasehemmere. Hele 95 prosent hadde virussuppresjon (< 50 viruskopier per ml blod), og 73 prosent hadde CD4-tall ≥ 500 (tabell 1).
Forekomst av depressive symptomer og andel med psykisk helsehjelp
En BDI-II-skår > 14, som indikerer moderate til alvorlige depressive symptomer, ble observert hos 76 (19 prosent) av de inkluderte. Av disse var det 61 prosent som ikke mottok psykisk helsehjelp på inklusjonstidspunktet.
Selv blant de 30 med BDI-II-skår på 25–63, som indikerer alvorlige depressive symptomer, var andelen uten psykisk helsehjelp så høy som 47 prosent. Personer gruppert etter BDI-II-kategoriene og andelen personer uten psykisk helsehjelp innen disse kategoriene er vist i tabell 2.
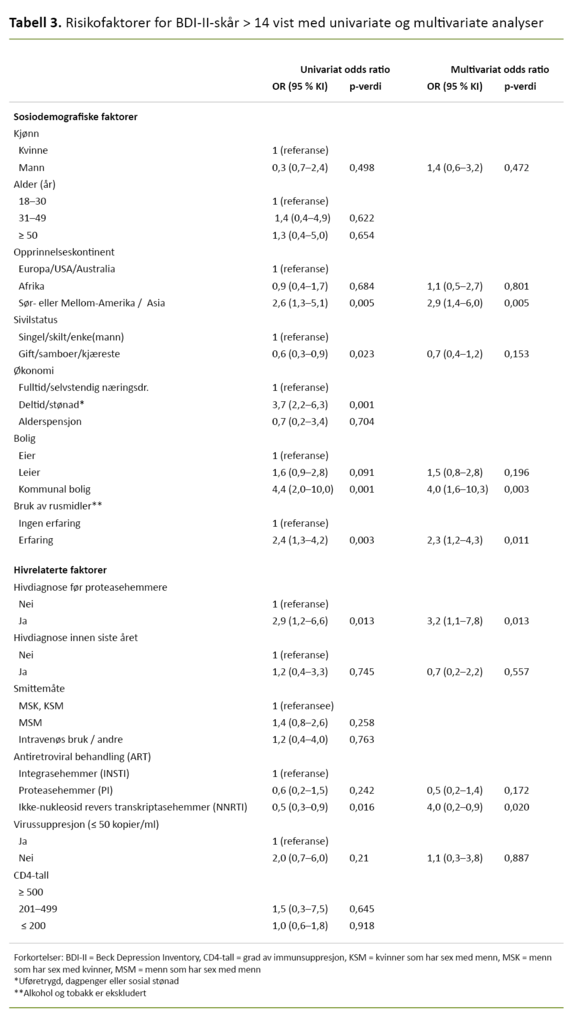
Risikofaktorer for BDI-II > 14 – moderate til alvorlige depressive symptomer
I den multivariate analysen var verken kjønn eller sivil status assosiert med BDI-II > 14. Risikoen for BDI-II > 14 var økt mer enn tre ganger ved hivdiagnose før introduksjon av proteasehemmere (OR 3,2, 95 % KI 1,1–7,9), mens hivdiagnose innen det siste året ikke var assosiert med BDI-II > 14.
Personer med opprinnelse fra Asia eller Sør- og Mellom-Amerika hadde omkring tre ganger høyere risiko for BDI-II > 14 (OR 2,9, 95 % KI 1,4–6,0) sammenliknet med personer fra Europa, USA og Australia. Personer med kommunal bolig hadde fire ganger høyere risiko for BDI-II > 14 (OR 4,0, 95 % KI 1,6–10,3) sammenliknet med personer som eide bolig. Erfaring med rusmidler – unntatt alkohol – ga også økt risiko for BDI-II > 14 (OR 2,3, 95 % KI 1,2–4,3).
Sammenliknet med integrasehemmerbasert ART var risikoen for BDI-II > 14 halvert hos personer med ikke-nukleosid revers transkriptasehemmerbasert ART (OR 0,5, 95 % KI 0,2–0,9). Virologisk svikt, altså > 50 viruskopier per milliliter blod, var ikke assosiert med BDI-II > 14 (tabell 3).
Diskusjon
Denne studien viste at forekomsten av moderate til alvorlige depressive symptomer hos dem med hiv var 19 prosent. En betydelig andel av disse, 61 prosent, hadde ikke etablert psykisk helsehjelp ved inklusjon. Av de 30 med alvorlige depressive symptomer var andelen uten etablert psykisk helsehjelp bekymringsfulle 47 prosent.
Hiv-diagnose før introduksjon av proteasehemmere, opprinnelse fra Asia eller Sør- og Mellom-Amerika og bruk av rusmidler utover alkohol økte risikoen for moderate til alvorlige depressive symptomer i justerte analyser. Det var overraskende at de med et ikke-nukleosid revers transkriptasehemmerbasert regime hadde redusert risiko for depressive symptomer sammenliknet med dem med et integrasehemmerbasert regime.
Forekomsten av depressive symptomer på 19 prosent i vårt materiale er lavere enn 33–38 prosent i danske hivkohorter ved bruk av samme skåringsverktøy (15–17). I disse studiene fikk deltakere med BDI-II > 20 per protokoll tilbud om konsultasjon med mål om å bekrefte eller avkrefte en psykiatrisk diagnose, hvilket kan representere en mulig skjevhet (bias) mot høyere BDI-II-skår.
Selv om hivpoliklinikker i Norge mangler psykiatrisk kompetanse, er vår erfaring at hivpasienter etablerer varige tillitsrelasjoner til sin faste lege og sykepleier, slik at hivpoliklinikkene representerer en trygg arena for samtaler og intervensjon for bedre fysisk og psykisk helse. Depressive symptomer som er identifisert med BDI-II, kan være tegn på depresjon, men også andre psykiske lidelser (16, 17). Vi oppmuntret derfor pasienter med BDI-II > 14 til å ta kontakt med fastlegen sin for videre henvisning, utredning og behandling.
Den bekymringsfullt høye andelen med depressive symptomer uten etablert psykisk helsehjelp understreker behovet for mer oppmerksomhet på psykisk helse for å bedre kvaliteten på hivomsorgen. Studien identifiserer risikofaktorer for skåren BDI-II > 14, som kan brukes til målrettet screening og preventive tiltak. I tråd med andre studier (9, 15–17) fant vi også at risikoen for depressive symptomer økte ved dårlig økonomi og usikre boligforhold.
Da vi sammenliknet med pasienter fra Europa, USA og Australia, så vi at risikoen for depressive symptomer hos dem fra kontinentene Asia, Sør- og Mellom-Amerika var høyere, men ikke hos dem fra det afrikanske kontinentet. I en metaanalyse av helse blant afrikanske immigranter fant man både høyere og lavere forekomst av psykisk sykdom sammenliknet med ikke-immigranter.
Afrikanske asylsøkere rapporterer entydig om høyere forekomst av psykisk lidelse, og flyktninger rapporterer om økt psykisk stress (23). I studien vår var 78 personer (20 prosent) fra det afrikanske kontinentet, men ingen av disse hadde flyktning- eller asylsøkerstatus. Dette funnet kan forklare den lave forekomsten av depressive symptomer.
Assosiasjonen mellom rus og depressive symptomer som er rapportert i andre skandinaviske (16, 17) og internasjonale hivpopulasjoner (9), ble også bekreftet i studien vår. Det er imidlertid verdt å merke seg at denne sammenhengen ikke er funnet i alle hivpopulasjonene. Det kan skyldes interaksjon mellom flere psykososiale faktorer (24).
Så vidt vi vet, er denne studien den første til å rapportere om økt risiko for depressive symptomer blant dem som fikk sin hivdiagnose før introduksjonen av proteasehemmere. Årsaken til det er sannsynligvis sammensatt og knyttet til daværende livsutsikter med hivinfeksjon, bivirkninger fra førstegenerasjons ART og/eller hivrelaterte komorbiditeter (25).
Noen hivmedisiner har negativ effekt på den psykiske helsen. Den ikke-nukleosid revers transkriptasehemmeren efavirenz er assosiert med høyere risiko for suicidale tanker (26) og er ikke anbefalt til personer med depresjonshistorikk (7).
Av 128 pasienter med ikke-nukleosid revers transkriptasehemmerbasert ART i denne studien brukte kun 14 prosent efavirenz, med like stor andel blant dem med BDI-II > 14: 2 av 16, 12,5 prosent, som dem med BDI-II ≤ 14: 16 av 112, 14,3 prosent.
I fem randomiserte, kontrollerte studier ble det ikke funnet forskjell i psykiske symptomer blant deltakere med integrasehemmerbasert ART (dolutegravir og raltegravir), efavirenz (ikke-nukleosid revers transkriptasehemmer) og proteasehemmerbasert ART (kun darunavir) (27).
Det er imidlertid viktig å utvise varsomhet i tolkningen av disse resultatene: Efavirenz ble mest sannsynlig ikke startet hos dem med en psykiatrisk historie i tråd med gjeldende retningslinjer (7, 13), og andre ikke-nukleosid revers transkriptasehemmere med mindre alvorlige psykiatriske bivirkninger er ikke inkludert i studien.
Kolakowska og medarbeidere har nylig oppsummert nevropsykiatriske bivirkninger ved integrasehemmere. Selv om standardisert registrering av nevropsykiatriske bivirkninger er utfordrende og studiene spriker, tyder dataene på at dolutegravir i større grad enn andre integrasehemmere bør brukes med forsiktighet hos pasienter med psykiske utfordringer inntil bedre data foreligger (28).
I motsetning til andre studier (9, 10) fant vi ingen assosiasjon mellom virologisk respons på behandling og depressive symptomer. Dette funnet kan mest sannsynlig forklares med den lave andelen på 16 personer med virologisk svikt (virusmengde > 50 kopier per milliliter blod) i studiepopulasjonen (tabell 1).
Studiens styrke var den høye deltakelsen: 82 prosent i denne studien sammenliknet med 60 prosent i de tidligere refererte danske studiene (15–17). Høy deltakelse kan ha vært fremmet av at BDI-II-skjemaene ble fylt ut i forbindelse med rutinekontrollen, slik at deltakerne kunne få bistand til utfyllingen hvis de ønsket det.
Et langvarig tillitsforhold til sykepleieren kan ha bidratt til høyere deltakelse, men også til en underrapportering av bruk av rusmidler: Enkelte tilkjennega en bekymring for at slike sensitive opplysninger skulle spres til instanser utenfor sykehuset.
BDI-II ble bare besvart én gang og gir dermed et øyeblikksbilde av depressive symptomer som typisk varierer over tid. Dette faktumet må man ta hensyn til i oppfølgingen av den enkelte, men det har mindre betydning for kartlegging av forekomst i en populasjon. Dessverre var ikke historikk over psykiske lidelser en del av kartleggingen. Det er en klar risikofaktor for depressive symptomer i de danske studiene (15–17).
Mangelen på historikk over psykiske lidelser i denne studien vanskeliggjør også tolkningen av den observerte assosiasjonen mellom BDI-II og ART-regime. Det er også en svakhet av vi ikke inkluderte de to screeningspørsmålene for depresjon, som er anbefalt brukt hvert år til hvert annet år i hivretningslinjene fra the European AIDS Clinical Society: «1. Have you often felt depressed, sad or without hope in the last few months?» og «2. Have you lost interest in activities that you usually enjoy?» (7).
Dersom funnene i studien vår skal ha relevans for fremtidige rutiner ved oppfølging og behandling av hiv, må vi sannsynliggjøre representativitet av studiekohorten på 397 pasienter sammenliknet med den totale hivkohorten, som per 31. desember 2018 inneholdt ytterligere 1342 pasienter. Basert på det lokale hivkvalitetsregistret, som inneholder prospektive sosiodemografiske, anamnestiske og kliniske data, kan vi beskrive hele hivkohorten uten å komme i konflikt med personvernregler.
Andelen menn i studiekohorten var høyere enn i hivkohorten: 80 prosent versus 73 prosent. Andelen personer ≤ 30 var den samme (5 prosent), mens gruppen 31–49 år var overrepresentert (58 prosent sammenliknet med 44 prosent), og gruppen ≥ 50 år var underrepresentert (37 prosent sammenliknet med 47 prosent).
Denne studien lyktes relativt bra med å inkludere personer med ikke-vestlig bakgrunn (32 prosent i studiekohorten versus 40 prosent i hivkohorten). Det gjelder også for personer med opprinnelse fra det afrikanske kontinentet (20 prosent versus 25 prosent). Andelen personer fra Asia eller Sør- og Mellom-Amerika var den samme (12 prosent i studiekohorten versus 13 prosent i den totale hivkohorten), noe som har betydning siden vi fant at opprinnelse fra Asia eller Sør- og Mellom-Amerika var en risikofaktor for BDI-II > 14.
Andelen med hivdiagnose før introduksjon av proteasehemmere var liten i begge kohortene, men underrepresentert i studiekohorten (7 prosent versus 12 prosent i hivkohorten). Det kan indikere en noe høyere forekomst av depressive symptomer i den totale hivkohorten.
Kvinner (20 prosent i studiekohorten versus 27 prosent i hivkohorten) og personer ≥ 50 år (37 prosent versus 47 prosent) var noe underrepresentert i studien, men det er usikkert hvor relevant dette funnet er, da vi ikke identifiserte kjønn eller alder som risikofaktor for BDI-II > 14 i studien vår.
Konklusjon
I denne studien forekom BDI-II skår > 14 hos 19 prosent av dem med hiv, som er indikativt for moderate til alvorlige depressive symptomer. Dette funnet understreker et behov for å inkludere vurdering av psykisk helse i en helhetlig hivomsorg. Det er oppsiktsvekkende at omkring 50 prosent av dem med alvorlige depressive symptomer ikke hadde adekvat psykisk helsehjelp.
Vi foreslår å kartlegge depressive symptomer med BDI-II hos personer med hiv på årskontrollen ved Infeksjonsmedisinsk poliklinikk. Ved ressursmangel kan det forsvares å begrense kartleggingen til pasienter med en eller flere risikofaktorer. Det er også behov for studier som evaluerer nytte og effekt ved å stille de to screeningspørsmålene for depresjon som anbefales av the European AIDS Clinical Society (7).
Det var overraskende at dem med ikke-nukleosid revers transkriptasehemmerbasert ART hadde redusert risiko for depressive symptomer sammenliknet med personer med integrasehemmerbasert ART. Dette funnet indikerer et behov for flere studier som utforsker sammenhengen mellom ulike ART-regimer og psykisk helse. I slike studier er det avgjørende å kartlegge tidligere psykiske helseplager, da de representerer en skjevhet (bias) ved valg av ART.
Forfatterne oppgir ingen interessekonflikter.

























0 Kommentarer