Smerteprosjektet COMFORTneo
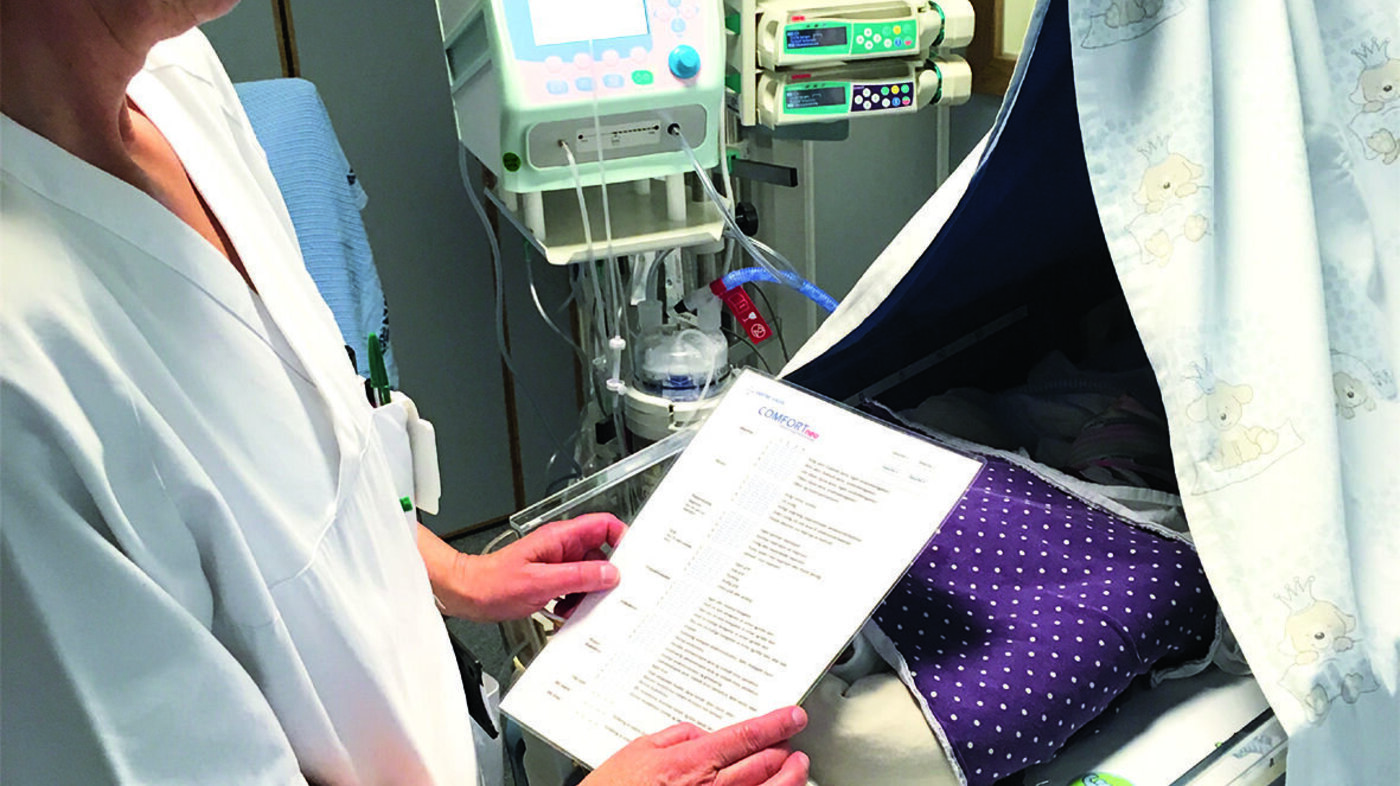
Smerte og stress hos premature og syke nyfødte kan avdekkes med COMFORTneo. Observasjonsverktøyet implementeres nå ved Nyfødtintensiv ved Drammen sykehus.
Premature og syke nyfødte gjennomgår mange smertefulle prosedyrer og stressende behandlinger i løpet av oppholdet i nyfødtavdelingen. COMFORTneo-observasjonsverktøy er oversatt til norsk og implementert ved Nyfødtintensiv, Drammen sykehus.
Bakgrunn
Premature og syke nyfødte barn opplever mye stress og smerte i løpet av oppholdet på Nyfødtintensiv. De uheldige konsekvensene av en slik negativ påvirkning er grundig dokumentert gjennom forskning (1–3). Det er således faglig og etisk riktig å gi god smertebehandling til denne sårbare gruppen barnepasienter. En nylig publisert europeisk studie viste at kun 10 prosent av premature og syke nyfødte blir rutinemessig vurdert for pågående stress og smerte (4).
En systematisk kartlegging av smerte og stress anbefales gjennomført regelmessig via et validert smertevurderingsverktøy (5). Alle nyfødtintensivavdelinger bør ha en smerteprosedyre som er kunnskapsbasert og gir føringer for farmakologisk og ikke-farmakologisk smertelindring (4).
Nyfødtintensiv
I 2012 bygget Nyfødtintensiv i Drammen, som første norske nyfødtseksjon, enerom til alle pasientene med soveplass til begge foreldrene. Seksjonen er definert som nivå II, og behandler barn født ned til 12 uker før termin. Fødepopulasjonen er rundt 5000 fødsler per år. Driften i den nye seksjonen er bygget opp rundt familiesentrert omsorg (FCC) og hud-mot-hud-omsorg (SSC), og vi tilrettelegger for at foreldrene skal være til stede hos barnet sitt døgnet rundt. Seksjonens definerte mål er at foreldrene skal delta i omsorgen for barnet så tidlig som mulig etter fødselen, og i tillegg skal barnet ha hud-mot-hud-omsorg så mye som mulig gjennom sykehusopphold
Familiesentrert omsorg
Familiesentrert omsorg (FCC) er et sentralt begrep og ansees som gullstandard behandling for det for tidlig fødte barnet (6, 7). Shields et al. definerer familiesentrert omsorg som «en måte å gi omsorg til barnet og familien innen helsetjenesten som sikrer at pleie og omsorg omfatter hele familien og ikke bare barnet, og der alle familiemedlemmene er anerkjent som omsorgsmottakere» (7). Alle som har en biologisk, følelsesmessig eller juridisk forbindelse til barnet, kan defineres som familie. Den norske forskriften om barns opphold på sykehus slår fast at barnet har rett til å ha en av foreldrene hos seg under hele oppholdet (8).
Det er stor interesse for familiesentrert omsorg i nyfødtmiljøet nasjonalt og internasjonalt. Svenske nyfødtavdelinger var tidlig ute med å legge om driften til enerom med kontinuerlig foreldretilstedeværelse og har publisert flere studier der de har evaluert og utforsket ulike perspektiver rundt en slik familiesentrert driftsmodell (9–11). Det er ikke en forutsetning for familiesentrert omsorg at foreldrene har enerom inne på seksjonen. Samtidig ses det som en betydelig fordel for det premature barnet og foreldrene (9).
Det er dokumentert en rekke positive effekter av enerom for barnet. Blant annet er det vist at familiesentrert omsorg og enerom gir redusert liggetid for premature barn og redusert risiko for utvikling av lungesykdommen bronkopulmonal dysplasi (9). Eneromsmodellen er også assosiert med færre tilfeller av sepsis, mindre behov for oksygen og høyere ammefrekvens ved utskrivelse (12).
Hud-mot-hud-omsorg
Hud-mot-hud-omsorg (SSC) er en del av en omsorgsmodell kalt Kangaroo Mother Care (KMC) med opprinnelse fra Colombia på 1980-tallet. Metoden innebærer at mor kontinuerlig bærer barnet hud-mot-hud og at barnet utelukkende får morsmelk. WHO lanserte retningslinjer for gjennomføring av metoden i 2003 og definerte KMC som «tidlig, kontinuerlig og forlenget hud-mot-hud-kontakt mellom mor og barn, med eksklusiv amming, tidlig hjemreise og tett oppfølging hjemme» (13).
Den positive effekten hud-mot-hud-omsorg har vist seg å ha for det premature barnet er grundig dokumentert i internasjonale studier (14–18). Hud-mot-hud-omsorg gir bedre utkomme for det premature barnet knyttet til fysiologisk stabilitet, søvn, amming, smertelindring, hjerneutvikling og foreldretilknytning (17). Hud-mot-hud-omsorg har også vist seg å ha flere fordeler for mor. Det har gitt økt melkeproduksjon samt tidligere og sterkere tilknytning til barnet. Hudkontakt med barnet virker stressreduserende og gir en høyere grad av mestringsfølelse relatert til morsrollen (17).
Smerteprosjektet
Nyfødtintensiv i Drammen definerte i 2014 et mål om å arbeide mer systematisk med smerteobservasjon og behandling. En tverrprofesjonell faggruppe for smerte ble etablert. Gruppas første oppgave var å planlegge implementering av et verktøy for observasjon av stress og smerte. Dette var grundig forankret hos lederne for sykepleier- og legegruppa. I samarbeid med Lovisenberg diakonale høgskole og høyskolelektor Solfrid Steinnes gjorde vi en systematisk kartlegging av bruk av scoringsverktøy i Norge. I september 2015 reiste smertegruppa på besøk til Rigshospitalet i København. Alle danske nyfødtintensivseksjoner gjorde en felles implementering av smerteobservasjonsverktøyet COMFORTneo i 2012 (19). Smertegruppens medlemmer er nå sertifiserte COMFORTneo-superbrukere.
COMFORTneo
Observasjonsverktøyet COMFORTneo er en videreutviklet og nyfødttilpasset utgave av Comfort Behavior Scale (20). Barnet observeres i to minutter, og følgende atferdsparametere vurderes; våkenhet, ro/uro, respiratorisk respons hos intuberte, gråt hos selvpustende, kroppsbevegelse, ansiktstonus og kropps-/muskeltonus. Hver variabel gir 0–5 poeng, altså er maks poengsum 30. En poengsum lavere enn 9 regnes som unormalt, og kan være et uttrykk for oversedasjon om barnet får sedering. Lav score kan også være uttrykk for ekstrem smerte/shut down-respons. 9–13 poeng regnes som normalt, mens 14–16 er grenseverdi for mulig smerte. 17–21 poeng antyder moderat smerte, mens score høyere enn 22 antyder intens smerte. Verktøyet inneholder i tillegg en klinisk sykepleiers vurdering av smerte og stress (Numeric Rating Scale), separate score fra 1–10 hvor 1 er ingen smerte eller stress og 10 er verst mulig smerte eller stress. NRS-score fungerer som en vurdering av barnets kliniske situasjon.
Oversettelsesprosessen
VanDijk anbefalte at vi tok utgangspunkt i den engelske versjonen av COMFORTneo. Instrumentet ble oversatt i henhold til Wild’s 10. trinn for oversettelse og kulturell tilpasning av instrumenter som rapporterer helseutfall (21). Først ble det innhentet samtykke fra utvikler av instrumentet (trinn 1). Deretter ble COMFORTneo oversatt fra engelsk til norsk av to uavhengige oversettere som begge er spesialsykepleiere med kunnskap om nyfødte og smertevurdering (trinn 2). De to versjonene ble deretter sammenliknet og diskutert (trinn 3) av Lyngstad og Steinnes før en endelig versjon ble oversatt tilbake av en profesjonell translatør med kunnskap i helseterminologi (trinn 4). Denne versjonen ble deretter sammenliknet med originalversjonen, og språklige og konseptuelle forskjeller ble avdekket og diskutert (trinn 5).
I neste trinn (6) – harmonisering – gikk Lyngstad og Steinnes igjennom alle versjoner for å sikre at variablene i instrumentet hadde fått best mulig oversettelse og var forståelige og presise. Deretter ble den norske versjonen av COMFORTneo testet ut i et kognitivt fokusgruppe-intervju (trinn 7). Deltakerne i fokusgruppen var sykepleiere som tar videreutdanning i nyfødtsykepleie, og som har mye kunnskap om nyfødte og smertevurdering. Deltakerne tilførte verdifull informasjon om brukervennlighet og klinisk nytte. I trinn 8 foretok Lyngstad og Steinnes en gjennomgang av funnene fra de kognitive intervjuene, og den tverrfaglige smertegruppen kommenterte den endelige versjonen. Det ble imidlertid ikke endret i variablene i instrumentet. Trinn 9, korrekturlesing og trinn 10 – rapportskriving – ble utført av Lyngstad og Steinnes.
Flytskjema
Overlege på Nyfødtintensiv i Drammen, Flore Le Marechal, utviklet to ulike flytskjemaer som gir føringer for behandling og tidspunkt for rescoring ut fra score-verdier. Ett flytskjema omhandler selvpustende barn og ett intuberte barn. Cut off-score for ulike tiltak bygger på funn i litteraturen (22).
Implementering
Den praktiske implementeringen av COMFORneo på seksjonen startet opp høsten 2016. Vi arrangerte to fagdager for alle ansatte som omhandlet smerte hos nyfødte generelt og bruk av COMFORTneo spesielt. Deretter gjennomførte smertegruppa en systematisk opplæring av alle sykepleiere. Tre timer teori og praktisk opplæring ble lagt inn i turnus. Ved årsskiftet var 80 sykepleiere og fem nyfødt-overleger sertifisert til å utføre smerteobservasjoner ved hjelp av COMFORTneo. Kickoff ble avholdt ved oppstart 6. februar der vi inviterte til fest på seksjonen. Smertegruppa stilte i egendesignete T-skjorter og sang en hjemmelaget COMFORTneo-sang. Hensiktene var et ønske om positiv oppmerksomhet rundt prosjektet samt å skape lagånd i personalgruppa; dette gjør vi sammen!
En praktisk implementering handler om tett og kontinuerlig oppfølging. Daglig avholdes pulsmøter på seksjonen med fokus på fag. Pulsmøtene er en viktig arena for implementeringsarbeid. Pulstavlen er sentralt plassert på seksjonen, og personalet samles her fire ganger i døgnet. Alle COMFORTneo-observasjoner registreres systematisk av den enkelte sykepleier på pulsmøtet, og vi kan diskutere utfordringer og svare på spørsmål knyttet til praktisk bruk av observasjonsverktøyet. Visittgående lege etterspør forrige døgns observasjoner og de registreres rutinemessig i barnets journal.
Veien videre
COMFORTneo vil bli testet for sensitivitet og spesifisitet i en pilotvalidering. Deretter planlegges en mer omfattende valideringsstudie hvor COMFORTneo vil bli sammenliknet med et annet smertevurderingsinstrument og Skin Conductance Algesimeter (SCA). Interrater-reliabilitetstesting vil også gjennomføres. Videre planlegges en intervensjon rettet mot foreldre i en familiesentrert modell.
Referanser
1. Bellieni CV. Pain assessment in human fetus and infants. The AAP Journal 2012;14(3):456–61.
2. Vinall J et al. Neonatal pain in relation to postnatal growth in infants born very preterm. Pain. 2012;153(7):1374–81.
3. Brummelte S. Cortisol levels in former preterm children at school age are predicted by neonatal procedural pain-related stress. Psychoneuroendocrinology. 2015;51:151–63.
4. Anand KJS, Eriksson M, Boyle EM, Avila-Alvarez A, Andersen RD, Sarafidis K et al. Assessment of continuous pain in newborns admitted to NICUs in 18 European countries. Acta Pædiatrica. 2017 Mar 3.
5. Anand KJS. Prevention and treatment of neonatal pain. 2016. Tilgjengelig fra: https://www.uptodate.com/contents/prevention-and-treatment-of-neonatal-… (nedlastet 09.06.2017).
6. Malusky SK. A Concept Analysis of Family-Centered Care in the NICU. Neonatal Network. 2005 Nov-Dec;24(6):25–32.
7. Shields L, Pratt J, Hunter J. Family centred care: a review of qualitative studies. Journal of clinical nursing 2006 Oct;15(10):1317–23.
8. Forskrift om barns opphold i helseinstitusjon. Kap. 2. Tilgjengelig fra: https://lovdata.no/dokument/SF/forskrift/2000-12-01-1217 (nedlastet 09.06.2017).
9. Örtenstrand A, Westrup B, Broström EB, Sarman I, Åkerström S, Brune T et al. The Stockholm Neonatal Family Centered Care Study: Effects on Length of Stay and Infant Morbidity. Pediatrics 2010 Feb;125(2):e278–85.
10. Wigert H, Hellström AL, Berg M. Conditions for parents’ participation in the care of their child in neonatal intensive care – a field study. BMC Pediatrics 2008;8(3):1–9.
11. Flacking R, Thomson G, Ekenberg L, Löwengren L, Wallin L. Influence of NICU co-care facilities and skin-to-skin contact on maternal stress in mothers of preterm infants. Sexual & Reproductive Healthcare 2013 Oct;4(3):107–12.
12. Pineda RG, Stransky KE, Rogers C, Duncan MH, Smith GC, Neil J, Inder, T. The single-patient room in the NICU: maternal and family effects. Journal of Perinatology 2012 Jul;32(7):545–51.
13. Verdens helseorganisasjon (WHO) Kangaroo Mother Care. A practical guideline. World Health Organization. 2003.
14. Blomqvist YT. Kangaroo Mother Care. Parents`experiences and patterns of application in two Swedish neonatal intensive care units. (Doktoravhandling). Uppsala: Uppsala universitet. 2012.
15. Feldman R, Rosenthal Z, Feldman A (2014). Maternal-Preterm Skin-to-Skin Contact Enhances Child Psysiologic Organization and Cognitive Control Across the First 10 years of Life. Biological Psychiatry. 2014 Jan 1;75(1):56–64.
16. Ludington-Hoe S. Kangaroo care as a neonatal therapy. Newborn and Infant Nursing Reviews 2013;(2):73–5.
17. Campbell-Yeo ML, Disher TC, Benoit BL, Johnston CC. Understanding kangaroo care and its benefits to preterm infants. Pediatric Health, medicine and Therapeutics 2015;(6):15–32.
18. Boundy EO, Dastjerdi R, Spigelman D, Fawzi WW, Missmer SA, Lieberman E et al. Kangaroo mother care and neonatal outcomes: A meta-analysis. Pedriatics. 2016;(1):1–16.
19. Aarhus universitet, Center for kliniske retningslinjer. Klinisk retningslinje for smertevurdering af neonatale børn. Tilgjengelig fra: http://www.cfkr.dk/images/71_klinisk-retningslinje-for-smertevurdering-… (nedlastet 09.06.2017).
20. Wild D, Grove A, Martin M, Eremenco S, McElroy S, Verjee-Lorenz A, Erikson P. Principles of good practice for the translation and cultural adaptation process for Patient-Reported Outcomes (PRO) Measures: Report of the ISPOR Task Force for Translation and Cultural Adaption. Value in Health. Vol 2015;8(2):94–104.
21. Aukes DI, Roofthooft DW, Simons SH, Tibboe D, van Dijk M. Pain management in neonatal intensive care evaluation of the compliance with guideline. Clin J Pain 2014 Nov 3.























0 Kommentarer