Betre kvalitet med behandlingsliner
Standardiserte behandlingsliner er et verkty som kan betre pasienttryggleiken og ressursutnyttinga.
Standardiserte behandlingsliner (pasientforløp/care pathways) er i aukande grad brukte internasjonalt som verkty for kvalitetsbetring i helsetenesta (1). Slike standardiserte behandlingsliner betrar ei rekke prosess- og utkommemål. Tilnærminga er oftast brukt innan sjukehus på homogene pasientgrupper med einsarta forløp. Men behandlingslinene har også stort potensiale for bruk på grupper med meir komplekse behov og i tverrsektoriell samhandling.
Standardisert behandlingsline
Der er mange ulike definisjonar av standardiserte
behandlingsliner (2), og terminologien, til dømes pasientforløp,
«critical-/clinical pathway», «care track», varierer (2). European
Pathway Association (E-P-A, sjå
www.e-p-a.org) er ein
non-profit organisasjon for nettverk, brukargrupper, akademiske
institusjonar, sjukehus, støtteorganisasjonar og tilsette i
helsetenestene som ynskjer bidra til utvikling og implementering av
standardiserte behandlingsliner. Organisasjonen har sterkt fokus på
evidensbaserte tiltak og forsking. E-P-A definerer ei standardisert
behandlingsline («care pathway») slik (3, 4): «Ei behandlingsline
er ein kompleks intervensjon som har gjensidig taking av avgjerder
og organisering av behandlingsprosessen for ei definert gruppe
pasientar i ein definert tidsperiode som mål. Karakteristika ved ei
standardisert behandlingsline er (2-4):
ei eksplisitt uttrykt utsegn om måla og nøkkelelementa i
behandlinga basert på evidens, beste praksis og pasientane sine
karakteristika og forventningar
tilrettelegging for kommunikasjon mellom teammedlemmene,
pasientane og deira pårørande
koordinering av behandlingsprosessen ved å koordinere rollene
og aktivitetane stegvis (sekvensielt) i det tverrfaglege teamet,
med omsyn til pasientane og dei pårørande
dokumentering, monitorering og evaluering av variasjonar og
utkommer
identifisering av naudsynte ressursar
Målet med å standardisere pasientforløpa er altså å betre
kvaliteten av pleie og behandling gjennom heile behandlingsforløpet
ved å betre risikojusterte pasientutkommer, betre pasienttryggleik
og optimalisere ressursutnyttinga. Ein slik definisjon av
standardiseringa av behandlingsprosessen som over, er langt meir
strikt enn mange andre kvalitetsbetringsintervensjonar.
Effekt
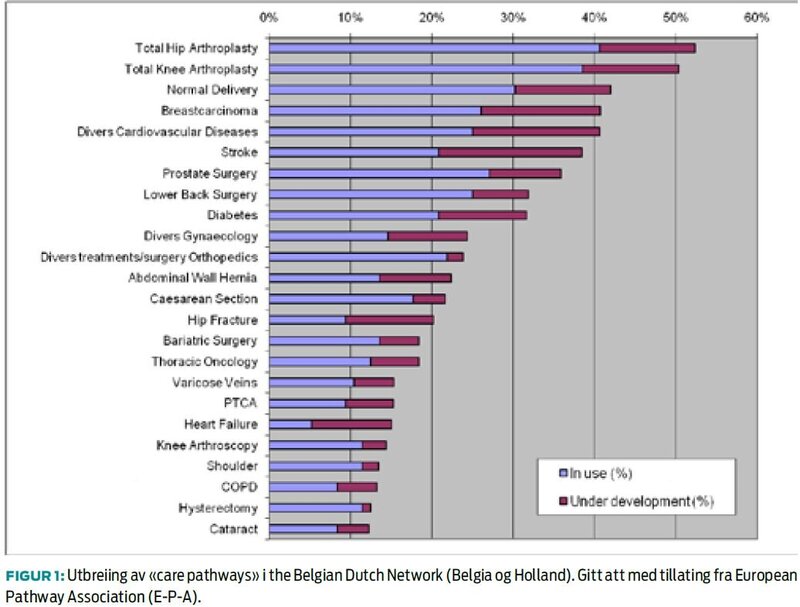
Mange internasjonale studier gjennomført dei siste tjue åra har vist at standardiserte behandlingsliner har effekt. Mest overtydande evidens er difor at implementeringa av desse betrar pasientutkommer og kostnad-nytte-ratioet (5-8). Men der er også mange studier som har vist at implementeringa av standardiserte behandlingsliner fører til kortare liggetid, lågare insidens av postoperative komplikasjonar og betra dokumentasjon (6, 9). Standardiseringa er best eigna på homogene pasientgrupper der alle skal gjennomgå det samme i løpet av sjukehusopphaldet. Difor er denne tilnærminga ofte nytta i kirurgiske fag, særleg i elektiv kirurgi (figur 1). Men tilnærminga er også forsøkt i pasientutval med lågare grad av prediktabilitet i åtferd og behandlingsbehov, der såkalla Hub-, eller Web-modellar for organiseringa av helsetenesta er meir eigna enn ei enkel line- (Chain-)tilnærming (10). Dette gjeld til dømes i rehabilitering (11), rus, psykiatri (12, 13) og palliativ behandling (14). I slike studier finn ein ofte ei meir fleirsidig tilnærming med element av «case management».
Framgangsmåte
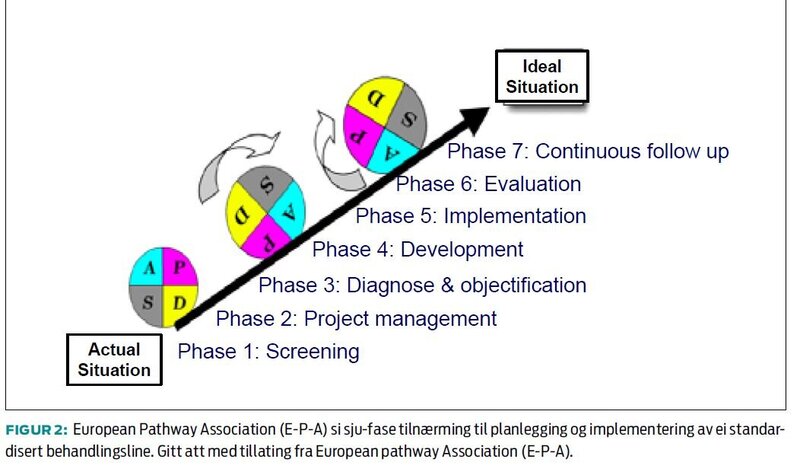
Planlegginga og implementeringa av behandlingslina for den utvalde pasientgruppa føregår i den enkelte kliniske eininga med utgangspunkt i det kliniske mikroteamet og Plan-Do-Check-Act (PDCA-) sirkelen (Deming’s sirkel) (15). Triaden av engasjert sjukepleiar (ansvarleg for det praktiske, til dømes møteinnkallingar og registrering av data), engasjert klinikar (til dømes overlækjar), og einingsleiar vil ofte vere eit godt utgangspunkt. Gruppa som arbeider med behandlingslina skal vere tverrfagleg og alle grupper som har med pasienten å gjere skal vere representerte, også til dømes laboratorietenestene. Ein pasientrepresentant bør vere med for å sikre brukarperspektivet. Det er vanleg at ein kompetent kvalitetsrådgjevar (fasilitator) gir råd i planlegginga og implementeringa, som ofte strekker seg over seks til ni månader. Kvalitetsrådgjevar har oversikt over aktuelle verkty som kan nyttast i prosessen (til dømes tre-tavle-teknikk (16), Gantt-diagram, og årsak–verknad diagram). E-P-A har utvikla ein sjufasemodell for planlegging, implementering, evaluering og kontinuerlig oppfølging av ei standardisert behandlingsline (figur 2). Denne bygger på prinsippet om kvalitetsbetring som ein kontinuerleg prosess, og bør saman med «Leuven Clinical Pathway Compass» (17) vere til hjelp for tilsette i norsk helseteneste som ynskjer lage ei behandlingsline i si eining.
Forskingsbehovet
Der er i dag behov for meir evaluering av standardiserte
behandlingsliner. Mange effektstudier er allereie utført (6), men
mange av desse er hemma av låg statistisk styrke på grunn av få
deltakarar (18), få indikatorar på prosess- og utkommer (dårleg
validitet) (18, 19), kort oppfølgingstid (18-21), forskingsdesign
utan parallellkontroll (18-21), og/eller at nøkkelelementa i
behandlingslinene varierer og ikkje er i tråd med ein overordna
definisjon av kva ingredienser ei standardisert behandlingsline
skal ha (2, 6). Fagfeltet treng meir evidens når det gjeld
spørsmåla:
kva verkar standardiserte behandlingsliner på (kva
pasientgrupper, kva prosess- og utkommemål)?
korleis verkar standardiserte behandlingsliner (verksame
ingrediensar=?)?
effekten av tverrsektorielle behandlingsliner (særlig relevant
i samband med Samhandlingsreformen)?
Nyleg vart det oppretta ein eigen norsk nasjonal seksjon av
E-P-A, som ønsker nye norske helsearbeidarar velkomne som
medlemmer. Seksjonen heldt eit vellukka tredagars kurs i
planlegging og implementering av standardiserte behandlingsliner på
Solstrand Fjord Hotel i Os ved Bergen i september 2011. I framtida
ønsker E-P-A å inspirere til etablering av gode evidensbaserte
standardiserte behandlingsliner i Noreg og til evalueringa av
desse.
Litteratur
1. Vanhaecht K, Bollmann M, Bower K, Gallagher C, Gardini
A, Guezo J, et al. Prevalence and use of clinical pathways in 23
countries - an international survey by the European Pathway
Association. J Integr Care Pathways 2006(10):28-34.
2. De Bleser L, Depreitere R, De Waele K, Vanhaecht K,
Vlayen J, Sermeus W. Defining pathways. J Nursing Management
2006;14(7):553-63.
3. Vanhaecht K, Panella M. Is there still need for
confusion about pathways? International Journal of Care Pathways
2010;14(1):1-3.
4. Vanhaecht K, Sermeus W, De Witte K. General
Introduction. In: Vanhaecht K SW, De Witte K, editor. The impact of
clinical pathways on the organisation of care processes. Leuven:
ACCO, 2007: 3-18.
5. Campbell H, Hotchkiss R, Bradshaw N, Porteous M.
Integrated care pathways. BMJ 1998; 316: 133-37.
6. Rotter T, Kinsman L, James E, Machotta A, Gothe H,
Willis J, et al. Clinical pathways: effects on professional
practice, patient outcomes, length of stay and hospital costs
(Review). The Cochrane Library. 2010(3).
7. Van Herck P, Vanhaecht K, Sermeus W. Effects of
clinical pathways: do they work? J Integr Care Pathways 2004; 8(3):
95-104.
8. Panella M, Marchisio S, Demarchi M, Manzoli L, Di
Stanislao F. Reduced in-hospital mortality for heart failure with
clinical pathways: the results of a cluster randomized controlled
trial. Qual Saf Health Care 2009; 18: 369-73.
9. Bandolier. On care pathways. Bandolier Forum.
2003(July):1-12.
10. Vanhaecht K, Panella M, Van Zelm R, W S. What about
care pathways? In: Ellershaw J, editor. Care of the dying. 2nd ed.
Oxford: Oxford University Press, 2010:1–14.
11. Falconer JA RE, Sutin JA, Strasser DC, Chang RW. The
critical path method in stroke rehabilitation: lessons from an
experiment in cost containment and outcome improvement. QRB Qual
Rev Bull 1993; 19(1): 8-16.
12. Bauer M, McBride L, Williford W, Glick H, Kinosian B,
Altshuler L, et al. Collaborative Care for Bipolar Disorder: Part
II. Impact on Clinical Outcome, Function, and Costs. 2006.
13. Biringer E, Hartveit M. A future for pathways in
mental health care in Norway-a discussion paper based on El- Ghorr
et al. (2010). International Journal of Care Pathways
2010;accepted.
14. Bookbinder M, Blank AE AE, Wollner D, Lesage P,
McHugh, M ea. Improving end-of-life care: Development and
pilot-test of a clinical pathway. J Pain Symptom Manag 2005; 29(6):
529-43.
15. Deming W. Quality Predictivity and Competitive
Positions. Cambridge, MS: MIT Press, 1982.
16. Vanhaecht K, Van Zelm R, Van Gerven E, Sermeus W,
Bower K, Panella M, et al. The 3-blackboard method as
consensus-development exercise for building care pathways. Int J
Care Pathways 2010; 15(3): 49-52.
17. Vanhaecht K, Sermeus W. The Leuven Clinical Pathway
Compass. Journal of Integrated Care Pathways 2003;7 (1):2-7.
18. Cooney R, Bryant P, Haluck R, Rodgers M, Lowery M. The
Impact of a Clinical Pathway for Gastric Bypass Surgery on Resource
Utilization. J Surg Res 2001; 98(2): 97-101.
19. Huerta S, Heber D, Sawicki M, LIU C, Arthur D,
ALEXANDER P, et al. Reduced length of stay by implementation of a
clinical pathway for bariatric surgery in an academic health care
center. Am Surgeon. 2001;67(12):1228-35.
20. Rouse A, Tripp B, Shipley S, Pories W, Cunningham P,
MacDonald K. Meeting the Challenge of Managed Care Through Clinical
Pathways for Bariatric Surgery Obes Surg. 1998;8(5):530-4.
21. Yeats M, Wedergren S, Fox N, Thompson J. The Use and
Modification of Clinical Pathways to Achieve Specific Outcomes in
Bariatric Surgery Am Surgeon.
2005;71(2):152-4(3).




















0 Kommentarer