Hypotermi hos operasjonspasienter ved ankomst til postoperativ avdeling
Sammendrag
Bakgrunn: Utilsiktet hypotermi hos operasjonspasienter kan gi uheldige konsekvenser som blant annet økt blødningsrisiko og infeksjonsfare. De siste tiårene er ulike tiltak blitt innført for å redusere varmetap hos pasienter før, under og etter operasjon. Praksisen kan likevel variere, og pasienter kan fortsatt bli utsatt for hypotermi.
Hensikt: Å kartlegge forekomsten av hypotermi blant elektive pasienter som har gjennomgått abdominal kirurgi eller torakskirurgi i generell anestesi, og undersøke om typen og varigheten av kirurgi, pasientens sykdomstilstand, alder og kjønn har sammenheng med hypotermi.
Metode: Prospektiv observasjonsstudie som ble utført på et universitetssykehus i Norge. Ett hundre pasienter fikk målt øretemperaturen (Tp) på tre tidspunkter: før kirurgisk inngrep, ved ankomst til postoperativ avdeling og én time etter ankomst til postoperativ avdeling. Vi samlet inn dataene i perioden desember 2017–januar 2018 og analyserte med deskriptiv statistikk og regresjonsanalyse.
Resultat: Tjuefire prosent av pasientene i studien var hypoterme (Tp < 36,0 °C) ved ankomst til postoperativ avdeling. Én time etter ankomst til postoperativ avdeling var 13 prosent av pasientene hypoterme. Regresjonsanalysen indikerte at pasienter med høy alder (p = 0,008) og som hadde gjennomført laparoskopisk kirurgi (p = 0,018), hadde signifikant høyere odds for lavere temperatur ved ankomst til postoperativ avdeling.
Konklusjon: Forekomsten av hypotermi blant operasjonspasienter som ankommer postoperativ avdeling, er fortsatt for høy. Spesielt eldre mennesker og pasienter som har fått utført laparoskopisk kirurgi, var utsatt for lavere kroppstemperatur. Resultatene bør føre til mer systematisk måling av temperatur og bedring av varmetiltak til operasjonspasienter, både på anestesiavdeling, operasjonsavdeling og postoperativ avdeling.
Referer til artikkelen
Bjørnø M, Mevik M, Løining D, Dalen I, Morken I. Hypotermi hos operasjonspasienter ved ankomst til postoperativ avdeling. Sykepleien Forskning. 2020;15(81641):e-81641. DOI: 10.4220/Sykepleienf.2020.81641
Å bevare pasientens normale kroppstemperatur i pre-, per- og postoperativ periode er svært viktig for pasientsikkerheten, forventet kirurgisk resultat og pasienttilfredsheten (1, 2).
Risikoen for hypotermi er spesielt høy for pasienter med alder > 60 år som har mangelfull ernæringsstatus og tilleggssykdommer som nedsetter termoreguleringen (3).
Utilsiktet hypotermi hos operasjonspasienter kan forlenge effekten av generell anestesi, redusere infeksjonsforsvaret med høyere forekomst av sårinfeksjoner, redusere sårtilhelingen og gi høyere forekomst av blødninger. Disse komplikasjonene kan føre til et behov for blodtransfusjon, forlenget mekanisk ventilasjon og økt sirkulasjonsstøtte (2, 4).
Operasjonspasienten blir ofte utsatt for varmetap på grunn av avkledning, lav temperatur i operasjonssalen, generell anestesi, kirurgisk inngrep av lengre varighet, laparotomi og innblåsing av kald og tørr CO₂-gass ved laparoskopi (5–8).
Laparotomi er et kirurgisk inngrep hvor bukhulen åpnes – åpen kirurgi, mens laparoskopi er et kirurgisk inngrep som utføres endoskopisk – kikkhullskirurgi (5–8).
Selv mild hypotermi, definert som kjernetemperatur mellom 35,0 og 36,0 °C, kan føre til alvorlige komplikasjoner (2, 9). Derfor er det viktig å systematisk måle og dokumentere pasientens temperatur for raskt å kunne identifisere og behandle hypotermi (3).
De siste tiårene har ulike tiltak som adekvat tildekking, varme infusjons- og skyllevæsker og bruk av varmelaken og varmluftstepper blitt iverksatt for å redusere varmetap hos pasienten før, under og etter operasjon (10–13). Likevel viser studier at forekomsten av hypotermi hos pasienter ved ankomsten til postoperativ avdeling er høy (17–46 prosent) (14, 15).
Den første postoperative perioden er risikofylt
Mens anestesi- og operasjonssykepleierne har ansvaret for å forebygge hypotermi blant pasientene før og under operasjon, har intensivsykepleierne et særskilt ansvar for pasientens temperatur ved ankomsten til postoperativ avdeling. Dersom kroppstemperaturen synker, øker faren for komplikasjoner og ytterligere belastninger for en allerede sårbar pasient.
Intensivsykepleierne har et særskilt ansvar for pasientens temperatur ved ankomsten til postoperativ avdeling.
Den første postoperative perioden er mest risikofylt for pasientene. Det er derfor viktig at operasjons-, anestesi- og intensivsykepleierne observerer og registrerer vitale parametere for å forebygge og behandle komplikasjoner som kan oppstå (3, 12).
De internasjonale retningslinjene for hypotermi anbefaler varmetiltak til alle operasjonspasienter og måling av temperatur kontinuerlig eller hvert 15. minutt i pre- og peroperativ periode.
Dersom pasienten er hypoterm ved ankomsten til postoperativ avdeling, skal det iverksettes ytterligere varmetiltak og temperaturen måles hvert 15. minutt inntil pasienten oppnår normal temperatur (3, 16).
Sykepleierne manglet kjennskap til retningslinjer
Det kan derimot være vanskelig å gjennomføre retningslinjer. Studier har vist at sykepleierne har hatt lite kjennskap til retningslinjene og hatt manglende kunnskap om hypotermi (17, 18).
Mens varmetap ved laparotomisk og lengre tids kirurgi kan være velkjent og pasientene får gode varmetiltak, kan for eksempel varmetap ved mindre kirurgiske inngrep og laparoskopi være mindre kjent (19).
Hensikten med studien
Hvor gode rutiner sykepleierne har for temperaturkontroll og tiltak for å forebygge hypotermi blant ulike operasjonspasienter, kan dermed variere.
Vi ønsket derfor å undersøke om det forekom hypotermi blant pasientene ved ankomst og under opphold på postoperativ avdeling, og undersøke om ulike faktorer hadde sammenheng med hypotermi.
Hensikten med studien var todelt:
- Å kartlegge forekomsten av hypotermi blant elektive pasienter som hadde gjennomgått abdominal kirurgi eller torakskirurgi i generell anestesi, og
- å undersøke om typen og varigheten av kirurgi, pasientens sykdomstilstand, alder og kjønn hadde sammenheng med hypotermi.
Metode
Design
Studien var en prospektiv observasjonsstudie. Vi samlet inn dataene på anestesiavdelingen og postoperativ avdeling på et større sykehus i Norge.
Deltakere
Vi inviterte pasienter til å delta i studien på tilfeldige dager i løpet av en tomånedersperiode. Inklusjons- og eksklusjonskriteriene var som følger:
Inklusjonskriterier:
- alder > 18 år
- planlagt utførelse av et kirurgisk inngrep i abdomen eller toraks
- bruk av generell anestesi, med eller uten epidural anestesi
Eksklusjonskriterier:
- pasienter med temperatur over 37,5 °C som utgangspunkt før operasjon
- øyeblikkelig hjelp-pasienter
- pasienter som ikke har blitt oppfattet som klare og orienterte, eller som ikke er norsk- eller engelsktalende
- pasienter som av en eller annen grunn må avvike fra planlagt operasjon
- gynekologisk kirurgi og kvinner med kjent graviditet
Datainnsamling
Datainnsamlingen foregikk i perioden fra desember 2017 til januar 2018. Alle pasientene som ble invitert til studien, takket ja. Vi registrerte temperaturen med et infrarødt øretermometer på tre tidspunkter: 1) før kirurgisk inngrep, 2) ved ankomst til postoperativ avdeling og 3) én time etter ankomst til postoperativ avdeling.
Operasjonsprogrammet med oversikt over operasjonens varighet og tidspunktet for overflytting til postoperativ avdeling ble brukt for å sikre at vi samlet inn dataene på rett tidspunkt.
Tympanisk temperaturmåling
Tympanisk temperaturmåling er et infrarødt øretermometer som måler pasientens kjernetemperatur ved å måle blodets temperatur i det arterielle blodet som passerer hypothalamus og trommehinnen i øregangen (20).
Studier viser at øretemperaturen målt med anvendt aurale prober er pålitelig for å kartlegge temperaturen og gunstig med tanke på tidsbruk og anvendelighet (15, 20). Øretermometeret som vi brukte i denne studien, var av merket Braun.
Termometeret ble på forhånd merket slik at vi kunne bruke det samme termometeret på alle pasientene. Første-, andre- og tredjeforfatteren gjennomgikk bruksanvisningen og prosedyren for øretemperaturmåling i fellesskap før oppstart for å sikre en pålitelig temperaturregistrering.
Under datainnsamlingen var alltid to av de nevnte forfatterne til stede. Alle tre deltok like mange dager under datainnsamlingen.
To av de nevnte forfatterne målte pasientens temperatur to ganger i samme øre for å utelukke feilmåling. Så lenge pasienten ikke hadde synlig ørevoks eller nylig hadde tildekket øret, målte vi temperaturen fra pasientens høyre øre.
Temperaturen ble nedskrevet i to ulike skjemaer før de ble sammenliknet. Dersom temperaturene avvek med flere desimaler eller var utenfor normalt referanseområde, tok vi ny måling.
Den høyeste registrerte temperaturen ble brukt under dataanalysen. Den høyeste temperaturen er sannsynligvis mer representativ for pasientens kjernetemperatur, da termometeret har vært lenger inn i øregangen og dermed truffet den tympaniske membranen bedre (12). Vi analyserte temperaturen som en kontinuerlig variabel.
Uavhengige variabler
Vi registrerte kliniske variabler fra pasientens operasjons- og anestesijournal etter utført kirurgi. Disse variablene var type kirurgi (laparaskopi/laparotomi), alder, kjønn, ASA-klasse og operasjonens varighet. Vi registrerte ikke hvilken spesifikk operasjon den enkelte pasienten fikk utført, eller hvilken type varmetiltak som var iverksatt før, under og etter operasjonen.
Varigheten på operasjonen ble dikotomisert til under to timer versus over to timer. Vi satte denne grensen på grunnlag av en metaanalyse som viser at en operasjon over to timers varighet dobler faren for komplikasjoner (21). Type kirurgi ble kategorisert til laparoskopisk eller laparotomisk kirurgi.
American Society of Anesthesiologists (ASA) klassifikasjon er en skala som brukes for å vurdere pasientens risikofaktorer i forbindelse med anestesi. ASA-klassifiseringen går fra klasse 1 til klasse 5, hvor klasse 1 symboliserer en frisk person, mens klasse 5 symboliserer en svært syk pasient med redusert sjanse for å overleve (22).
Analyse
Etter datainnsamlingen skrev vi inn primærdataene i dataprogrammet Statistical Package for the Social Sciences (SPSS), versjon 19.0.
Den statistiske analysen inkluderte deskriptiv statistikk (gjennomsnitt, standardavvik [SD], prosenter, boksdiagram), grafisk fremstilling (boksplott) og enkel og multippel lineær regresjonsanalyse.
Multippel lineær regresjonsanalyse ble utført for å teste sammenhengen mellom de ulike uavhengige variablene og den avhengige variabelen hypotermi. Det valgte signifikansnivået var en p-verdi < 0,05.
Etiske overveielser
Sykehusets personvernombud godkjente studien som et kvalitetsforbedringsprosjekt. Vi ga muntlig informasjon om studien til alle pasientene i studien før oppstarten, og alle skrev frivillig under på et samtykkeskjema for deltakelse.
Pasientene fikk med seg et informasjonsskriv om studien etter operasjonen med mulighet for å trekke seg fra studien hvis ønskelig.
Vi oppbevarte samtykkeskjemaet og nummererte temperaturskjemaer med variabler atskilt fra hverandre i to låste skap. Alle skjemaene ble makulert etter at vi hadde utført dataanalysen.
Resultater
De fleste pasientene som ble inkludert i studien, hadde fått utført kirurgi knyttet til lungekreft, aortaaneurisme, gallestein, nyrekreft, utlegging av tykktarms- eller tynntarmsstomi og fedmekirurgi.
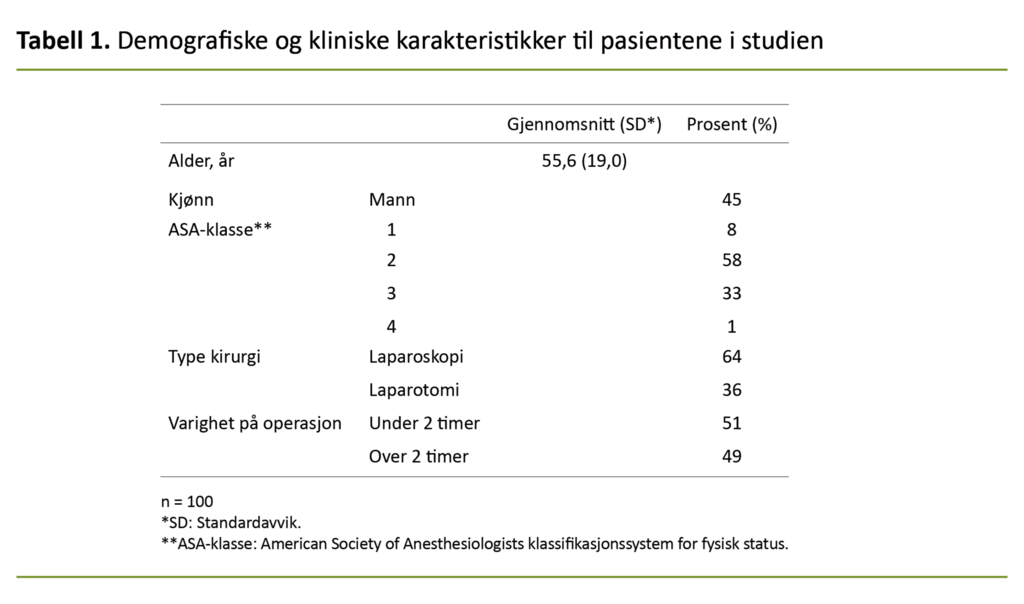
Til sammen inkluderte vi 100 pasienter i studien. Av dem var 45 menn og 55 kvinner. Alderen varierte fra 19 til 93 år med en gjennomsnittsalder på 56 år (SD = 19) (tabell 1). Alle pasientene lå i seng i påvente av operasjon.
Figur 1 viser et boksdiagram over mediantemperaturen og kvartiler ved de tre måletidspunktene. Den laveste registrerte temperaturen på 35,1 °C ble målt ved ankomsten til postoperativ avdeling.
Mediantemperaturen for alle tre tidspunktene var innenfor normaltemperatur: før kirurgi 36,7 °C, ved ankomst til postoperativ avdeling 36,4 °C og 36,5 °C én time etter ankomst til postoperativ avdeling.
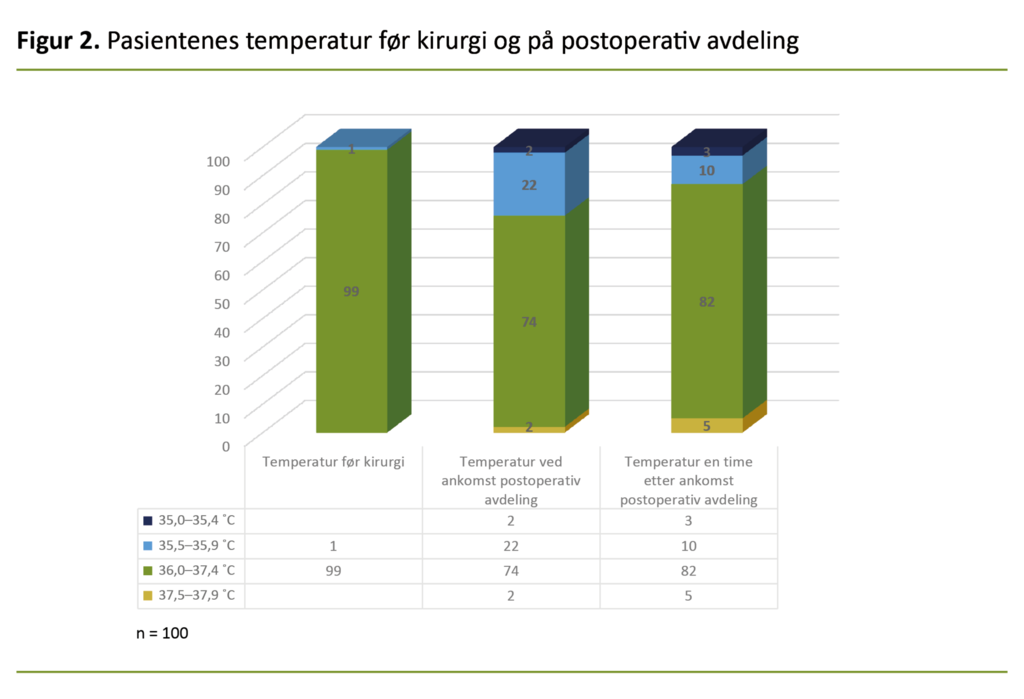
I figur 2 presenterer vi dataene i et histogram med tre stolper som symboliserer de tre forskjellige tidspunktene for temperaturkontroll. Av 100 pasienter var 37 pasienter registrert hypoterme ved ett tidspunkt eller begge tidspunktene på postoperativ avdeling.
Det var 24 prosent av pasientene som var hypoterme ved ankomsten til postoperativ avdeling, mens 13 prosent var hypoterme én time etter ankomsten.
Det var 24 prosent av pasientene som var hypoterme ved ankomsten til postoperativ avdeling.
To pasienter hadde en temperatur på mindre enn 35,4 °C ved ankomsten til postoperativ avdeling, mens dette antallet hadde økt til tre pasienter én time etter ankomsten til postoperativ avdeling.
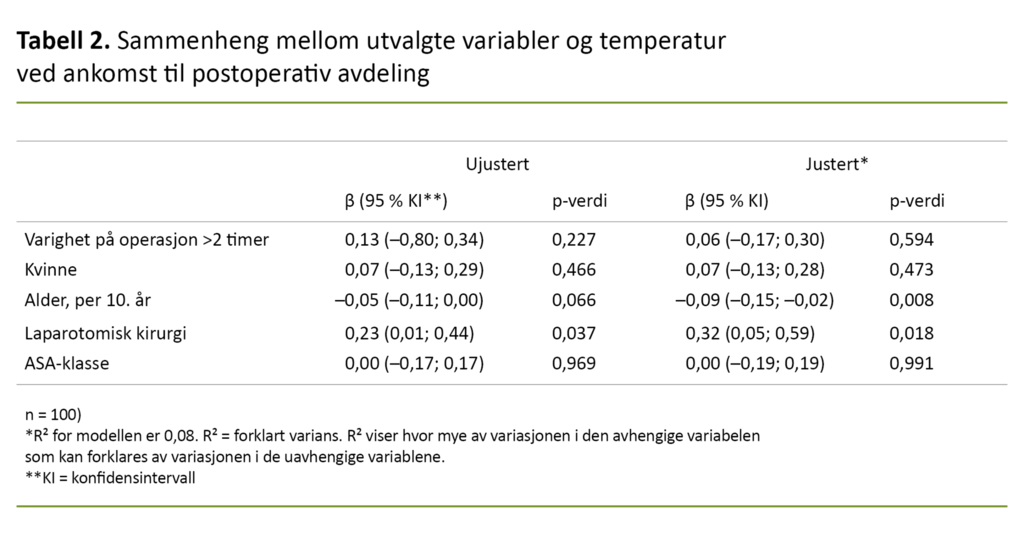
Resultatene fra den multiple lineære regresjonsanalysen viser at type kirurgi og alder er statistisk signifikant assosiert med temperaturen ved ankomst til postoperativ avdeling. Funnene indikerer at for hvert tiende års økning i alder synker forventet kjernetemperatur med 0,1 °C.
Pasienter som hadde fått utført laparoskopisk kirurgi, hadde i gjennomsnitt 0,32 °C lavere temperatur enn pasienter som hadde fått utført laparotomisk kirurgi.
I tabell 3 viser regresjonsanalysen at kun høy alder er statistisk signifikant med lavere temperatur én time etter ankomst til postoperativ avdeling.
De uavhengige variablene kan forklare temperaturen ved ankomsten til postoperativ avdeling med henholdsvis 8 prosent (tabell 2) og én time etter med 11 prosent (tabell 3).
Begge regresjonsanalysene viser at operasjonens varighet, ASA-klasse eller kjønn ikke har sammenheng med hypotermi blant pasienter på postoperativ avdeling.
Diskusjon
Hensikten med studien var å kartlegge forekomsten av hypotermi blant pasienter på postoperativ avdeling. I tillegg ville vi undersøke hvilke grupper av operasjonspasienter som var mest utsatt for hypotermi.
Funnene indikerte at forekomsten av hypotermi blant pasienter ved ankomst til postoperativ avdeling var høy (24 prosent). Grupper som var utsatt for lav kroppstemperatur, var eldre pasienter og pasienter som hadde fått utført laparoskopisk kirurgi.
Ivaretakelse av pasientens temperatur under operasjon
Andelen av postoperativ hypotermi (24 prosent) blant pasientene i studien kan tyde på at ikke alle har fått adekvate varmetiltak under den pre- og peroperative perioden. Tallet er høyere sammenliknet med en ny, stor tysk studie som viser en forekomst av 8,3 prosent postoperativ hypotermi (23).
Tallet er likevel sammenliknbart med funn fra andre studier som viser at forekomsten av postoperativ hypotermi blant pasientene varierer mellom 17 og 46 prosent (14, 15, 24). I alle disse studiene ble det brukt tympanisk temperaturmåling da temperaturen ble registrert.
På grunn av høy forekomst av per- og postoperativ hypotermi er det innført retningslinjer om preoperativ oppvarming av alle operasjonspasienter (3). En studie har vist at kun ti minutters preoperativ oppvarming kan være effektivt for å bevare pasientens normale temperatur under operasjonen (25).
I studien vår var det ingen sammenheng mellom enkelte velkjente risikofaktorer for å utvikle hypotermi, som lang varighet på operasjonen, laparotomisk inngrep og høyere ASA-klasse (7, 26). Dette funnet kan tyde på at grupper av pasienter har fått gode og effektive varmetiltak.
Eldre pasienter ble dårligere ivaretatt
Studien indikerte derimot at eldre pasienter ikke ble godt nok ivaretatt. Det var en sammenheng mellom pasientens høye alder og lavere kroppstemperatur. Eldre pasienter er predisponert for hypotermi på grunn av nedsatt termoregulering, som skyldes mindre muskelmasse og endret metabolisme (27).
I studien var det også en sammenheng mellom laparoskopisk kirurgi og lavere kroppstemperatur. Det kan tyde på at disse pasientene ikke har fått varmetiltak, eller at tiltakene ikke var effektive nok.
Studien indikerte at eldre pasienter ikke ble godt nok ivaretatt.
Ved laparoskopisk kirurgi blåses kald og tørr CO₂-gass inn i bukhulen, som fører til varmetap og økt risiko for å utvikle hypotermi (8).
Operasjonsteamet kjenner kanskje ikke alltid til dette. Laparoskopi utføres både ved større og mindre kirurgiske inngrep. I en spørreundersøkelse til operasjons-, anestesi- og intensivsykepleiere ble mindre kirurgi rangert som laveste risikofaktor for å utvikle hypotermi (18, 19).
Alle operasjonspasienter skal ha varmetiltak
En nyere randomisert studie har vist at det er signifikant bedre å forebygge hypotermi under laparoskopi med varmluftstepper enn å bruke passive varmetiltak når varigheten av prosedyren er over en time (28).
Ved den aktuelle operasjons- og anestesiavdelingen var det innført retningslinjer og prosedyrer for å forebygge hypotermi ved ulike kirurgiske inngrep. Vi registrerte dessverre ikke hvilke varmetiltak som ble iverksatt til pasientene i studien.
Ifølge retningslinjer for forebygging av utilsiktet hypotermi skal alle operasjonspasienter ha varmetiltak, og da fortrinnsvis varmluftstepper (3, 16, 29).
I National Institute for Health and Clinical Excellences (NICE) retningslinjer blir det anbefalt varmluftstepper til alle operasjonspasienter som får anestesi over 30 minutters varighet, og/eller som har temperatur under 36 °C når de gjøres klar til å overflyttes til postoperativ avdeling (9).
Ivaretakelse av pasientens temperatur under opphold på postoperativ avdeling
To av pasientene i studien hadde en temperatur under 35,4 °C ved ankomsten til postoperativ avdeling. Én time etter ankomsten var fortsatt 13 prosent av pasientene hypoterme, mens antallet pasienter med en temperatur på mindre enn 35,4 °C hadde økt til tre.
Én time etter ankomsten var fortsatt 13 prosent av pasientene hypoterme.
Vi vet at det ikke var innført retningslinjer for systematisk temperaturkontroll og varmetiltak til hypoterme pasienter på den aktuelle postoperative avdelingen der registreringen skjedde. Ifølge retningslinjene skal pasientens temperatur måles direkte etter ankomsten til postoperativ avdeling.
Målsettingen er å minimere varmetapet fra hud og utsatte områder, nedkjøling forårsaket av infusjon av kalde væsker eller bruk av kalde gasser for åndedrett. Pasienter som er hypoterme, skal varmes inntil de når normaltemperatur (11, 16).
Sykepleierne ble ikke opplyst om hypotermi blant pasientene
Selv om intervensjoner for oppvarming av pasienter med utilsiktet postoperativ hypotermi er de samme som ved pre- og peroperativ hypotermi, blir utgangspunktet helt forskjellig hos en våken pasient.
Behandling av hypotermi på postoperativ avdeling er sammensatt, der pasientens smerter, kvalme og skjelving har en sammenheng. Når hypotermi har oppstått, er det viktig at tiltak for å forsøke å varme opp pasienten skjer så raskt som mulig for å minimere mulige komplikasjoner.
De aller fleste pasientene er våkne rett etter at operasjonen er fullført, og det er viktig at ethvert tiltak er godt tolerert og effektivt (11, 16).
Vi opplevde det som forskningsetisk utfordrende ikke å opplyse om hypotermi blant pasientene til de pasientansvarlige sykepleierne. Temperaturen ble kun oppgitt til en intensivsykepleier på postoperativ avdeling ved ett tilfelle i starten av datainnsamlingen.
Dette tilfellet gjaldt en pasient som hadde en temperatur på 35,1°C én time etter ankomsten til postoperativ avdeling. På grunn av pasientens lave temperatur og kliniske tilstand vurderte vi at temperaturen burde vært informert om til den pasientansvarlige intensivsykepleieren.
Styrker og svakheter ved studien
Det er en styrke ved studien at tympanisk temperaturmåling blir mye brukt i tilsvarende studier (7, 14, 15, 24). Det gjør at resultatene kan sammenliknes.
Studien har flere svakheter. For det første har ikke tympanisk temperaturmåling samme pålitelighet som temperatur målt med et pulmonalt arteriekateter, som er et svært pålitelig mål på pasientens kjernetemperatur (30).
En studie har vist at tympanisk temperaturmåling måler 0,1–0,4 prosent lavere temperatur enn pulmonalt arteriekateter (30). Denne faktoren kan bidra til at forekomsten av hypotermi i studien vår er overestimert.
Men selv om man legger til 0,5 grader til den målte tympaniske temperaturen, vil det fortsatt forekomme hypotermi blant de inkluderte pasientene i studien.
For å styrke påliteligheten til målingene var vi to forfattere under datainnsamlingen, som noterte ned den målte temperaturen i forskjellige skjemaer før vi sammenliknet temperaturene. I tillegg valgte vi å bruke den høyeste registrerte temperaturen for å sikre pålitelig temperatur.
For det andre var det vanskelig å være «anonyme» observatører. Vår synlighet under datainnsamlingen bør tas i betraktning når funnene tolkes. For det tredje er populasjonen liten, og dataene er kun samlet inn fra ett sykehus. Det reduserer generaliseringen av resultatene.
Til slutt er det en svakhet ved studien at forklart varians blant variablene i tabell 2 og 3 var på 8 og 11 prosent. Denne variansen er forholdsvis liten. Andre variabler som ikke er inkludert i studien, kan ha en større sammenheng med hypotermi.
Slike variabler kan være høyde, vekt, spesifikk diagnose eller inngrep, manglende varmetiltak eller type varmetiltak før, under og etter kirurgi. Det svekker validiteten til studien at disse variablene ikke ble registrert.
Konklusjon
Studien viser en høy forekomst av hypoterme pasienter, både ved ankomsten til postoperativ avdeling og én time etter ankomsten til postoperativ avdeling ved et sykehus i Norge. Spesielt utsatte grupper for lav kroppstemperatur var eldre pasienter og pasienter som hadde fått utført laparoskopisk kirurgi.
Resultatene bør føre til en mer systematisk måling av temperaturen og bedre varmetiltak til operasjonspasienten, både på anestesi- og operasjonsavdelingen.
For å sikre et godt pasientforløp på postoperativ avdeling bør systematisk temperaturkontroll innføres som en rutine på lik linje med andre vitale målinger, slik at hypoterme pasienter blir tidlig identifisert, får adekvate varmetiltak og dermed unngår komplikasjoner knyttet til hypotermi.
Vi vil rette en stor takk til pasientene som deltok i studien. Tusen takk til fagutviklingssykepleier Gunhild Bakkalia Bjørnå, som hjalp til med å veilede og tilrettelegge studien. Takk også til personalet ved den aktuelle anestesiavdelingen, operasjonsavdelingen og postoperative avdelingen.
Referanser
1. Wagner VD. Patient safety chiller: unplanned perioperative hypothermia. AORN J. 2010;92(5):567–71.
2. Leeth D, Mamaril M, Oman KS, Krumbach B. Normothermia and patient comfort: a comparative study in an outpatient surgery setting. J Perianesth Nurs. 2010;25(3):146–51.
3. Torossian A, Brauer A, Hocker J, Bein B, Wulf H, Horn EP. Preventing inadvertent perioperative hypothermia. Dtsch Arztebl Int. 2015;112(10):166–72.
4. Akers JL, Dupnick AC, Hillman EL, Bauer AG, Kinker LM, Wonder AH. Inadvertent perioperative hypothermia risks and postoperative complications: a retrospective study. AORN J. 2019;109(6):741–7.
5. Miyazaki R, Hoka S. What is the predictor of the intraoperative body temperature in abdominal surgery? J Anesth. 2019;33(1):67–73.
6. Lenhardt R. Body temperature regulation and anesthesia. Handb Clin Neurol. 2018;157:635–44.
7. de Brito Poveda V, Galvao CM, dos Santos CB. Factors associated to the development of hypothermia in the intraoperative period. Rev Lat Am Enfermagem. 2009;17(2):228–33.
8. Jacobs VR, Morrison JE jr., Mettler L, Mundhenke C, Jonat W. Measurement of CO(2) hypothermia during laparoscopy and pelviscopy: how cold it gets and how to prevent it. The Journal of the American Association of Gynecologic Laparoscopists. 1999;6(3):289–95.
9. National Institute for Health and Clinical Excellence. Clinical practice guideline. The management of inadvertent perioperative hypothermia in adults. London: National Institute for Health and Clinical Excellence; 2007. Tilgjengelig fra: https://www.nice.org.uk/guidance/cg65/update/CG65/documents/perioperative-hypothermia-inadvertent-guideline-guideline-for-consultation2 (nedlastet 14.01.2020).
10. AORN Recommended Practices Committee. Recommended practices for the prevention of unplanned perioperative hypothermia. AORN J. 2007;85:972–88.
11. Warttig S, Alderson P, Campbell G, Smith AF. Interventions for treating inadvertent postoperative hypothermia. Cochrane Database of Systematic Reviews. 2014;(11):CD009892.
12. Madrid E, Urrutia G, Roque i Figuls M, Pardo-Hernandez H, Campos JM, Paniagua P, et al. Active body surface warming systems for preventing complications caused by inadvertent perioperative hypothermia in adults. Cochrane Database of Systematic Reviews. 2016;4:CD009016.
13. Campbell G, Alderson P, Smith AF, Warttig S. Warming of intravenous and irrigation fluids for preventing inadvertent perioperative hypothermia. Cochrane Database of Systematic Reviews. 2015;(4):CD009891.
14. Karalapillai D, Story D, Hart GK, Bailey M, Pilcher D, Schneider A, et al. Postoperative hypothermia and patient outcomes after major elective non-cardiac surgery. Anaesthesia. 2013;68(6):605–11.
15. Salota V, Slovakova Z, Panes C, Nundlall A, Goonasekera C. Is postoperative tympanic membrane temperature measurement effective? Br J Nurs. 2016;25(9):490–3.
16. Bashaw MA. Guideline implementation: preventing hypothermia. AORN J. 2016;103:304–13.
17. Munday J, Delaforce A, Forbes G, Keogh S. Barriers and enablers to the implementation of perioperative hypothermia prevention practices from the perspectives of the multidisciplinary team: a qualitative study using the Theoretical Domains Framework. J Multidiscip Healthc. 2019;12:395–417.
18. Hegarty J, Walsh E, Burton A, Murphy S, O'Gorman F, McPolin G. Nurses' knowledge of inadvertent hypothermia. AORN J. 2009;89(4):701–4, 7–13.
19. Giuliano KK, Hendricks J. Inadvertent perioperative hypothermia: current nursing knowledge. AORN J. 2017;105(5):453–63.
20. Gasim GI, Musa IR, Abdien MT, Adam I. Accuracy of tympanic temperature measurement using an infrared tympanic membrane thermometer. BMC Res Notes. 2013;6:194.
21. Cheng H, Chen BP, Soleas IM, Ferko NC, Cameron CG, Hinoul P. Prolonged operative duration increases risk of surgical site infections: a systematic review. Surg Infect (Larchmt). 2017;18(6):722–35.
22. Doyle DJ, Garmon EH. American Society of Anesthesiologists Classification (ASA Class). Treasure Island, Florida: StatPearls Publishing; 2020.
23. Kleimeyer JP, Harris AHS, Sanford J, Maloney WJ, Kadry B, Bishop JA. Incidence and risk factors for postoperative hypothermia after orthopaedic surgery. J Am Acad Orthop Surg. 2018;26(24):e497–e503.
24. Karalapillai D, Story DA, Calzavacca P, Licari E, Liu YL, Hart GK. Inadvertent hypothermia and mortality in postoperative intensive care patients: retrospective audit of 5050 patients. Anaesthesia. 2009;64(9):968–72.
25. Horn EP, Bein B, Bohm R, Steinfath M, Sahili N, Hocker J. The effect of short time periods of pre-operative warming in the prevention of peri-operative hypothermia. Anaesthesia. 2012;67(6):612–7.
26. Kongsayreepong S, Chaibundit C, Chadpaibool J, Komoltri C, Suraseranivongse S, Suwannanonda P, et al. Predictor of core hypothermia and the surgical intensive care unit. Anesth Analg. 2003;96(3):826–33.
27. Mohanty S, Rosenthal RA, Russell MM, Neuman MD, Ko CY, Esnaola NF. Optimal perioperative management of the geriatric patient: a best practices guideline from the American College of Surgeons NSQIP and the American Geriatrics Society. J Am Coll Surg. 2016;222(5):930–47.
28. Su SF, Nieh HC. Efficacy of forced-air warming for preventing perioperative hypothermia and related complications in patients undergoing laparoscopic surgery: a randomized controlled trial. Int J Nurs Pract. 2018;24(5):e12660.
29. Torossian A, Van Gerven E, Geertsen K, Horn B, Van de Velde M, Raeder J. Active perioperative patient warming using a self-warming blanket (BARRIER EasyWarm) is superior to passive thermal insulation: a multinational, multicenter, randomized trial. Journal of Clinical Anesthesia. 2016;34:547–54.
30. Nierman DM. Tools that we use: if you can't measure it, you can't manage it. Critical Care Medicine. 2007;35(1):312–3.



















0 Kommentarer