Sammenhengen mellom depressive symptomer og egenbehandling (self-management) hos personer med diabetes 2
Sammendrag
Bakgrunn: Diabetes mellitus type 2 er den mest utbredte diabetestypen både i verden og i Norge. Personer med type 2-diabetes har en betydelig økt risiko for å utvikle depressive symptomer. Depresjon hos personer med diabetes er assosiert med negative konsekvenser, som økt risiko for komplikasjoner, redusert livskvalitet og i verste fall tidligere død.
Hensikt: Å kartlegge forekomsten av depressive symptomer hos personer med type 2-diabetes som var inkludert i en mobilhelseintervensjon. Vi ville også se på sammenhengen mellom depressive symptomer og egenbehandling (self-management).
Metode: Dette er en tverrsnittsstudie basert på baselinedata fra den norske randomiserte, kontrollerte studien i EU-prosjektet RENEWING HEALTH. I denne studien blir analysene basert på baselinedata ved inklusjon av deltakere i den norske delstudien, og deltakernes data analyseres som en gruppe (n = 151).
Resultat: Totalt 34/149 (22,5 prosent) av deltakerne hadde symptomer på depresjon (CES-D ≥ 16) ved inklusjon. Vi fant at de som rapporterte om depressive symptomer, skåret lavere på egenbehandling (målt med heiQ). Vi fant at de som er yngre, hadde en økt sannsynlighet for å rapportere om depressive symptomer (p = 0,042). Det var åtte ganger større sannsynlighet for at de som rapporterte om depressive symptomer, var utenfor arbeid sammenliknet med dem uten depressive symptomer.
Konklusjon: Om lag en femtedel av vårt utvalg av personer med diabetes type 2 rapporterte om depressive symptomer, og de som rapporterte om depressive symptomer, skåret lavere på egenbehandling.Nasjonale faglige retningslinjer for diabetes diskuterer hvorvidt personer med diabetes type 2 og depressive symptomer skal screenes for depressive symptomer for å kunne gi bedre helsetjenester til disse personene.
Referer til artikkelen
Rønning M, Holmen H, Ribu L. Sammenhengen mellom depressive symptomer og egenbehandling (self-management) hos personer med diabetes 2. Sykepleien Forskning. 2020;15(80751):e-80751. DOI: 10.4220/Sykepleienf.2020.80751
Diabetes er en kronisk sykdom med mange negative konsekvenser for den enkeltes liv og helse. Av alle med diabetes har om lag 90 prosent diabetes type 2 (1).
Det er anslått at det er om lag 424,9 millioner personer på verdensbasis som lever med diabetes, og at så mange som 212,4 millioner personer (50 prosent) av alle mellom 20 og 79 år er uvitende om at de har diabetes.
Stadig flere lever med diabetes også i Norge, hvor om lag 216 000 personer har en kjent diabetes type 2. I 2016 var det rundt 183 000 personer som brukte glukosesenkende medikamenter (2).
Sammenheng mellom diabetes og symptomer på depresjon
Samtidig er det vist en sammenheng mellom diabetes og symptomer på depresjon (3).
Personer med diabetes har en betydelig økt risiko for å utvikle depressive symptomer sammenliknet med dem uten diabetes (4), og det er vist at depresjon hos personer med diabetes kan ha en sammenheng med dårlig metabolsk kontroll (hyperglykemi) (3), høyere risiko for komplikasjoner (1,3), lavere arbeidsdeltakelse (5), redusert livskvalitet (4, 5) og tidligere død (6).
Disse funnene er spesielt alvorlige når vi vet at personer med type 2-diabetes og depresjon har høyere odds for arbeidsuførhet enn de med bare diabetes eller bare depresjon (7).
Depressive symptomer hos personer med diabetes kan i tillegg redusere evnen til egenbehandling (self-management) (3). Egenbehandling kan defineres som «individets evne til å kunne håndtere symptomer, livsstilsendringer og psykososiale og fysiske konsekvenser forbundet med å leve med en kronisk sykdom» (8).
Egenbehandling av diabetessykdommen og etterlevelse av anbefalt behandling er viktig for å fremme helse samt forebygge eller forsinke komplikasjoner i forbindelse med diabetessykdommen (1, 9).
Dersom behandleren ikke er oppmerksom på de psykososiale forholdene som er knyttet til sykdommen, kan det medføre en forverring i egenbehandlingen, da personer med depresjon kan ha behov for mer psykososial støtte enn de uten depresjon (10).
Personer med symptomer på depresjon bør screenes
Det blir derfor anbefalt å screene personer med symptomer på depresjon for psykososiale forhold ved blant annet å kartlegge personens holdninger til sykdommen, forventninger til behandling, behandlingseffekt, personens livskvalitet og tilgjengelige ressurser med selvrapporterte spørreskjemaer (9).
International Diabetes Federation (IDF) foreslår også at personer med diabetes skal screenes for depressive symptomer for å unngå økt antall sykehusinnleggelser og tidlig død, med noen enkle spørsmål om psykologiske forhold i et validert spørreskjema (11).
I Norge er det Nasjonal faglig retningslinje for diabetes som er styrende for behandlingen av personer med diabetes, og her vises det til manglende evidens for screening av depresjon hos dem med diabetes, og det anbefales derfor at det kun skal gjennomføres screening ved klinisk mistanke (12).
Hensikten med studien
Hensikten med denne studien var å kartlegge forekomsten av depressive symptomer hos personer med type 2-diabetes som var inkludert i en mobilhelseintervensjon. Vi ønsket også å se på blant annet sammenhengen mellom depressive symptomer og egenbehandling (self-management).
Forskningsspørsmålet var som følger: Hva er forekomsten av depressive symptomer i et gitt utvalg av personer med diabetes type 2, og hvilke sammenhenger er det mellom forekomsten av depressive symptomer og deltakernes sosiodemografiske og kliniske karakteristika og deres egenbehandling av sykdommen?
Metode
Studiens design
Studien vår er en tverrsnittsstudie basert på baselinedata fra den norske delstudien av EU-prosjektet RENEWING HEALTH. I den norske delstudien evaluerte vi en mobilapp med en diabetesdagbok hos personer med type 2-diabetes, med eller uten helseveiledning fra diabetessykepleier.
Vi gjennomførte en trearmet randomisert, kontrollert studie som er beskrevet i detalj tidligere (13–15). I denne studien ble resultatene utelukkende basert på baselinedata fra alle inkluderte i den norske delstudien, og vi analyserte deltakernes data som en gruppe (n = 151).
Deltakere og rekruttering
Inklusjonen av deltakere startet i mars 2011 og varte til oktober 2012. Deltakerne var hjemmeboende og ble rekruttert av sine fastleger fra både sørlige og nordlige deler av Norge.
Noen ble rekruttert fra frivillighetssentralene i kommunene, der de var henvist av sine fastleger for livsstilsendring. Det ble også rekruttert deltakere fra «Diabetes startkurs», som gjennomføres av spesialisthelsetjenesten, og som tilbys nydiagnostiserte hjemmeboende personer med diabetes i Norge (12).
Inklusjonskriteriene var ≥18 år, langtidsblodsukker (HbA1c) på nivå ≥7,1 prosent (54,1 mmol/mol) og å være diagnostisert med diabetes type 2 i mer enn tre måneder før studiestart.
Det var i tillegg viktig at deltakerne var i kognitiv stand til å kunne gjennomføre studien, og at de kunne bruke en mobiltelefon. Alvorlig fysisk eller psykisk sykdom var eksklusjonskriterier.
Før oppstart av prosjektet diskuterte vi om noen av deltakerne skulle få en sterkere intervensjon enn andre, blant annet de med depresjon eller depresjonssymptomer.
En tilpasning av intervensjonen basert på eventuelle depressive symptomer ville imidlertid kreve flere ressurser enn det vi hadde til rådighet, og denne tilpasningen ble derfor ikke innført i prosjektet.
Totalt ble 151 deltakere inkludert, og vi hentet inn data ved oppstart før deltakerne ble randomisert inn i én av de to intervensjonsgruppene eller i kontrollgruppen.
Prosedyre
Legene og andre impliserte i rekrutteringen fikk informasjon av oss på forhånd om de ulike kriteriene for å delta i studien. Vi hentet inn selvrapporterte data ved å bruke spørreskjema.
Noen kliniske variabler ble innhentet fra deltakernes fastlege. HbA1c ble enten innhentet fra deltakernes fastlege eller med et utlånt HbA1c-apparat som vi disponerte, for å sikre en så lik prosedyre som mulig.
Variablene som ble innhentet
I denne tverrsnittsstudien innhentet vi et mindre antall variabler fra hovedstudien, som tidligere er beskrevet i detalj (13–15).
Sosiodemografiske og kliniske variabler
De sosiodemografiske dataene ble innhentet fra de selvrapporterte spørreskjemaene utviklet i EU-prosjektet og omhandlet personlige opplysninger som alder, kjønn, sivilstand, utdanning, sivilstatus og arbeidsstatus.
Variabelen for arbeidsstatus ble konstruert som en dikotom variabel med dem som var i arbeid (inkludert pensjonister), og de som ikke var i arbeid. Noen kliniske variabler var selvrapporterte, slik som samtidige sykdommer (komorbiditet), hypoglykemi, diabetesvarighet og egenmåling av blodsukker.
De resterende kliniske karakteristikaene ble innhentet gjennom fastlegekontorene, deriblant: HbA1c, vekt, høyde, blodtrykk og medikasjon.
Livsstilsvariabler
Livsstilsvariabler som røyking og fysisk aktivitet ble innhentet gjennom selvrapporterte spørreskjemaer. Røyking ble benyttet som en dikotom variabel med spørsmål om man røyker tobakk daglig: ja eller nei.
Spørsmål om fysisk aktivitet ble innhentet og deretter konstruert som en dikotom variabel: fysisk aktiv eller inaktiv (13).
Depressive symptomer
For å måle depressive symptomer benyttet vi The Center for Epidemiological Studies Depression Scale (CES–D).
Dette verktøyet måler depressive symptomer i løpet av siste uke, og det er ikke et diagnoseverktøy (16). CES-D inneholder 20 spørsmål med svaralternativer som varierer fra 0 til 3 poeng der 0 = «Sjelden eller aldri», 1 = «En del eller litt av tiden», 2 = «En moderat del av tiden eller ganske ofte», og 3 = «Mesteparten eller hele tiden».
Skåren varierer fra 0 til 60, der høy skår indikerer mer depressive symptomer. Med en skår på <16 er det ingen tegn til depressive symptomer, og ≥16 viser til at det er en risiko for depressive symptomer.
Skjemaet er validert i USA og viser seg å være gyldig og pålitelig (16), men det er ikke validert i Norge, selv om det er et hyppig benyttet skjema.
I vår studie fant vi at reliabiliteten til CES-D målt med Cronbachs alfa hadde en tilfredsstillende indre konsistens med alfa = 0,77, selv om det er anbefalt en alfa over 0,8 (15).
Helsekompetanse og egenbehandling
The Health Education Impact Questionnaire (heiQ) er et spørreskjema for personer med kronisk sykdom med til sammen 40 spørsmål (17).
Disse spørsmålene måler personens helsekompetanse og egenbehandling (self-management). Det er et spørreskjema med åtte domener: «Positivt og aktivt engasjement i livet», «Helserettet atferd», «Tilegning av ferdigheter og teknikker», «Konstruktive holdninger og tilnærmingsmåter», «Egenovervåkning og innsikt», «Orientering i helsetjenesten», «Sosial integrasjon og støtte», og «Emosjonelt velvære».
Dette skjemaet har vist seg å være gyldig og pålitelig (17), og det er oversatt til norsk og psykometrisk testet i et norsk utvalg (18).
Etiske overveielser
Den randomiserte, kontrollerte studien med delstudier er tidligere godkjent av Regionale komiteer for medisinsk og helsefaglig forskningsetikk (REK) (referansenummer 2010/427).
Alle som ønsket å delta i undersøkelsen, fikk et informasjonsbrev med en kort oppsummering av prosjektet, og med en invitasjon til å få mer utdypende informasjon om deltakelse.
Mer detaljert informasjon ble deretter gitt både skriftlig og muntlig, og de som ønsket å delta, signerte et informert samtykkeskriv om å delta i studien (13).
Statistiske analyser
De statistiske analysene til denne studien ble gjennomført med analyseprogrammet SPSS, versjon 23. Vi har gjort eksplorerende undersøkelser for å se etter utfall. Vi valgte forklaringsvariabler ut fra tidligere forskning og erfaring på området.
De kategoriske sosiodemografiske og kliniske variablene og behandlings- og livsstilsvariablene blir presentert som antall (n) sammen med prosent (%).
Vi utførte alle analysene basert på tilgjengelige data, og vi har ikke benyttet imputering for manglende tall. De kontinuerlige sosiodemografiske og kliniske variablene og behandlings- og livsstilsvariablene er presentert som median med minimum- og maksimumsverdier (min–maks).
For å undersøke en statistisk signifikant sammenheng mellom den dikotome variabelen for depressive symptomer (CES-D < 16, CES-D ≥ 16) og de kategoriske sosiodemografiske og kliniske variablene samt behandlings- og livsstilsvariablene benyttet vi Pearsons kjikvadrattest.
Vi benyttet Mann-Whitney U-test for å se om det var en signifikant sammenheng mellom den dikotome variabelen for depressive symptomer (CES-D < 16, CES-D ≥ 16) og de kontinuerlige variablene.
Variablene fra de univariate og ujusterte analysene som viste en statistisk signifikant sammenheng med CES-D, ble tatt inn i logistiske regresjonsanalyser der vi justerte for alder, kjønn og hypoglykemi. Det valgte signifikansnivået var 5 prosent og tosidig.
Sammenhenger mellom komorbiditet og CES-D-skår ble imidlertid ikke analysert i vår delstudie da spørsmål om mental helse var inkludert i variablene som målte komorbiditet, noe som ville kunne korrelere med spørsmålene i CES-D.
Vi tok heller ikke med andre variabler som kunne korrelere med CES-D, og derfor utelot vi også «Positivt og aktivt engasjement i livet», «Helserettet atferd» og «Emosjonelt velvære» i heiQ fra analysene.
Resultater
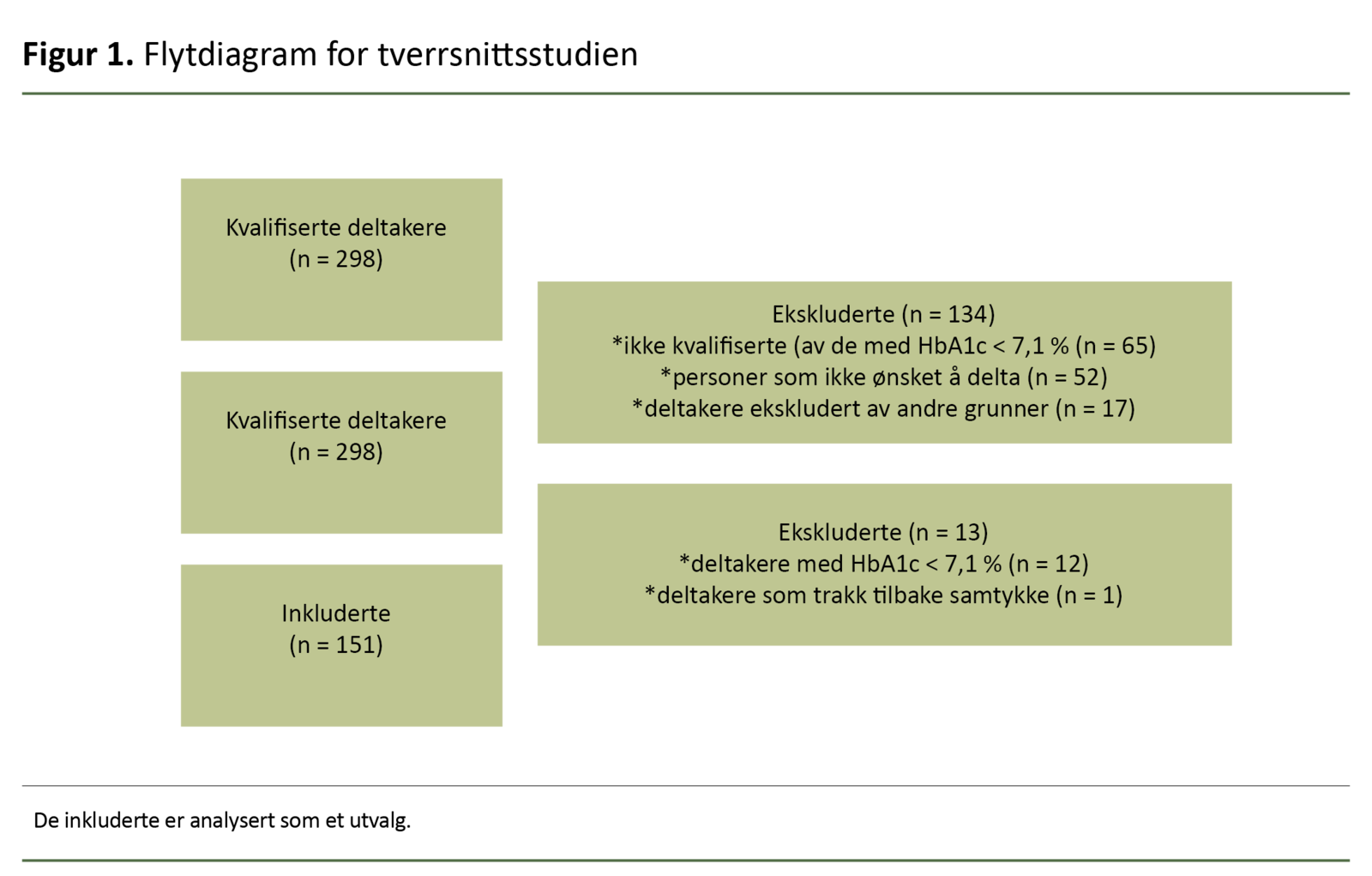
I hovedstudien var det totalt 298 personer som møtte inklusjonskriteriene, hvorav 65 ble ekskludert på grunn av HbA1c < 7,1 prosent, 52 ønsket ikke å delta, og 17 ble ekskludert av andre grunner (figur 1).
Inklusjonskriteriene er beskrevet i detalj tidligere (13). Det var totalt 151 deltakere med diabetes type 2 ved oppstart (13). Utvalget i hovedstudien ble randomisert i tre grupper, men i denne studien er de analysert som ett utvalg (n = 151).
Karakteristika ved utvalget
Median alder hos deltakerne var 58 år (min–maks = 20–80), og 62 av deltakerne (41,1 prosent) var kvinner.
Av deltakerne hadde 100 ≤ 12 år utdanning (66,2 prosent), 107 av deltakerne (70,9 prosent) var i arbeid, og 41 (27,2 prosent) bodde alene (tabell 1). Totalt 34/149 av deltakerne (22,5 prosent) hadde symptomer på depresjon (CES-D ≥ 16).

Median HbA1c hos deltakerne var 7,7 prosent (min–maks = 5,6–13,0) (tabell 2). Det var til sammen 9 av 131 deltakere (6,0 prosent) som ikke brukte glukosesenkende medikamenter, og 142 (94,0 prosent) målte blodsukkeret selv.
Median kroppsmasseindeks (KMI) var 30,9 kg/m² (min–maks = 19,9–52,6) og 98 av deltakerne (64,9 prosent) rapporterte at de var fysisk inaktive. Median diabetesvarighet var 9 år (min–maks = 1–36), og 97 av deltakerne (64,2 prosent) hadde en til to samtidige sykdommer (komorbiditet) i tillegg til diabetes type 2.
Vi fant ingen statistisk signifikant sammenheng mellom CES-D-skår og deltakerkarakteristika, bortsett fra arbeidsstatus (tabell 1) og hypoglykemi (tabell 2).

Ujusterte analyser
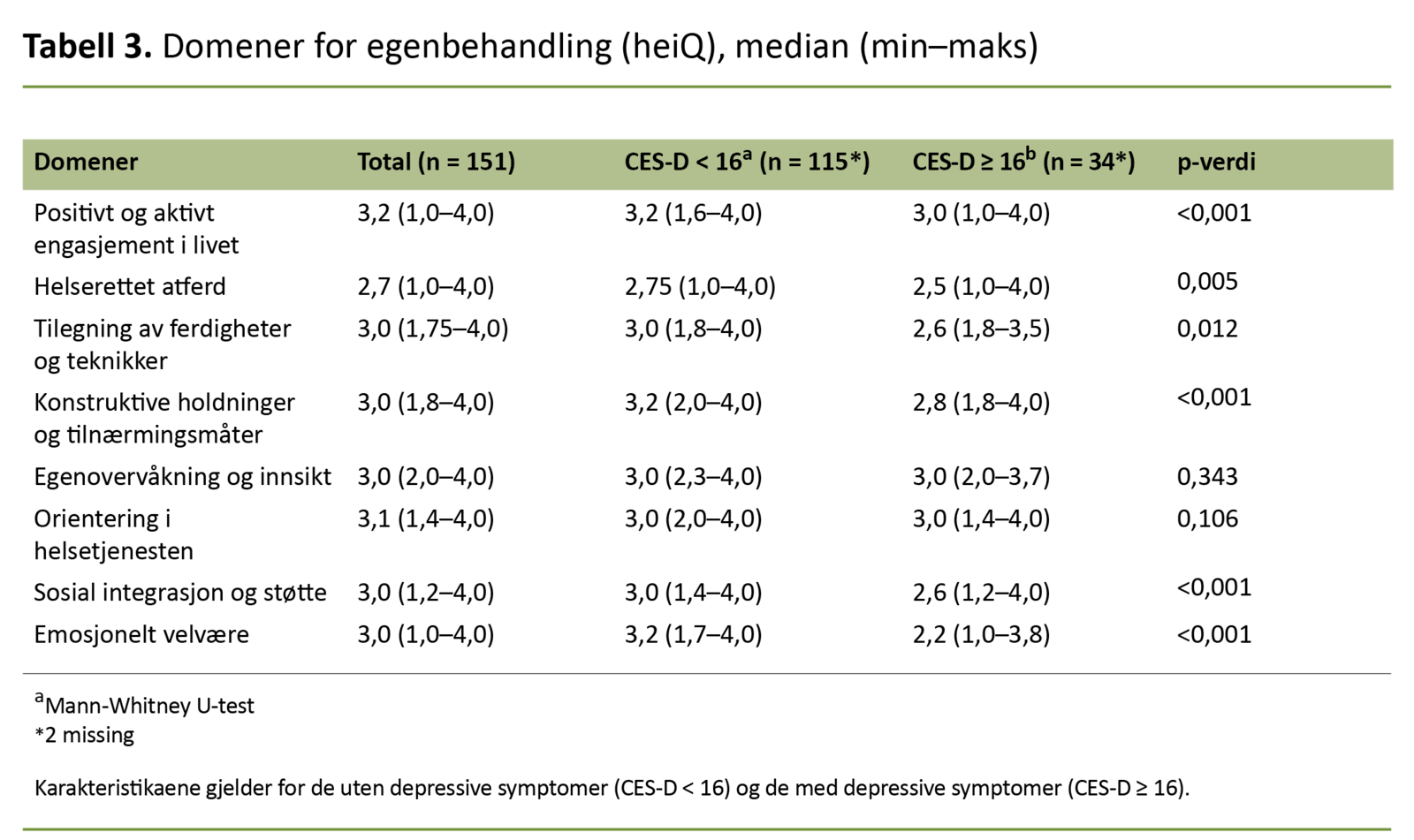
Tabell 3 viser egenbehandling (self-management) målt med heiQ og sammenhengen med rapporterte depressive symptomer (CES-D). Vi fant at de som rapporterte om depressive symptomer, skåret lavere på seks av åtte domener for egenbehandling målt med heiQ.
Justerte analyser
Logistisk regresjon viste at lavere alder hadde en sammenheng med en økt sannsynlighet for å rapportere om depressive symptomer sammenliknet med ikke-depressive symptomer (p = 0,042), justert for kjønn og hypoglykemi.
Videre fant vi at oddsen for å rapportere føling var høyere blant de som samtidig rapportere om depressive symptomer sammenliknet med dem uten depressive symptomer (p = 0,021), justert for alder og kjønn (tabell 4).
Lavere alder hadde en sammenheng med en økt sannsynlighet for å rapportere om depressive symptomer.
Analyser der vi så på deltakernes deltakelse i arbeidslivet, viste at oddsen var åtte ganger høyere for å være utenfor arbeid blant dem som rapporterte om depressive symptomer sammenliknet med dem uten depressive symptomer, justert for alder og kjønn.
Analyser av egenbehandling (heiQ) viste at blant de som rapporterte om depressive symptomer, var det 5 prosent økt sannsynlighet for å ha en lavere skår på «Konstruktive holdninger og tilnærmingsmåter» sammenliknet med dem uten depressive symptomer (p < 0,001).
Videre fant vi at de som rapporterte om depressive symptomer, hadde høyere odds for samtidig å rapportere om lavere skår på «Tilegning av ferdigheter og teknikker» og «Sosial integrasjon og støtte» – henholdsvis 19 prosent og 25 prosent.

Diskusjon
Vi fant at så mange som en femtedel av deltakerne (22,5 prosent) rapporterte om symptomer på depresjon (CES-D ≥ 16) da de ble inkludert i den norske delstudien. De med lavere alder i utvalget hadde større sannsynlighet for å rapportere om depressive symptomer.
De med lavere skår på heiQ-domenet «Sosial integrasjon og støtte» hadde større sannsynlighet for å rapportere om depressive symptomer sammenliknet med dem som ikke rapporterte om slike symptomer.
De som rapporterte om depressive symptomer, hadde også åtte ganger større sannsynlighet for å være utenfor arbeid.
Så mange som en femtedel av deltakerne rapporterte om symptomer på depresjon.
Videre viste det seg at det var økt sannsynlighet for en lavere skår på heiQ-domenet «Konstruktive holdninger og tilnærmingsmåter» i tillegg til lavere skår på «Tilegning av ferdigheter og teknikker» hos dem som rapporterte om depressive symptomer.
Det kom også frem at de som rapporterte at de opplevde hypoglykemi, hadde større sannsynlighet for å rapportere om depressive symptomer enn de uten slike symptomer.
En femtedel rapporterte om symptomer på depresjon
Vi fant at om lag en femtedel av deltakerne rapporterte om symptomer på depresjon.
Tidligere forskning i Norge på friske eldre med samme måleinstrument (CES-D) har imidlertid vist at mer enn hver femte person over 75 år har symptomer på depresjon, og at sammen med ensomhet opptrer dette symptomet hyppigere blant de yngste og eldste, sammenliknet med personer som er i mellomfasen i livet (19).
Dette funnet er i overensstemmelse med funnene i vår studie, der de med lavere alder hadde større sannsynlighet for å rapportere om depressive symptomer, sammenliknet med dem som ikke rapporterte om depressive symptomer.
The American Diabetes Association (ADA) anbefaler å screene alle eldre med diabetes (≥ 65 år) for både kognitiv svikt og depresjon (9), og de har tidligere listet opp en rekke mulige kartleggingsinstrumenter (20).
Tidligere forskning har også vist at yngre pasienter kan være mer åpne for å diskutere psykososiale behov enn pasienter over 65 år, men at mange pasienter ikke er oppmerksomme på at en konsultasjon også kan omhandle faktorer knyttet til psykososialt velvære (21).
Mangel på sosial integrasjon hadde sammenheng med depressive symptomer
En lavere skår på heiQ-domenet «Sosial integrasjon og støtte» viste seg i dette utvalget å være assosiert med en økt sannsynlighet for å rapportere om depressive symptomer.
Det er tidligere vist at mangel på sosial støtte kan være en risikofaktor for økt dødelighet, og at den sosiale støtten rundt personen bør tas like alvorlig som andre risikofaktorer, som blant annet røyking og høyt blodtrykk (22).
I vårt utvalg var det også åtte ganger større sannsynlighet for å være utenfor arbeid blant dem som rapporterte om depressive symptomer sammenliknet med dem som ikke rapporterte om depressive symptomer.
Det er tidligere vist at mangel på sosial støtte kan være en risikofaktor for økt dødelighet.
Nyere forskning viser til hvordan personer som står utenfor arbeidslivet, kan oppleve det som lettere om de får støtte, spesielt av noen som er i samme situasjon som dem selv. Forskning viser også at de som har et dårligere helsepotensial, har det vanskeligere enn dem som er friske (23).
Konstruktiv tenkning ga færre symptomer på depresjon
Videre fant vi at dersom deltakeren har høy skår på «Konstruktive holdninger og tilnærmingsmåter» i behandlingen av sin diabetes, er det mindre sannsynlig at vedkommende har symptomer på depresjon.
Det er også vist at personens holdning til behandlingen vil påvirke hvordan hun eller han følger opp sin egenbehandling (24). Det er imidlertid ikke bare pasientens holdninger til diabetesbehandlingen som er avgjørende for utfallet, men også helsepersonellets holdninger er viktige.
Tidsnød og mangel på tilgjengelig personell i helsevesenet kan også representere en barriere for å kunne utvikle og gjennomføre pasientundervisning, gode behandlingsplaner og medikamentell oppfølging (24).
I Norge er det kun 45 prosent av de med diabetes type 2 som når sine HbA1c-mål (25). Manglende oppnåelse av HbA1c-mål kan påvirkes av at mange pasienter med diabetes type 2 sliter med å følge behandlingsregimet (24, 25).
I studien vår fant vi ingen statistisk signifikant sammenheng mellom HbA1c og forekomst av symptomer på depresjon, og dette funnet samsvarer med tidligere forskning (26).
Kunnskap om ferdigheter og hjelpemidler beskytter
Våre funn viser imidlertid at en høy skår på «Tilegning av ferdigheter og teknikker» kan gjøre det mindre sannsynlig at personer med diabetes type 2 har symptomer på depresjon, noe som kan komme av at personen har god kunnskap om ferdigheter og hjelpemidler for å ivareta egen helse og behandling (17).
Ved hyperglykemi blir pasientene ofte satt på glukosesenkende behandling, noe som kan medføre økt risiko for hypoglykemi. De som rapporterte at de opplevde hypoglykemi i vår studie, hadde større sannsynlighet for å rapportere om depressive symptomer, som er i overensstemmelse med tidligere forskning (27).
Det å identifisere pasientens følelsesmessige bekymringer relatert til vedkommendes diabetes er derfor en viktig del av behandlingen til denne pasientgruppen (27).
Helsepersonell må være oppmerksomme på tegn til depresjon
Mens IDF foreslår at personer med diabetes skal screenes for komplikasjoner som depresjon (1, 11), anbefales ikke dette i Norge da det ikke er evidens for at en slik intervensjon har noen effekt (12).
I Nasjonal faglig retningslinje for diabetes foreslås det isteden å utrede for depresjon ved klinisk mistanke, med en presisering av at helsepersonell må være oppmerksomme på den økte forekomsten av depresjon hos personer med diabetes (12).
Symptomer på depresjon hos de med type 2-diabetes kan være like utbredt og kanskje mer enn alvorlig depresjon, og det er tidligere vist at de med symptomer på depresjon, ikke følges opp like tett som de med en depresjonsdiagnose (26).
Symptomer på depresjon hos de med type 2-diabetes kan være like utbredt og kanskje mer enn alvorlig depresjon.
I vår hovedstudie, der vi testet ut mobilteknologi i et randomisert, kontrollert forsøk, fant vi ikke effekt på det primære endepunktet HbA1c, og vi har tidligere diskutert en rekke mulige grunner til dette (13–15).
Depresjon kan være én grunn, og som følge av manglende egenbehandling kan deltakerne ha hatt behov for sterkere tiltak enn appen de fikk tildelt.
Forskning viser at screeningverktøy som pasientrapporterte utfallsmål (patient-reported outcome measures, PROM) også kan benyttes for å fremme kommunikasjonen mellom pasienten og helsepersonellet, slik at pasienten kan bli mer involvert i sin egen behandling (28).
Begrepet PRO (patient-reported outcome) inkluderer «enhver rapportering som kommer direkte fra pasienten om pasientens helsetilstand og status uten at det er gjort endringer eller tolkninger av en kliniker eller noen annen» (vår oversettelse) (29).
Forskning viser at bruken av PROM ikke medfører mer tid på den kliniske konsultasjonen (29), noe som er et viktig poeng da helsepersonell ofte har liten tid i klinikken (24).
Verktøy for screening av psykososiale forhold brukes allerede i Norge (30), og funnene i delstudien vår viser at det er behov for mer forskning om hvorvidt risikoutsatte personer med diabetes skal screenes for depresjon på samme måte som de kontrolleres for HbA1c ved jevnlige kontroller.
Styrker og svakheter ved studien
I denne studien benyttet vi spørreskjemaet heiQ, som gjennom sine spørsmål oppsummeres i åtte domener. Vi brukte ikke alle disse domenene da noen av disse, som for eksempel «Emosjonelt velvære», ville målt liknende fenomener som måles i CES-D.
Vi har av samme grunn ikke undersøkt sammenhengen mellom komorbiditet og CES-D siden mental helse ble undersøkt både i komorbiditet og i CES-D. Målene kunne derfor korrelere.
De tre utvalgte domenene fra heiQ i denne artikkelen illustrerer godt hvordan dårligere egenbehandling er assosiert med depressive symptomer.
Videre er det en begrensning at spørreskjemaet CES-D er validert internasjonalt (16), men ikke psykometrisk testet i Norge. Det vil derfor være knyttet noe usikkerhet til resultatene i denne studien.
På den annen side er antallet som rapporterer om depressive symptomer, i overensstemmelse med den norske studien av livsløp, aldring og generasjon (NorLAG), som benytter samme skjema (19).
En annen svakhet ved denne studien er at utvalget hadde meldt seg frivillig til å delta i en randomisert, kontrollert studie med det formålet å endre livsstil ved hjelp av en mobilapp for egenbehandling, og de rekrutterte personene kunne derfor være ekstra motiverte til å endre atferd, og som sådan ikke være representative for personer med type 2 diabetes.
Nå fant vi imidlertid at mange av deltakerne syntes det var krevende å endre livsstil (31), men metoden for rekruttering er uansett en begrensing i en studie som denne.
En annen metodisk begrensning er at undersøkelsen vår er eksplorerende, der vi ser om vi finner utfall. Funnene må bekreftes i videre forskning med et større utvalg, og eventuelt ved å bruke andre metoder.
Studien er en tverrsnittsstudie som ikke gjør det mulig å forklare årsak–virkning, og vår intensjon var kun å se på sammenhenger.
Konklusjon
Vi fant at en femtedel av deltakere med diabetes type 2 som deltok i en randomisert, kontrollert studie med en elektronisk diabetesdagbok for egenbehandling (self-management), rapporterte symptomer på depresjon da de ble inkludert i studien.
De av pasientene som rapporterte om depressive symptomer, skåret generelt lavere på egenbehandling (heiQ). Vi fant at de som er yngre, hadde større sannsynlighet for å rapportere om depressive symptomer.
De med depressive symptomer kan ha behov for mer støtte av sykepleiere og annet helsepersonell i behandlingen.
Det er derfor diskutert hvorvidt screening av depressive symptomer hos risikoutsatte personer er hensiktsmessig, både i Norge og internasjonalt. Denne problemstillingen er aktuell både i forskning og klinisk praksis.
Referanser
1. International Diabetes Federation. International Diabetes Federation Diabetes Atlas; 2017. 8. utg. Tilgjengelig fra: http://www.diabetesatlas.org/ (nedlastet 14.08.2018).
2. Stene LC, Strøm H, Gulseth HL. Diabetes i Norge. Oslo: Folkehelseinstituttet; 2014. Tilgjengelig fra: https://www.fhi.no/nettpub/hin/helse-og-sykdom/diabetes-i-norge---folkehelserappor/ (nedlastet 14.08.2018).
3. Holt R, de Groot M, Golden S. Diabetes and depression. Current Diabetes Reports. 2014;14(6):1–9.
4. Rotella F, Mannucci E. Diabetes mellitus as a risk factor for depression. A meta-analysis of longitudinal studies. Diabetes Research and Clinical Practice. 2013;99(2):98–104.
5. Egede LE. Diabetes, major depression, and functional disability among U.S. adults. Diabetes Care. 2004;27:421–8.
6. Park M, Katon WJ, Wolf FM. Depression and risk of mortality in individuals with diabetes: a meta-analysis and systematic review. General Hospital Psychiatry. 2013;35(3):217–25.
7. Nouwen A, Winkley K, Twisk J, Lloyd C, Peyrot M, Ismail K, et al. Type 2 diabetes mellitus as a risk factor for the onset of depression: a systematic review and meta-analysis. Clinical and Experimental Diabetes and Metabolism. 2010;53(12):2480–6.
8. Barlow J, Wright C, Sheasby J, Turner A, Hainsworth J. Self-management approaches for people with chronic conditions: a review. Patient Education and Counseling. 2002;48(2):177–87.
9. American Diabetes Association. 5. Lifestyle management. Standards of medical care in diabetes 2019. Diabetes Care. 2019;42(Suppl. 1):S46–60. DOI: 10.2337/dc19-S005
10. Richards D, Chellingsworth M, Hope R, Turpin G, Whyte M. Reach out: national programme supervisor materials to support the delivery of training for psychological wellbeing practitioners delivering low intensity interventions 2010. Tilgjengelig fra: http://www.babcp.com/files/Accreditation/PWP/IAPT-PWP-Supervision-Manual-Reach-Out.pdf (nedlastet 14.08.2018).
11. International Diabetes Federation. Recommendations For Managing Type 2 Diabetes In Primary Care. Brussel; 2017. Tilgjengelig fra: www.idf.org/managing-type2-diabetes (nedlastet 14.08.2018).
12. Helsedirektoratet. Nasjonal faglig retningslinje for diabetes. Oslo; 2017. Tilgjengelig fra: https://helsedirektoratet.no/retningslinjer/diabetes (nedlastet 14.08.2018).
13. Torbjørnsen A, Jenum AK, Småstuen MC, Årsand E, Holmen H, Wahl AK, Ribu L. A low-intensity mobile health intervention with and without health counseling for persons with type 2 diabetes, part 1: baseline and short-term results from a randomized controlled trial in the Norwegian part of RENEWING HEALTH. JMIR mHealth and uHealth. 2014;2(4):e52.
14. Holmen H, Torbjørnsen A, Wahl AK, Jenum AK, Småstuen MC, Årsand E, Ribu L. A mobile health intervention for self-management and lifestyle change for persons with type 2 diabetes, part 2: one-year results from the Norwegian randomized controlled trial RENEWING HEALTH. JMIR mHealth and uHealth. 2014;2(4):e57.
15. Holmen H. Mobile health for diabetes self-management. (Doktoravhandling.) Oslo: Universitetet i Oslo, Medisinsk fakultet; 2017.
16. Radloff LS. The CES-D scale: a self-report depression scale for research in the general population. Applied Psychological Measurement. 1977 juni;1(3):385–401.
17. Osborne RH, Elsworth GR, Whitfield K. The Health Education Impact Questionnaire (heiQ): An outcomes and evaluation measure for patient education and self-management interventions for people with chronic conditions. Patient Education and Counseling. 2007;66(2):192–201.
18. Wahl AK, Osborne RH, Langeland E, Wentzel-Larsen T, Mengshoel AM, Ribu L, et al. Making robust decisions about the impact of health education programs: Psychometric evaluation of the Health Education Impact Questionnaire (heiQ) in diverse patient groups in Norway. Patient Education and Counseling. 2016;99(10):1733.
19. Hansen T, Daatland SO. Aldring, mestringsbetingelser og livskvalitet. Oslo: Helsedirektoratet; 2016.
20. Young-Hyman D, de Groot M, Hill-Briggs F, Gonzalez JS, Hood K, Peyrot M. Psychosocial care for people with diabetes: A position statement of the American Diabetes Association. Diabetes Care. 2016;39(12), 2126–40.
21. van Dijk-de Vries A, van Bokhoven MA, de Jong S, Metsemakers JFM, Verhaak PFM, van Der Weijden T, et al. Patients’ readiness to receive psychosocial care during nurse-led routine diabetes consultations in primary care: a mixed methods study. International Journal of Nursing Studies. 2016;63:58–64.
22. Holt-Lunstad J, Smith TB, Layton JB, Brayne C. Social relationships and mortality risk: a meta-analytic review (social relationships and mortality). PLoS Medicine. 2010;7(7):e1000316.
23. Heggebø K, Elstad JI. Is it easier to be unemployed when the experience is more widely shared? Effects of unemployment on self-rated health in 25 European countries with diverging macroeconomic conditions. European Sociological Review. 2018;34(1):22–39.
24. Nam S, Chesla C, Stotts NA, Kroon L, Janson SL. Barriers to diabetes management: Patient and provider factors. Diabetes Research and Clinical Practice. 2011;93(1):1–9.
25. Mouland G. Diabetes i en fastlegepraksis – ble behandlingsmålene nådd? Tidsskrift for Den norske legeforening. 2014;134(2):168–72.
26. Golden SH, Shah N, Naqibuddin M, Payne JL, Hill-Briggs F, Wand GS, et al. The prevalence and specificity of depression diagnosis in a clinic-based population of adults with type 2 diabetes mellitus. Psychosomatics. 2017;58(1):28–37.
27. Pearce MJ, Pereira K, Davis E. The psychological impact of diabetes: a practical guide for the nurse practitioner. Journal of the American Association of Nurse Practitioners. 2013;25(11):578–83.
28. Snyder CF, Aaronson NK, Choucair AK, Elliott TE, Greenhalgh J, Halyard MY, et al. Implementing patient-reported outcomes assessment in clinical practice: a review of the options and considerations. Quality of Life Research. 2012;21(8):1305–14.
29. Santana MJ, Haverman L, Absolom K, Takeuchi E, Feeny D, Grootenhuis M, et al. Training clinicians in how to use patient-reported outcome measures in routine clinical practice. Quality of Life Research. 2015;24(7):1707–18.
30. Hernar I. Bruk av pasientrapporterte målinger for å bedre kvaliteten på oppfølgingen av personer med diabetes – en feasibility studie. Bergen: Helse Bergen HF, Haukeland universitetssjukehus; 2017. Tilgjengelig fra: https://helseforskning.etikkom.no/prosjekterirek/prosjektregister/prosjekt?p_document_id=796318&p_parent_id=802344&_ikbLanguageCode=us (nedlastet 14.08.2018).
31. Ribu L, Rønnevig M, Corbin J. People with type 2 diabetes struggling for self-management: A part study from the randomised controlled trial in RENEWING HEALTH. Nursing Open. 23.05.2019;1–9.



















0 Kommentarer