Er det likegyldig hvem som sponser klinisk forskning?

Kliniske studier som sponses av farmasøytisk industri, har trolig mer fordelaktige funn og konklusjoner enn studier som ikke sponses av farmasøytisk industri.
Det viser en Cochrane-oversikt.
Hva sier forskningen?
I systematiske oversikter samles forskning. I denne systematiske oversikten har forfatterne samlet forskning om sammenhengen mellom sponsing fra farmasøytisk industri og resultater i kliniske studier. Kliniske studier helt eller delvis sponset at farmasøytisk industri, ble sammenliknet med kliniske studier som ble finansiert fra andre kilder.
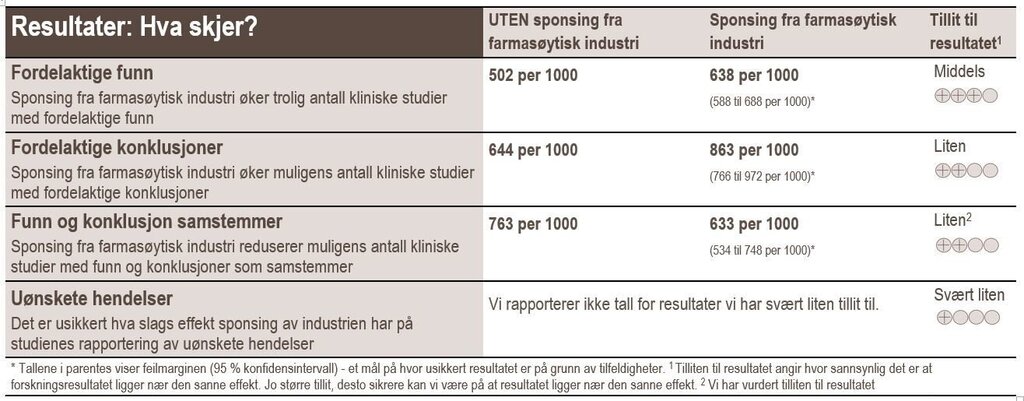
Resultatene viser at sponsing fra farmasøytisk industri
- trolig øker antall kliniske studier med fordelaktige funn (middels tillit til resultatet)
- muligens øker antall kliniske studier med fordelaktige konklusjoner (liten tillit til resultatet)
- muligens reduserer antall kliniske studier med funn og konklusjoner som samstemmer (liten tillit til resultatet)
Hvorvidt det er en sammenheng mellom sponsing fra farmasøytisk industri og rapportering av uønskete hendelser, er usikkert.
Bakgrunn
Resultater fra kliniske studier på legemidler og medisinske metoder (medical devices) påvirker medisinsk praksis og dermed behandlingsalternativene som pasienter tilbys. Klinisk forskning er i stadig større grad sponset av selskaper som lager produktene, enten fordi selskapene selv utfører studier eller helt eller delvis betaler andre for å utføre dem. Selskapene kan tenkes å påvirke studieresultater ved å påvirke eller bestemme
- spørsmålsformulering
- studiedesign
- utførelse av studien
- hvordan data analyseres
- selektiv rapportering av fordelaktige funn
Flere og flere forskningstidsskrifter krever at studier som publiseres, beskriver rollen til sponsoren(e). De fleste seriøse tidsskrifter krever også at studiens publiserte protokoll skal vedlegges når en studie vurderes for publisering. En slik protokoll skal være registrert i en database (som for eksempel clinicaltrials.gov), og den skal være publisert før studien igangsettes. Den bør som et minimum inneholde en god beskrivelse av populasjonen, tiltaket, sammenlikningen, utfallene og studiedesignet, slik at det blir mulig å vurdere eventuelle feil eller skjevheter i rapporteringen av studieresultatene.
Hva er denne informasjonen basert på?
Forfatterne av Cochrane-oversikten gjorde systematiske søk i aktuelle forskningsdatabaser i februar 2015 og inkluderte til sammen 75 publikasjoner. 57 omhandlet legemidler, 3 medisinsk utstyr/metode, 2 studier omhandlet både legemidler og medisinsk metode/utstyr og 13 inkluderte forskjellige typer tiltak (som legemidler, metoder/utstyr, atferdstiltak). 58 publikasjoner inkluderte kun kliniske studier, 2 kun observasjonsstudier og 15 både og. Antall inkluderte studier per publikasjon var 105 (median, med spennvidde fra 9 til 930).
Forfatterne analyserte også sammenhengen mellom studiekvalitet (fare for systematiske feil) og hvem som sponset de kliniske studiene. De fant ingen vesentlige forskjeller, bortsett fra at industri-sponsete studier kom noe bedre ut når det gjaldt bruk av blinding, det vil si at de som deltar i studien, ikke vet om de får aktivt medikament eller placebo. Disse funnene er ikke kritisk vurdert og bør derfor tolkes med forsiktighet.
Referanse
Lundh A, Lexchin J, Mintzes B, Schroll JB, Bero L. Industry sponsorship and research outcome. Cochrane Database of Systematic Reviews 2017, Issue 2. Art. No.: MR000033. DOI: 10.1002/14651858.MR000033.pub3.
Les hele oversikten i Cochrane Library: Industry sponsorship and research outcome






















0 Kommentarer