Stell og bruk av sentralt venekateter i intensivavdeling
Studien tyder på at praksis for stell og bruk av sentralt venekateter spriker, og i for liten grad er kunnskapsbasert.
Bakgrunn: Intensivpasienter med sentralt venekateter (SVK) er utsatt for å få mikroorganismer i blodbanen ved daglig stell og bruk av SVK. Blodbaneinfeksjoner kan gi forlenget opphold i intensivavdeling, med påfølgende økt mortalitet. Med de personlige belastninger og samfunnsmessige kostnadene dette kan gi, er det et område som bør kvalitetssikres.
Hensikt: Studien har til hensikt å kartlegge intensivsykepleiers praksis tilknyttet stell og bruk av SVK, med vekt på forebygging av blodbaneinfeksjoner. Selvrapportert praksis vil sammenliknes med Center for Disease Control’s (CDC) Guidelines for the Prevention of Intravascular Catheter-Related Infections.
Metode: En kvantitativ tverrsnitt studie med deskriptivt design ble benyttet. Data ble innsamlet ved hjelp av et strukturert spørreskjema som ble sendt ut til 390 sykepleiere ved seks intensivavdelinger i Norge. Svarresponsen ble 52,4 prosent.
Resultat: Det var to områder som i stor grad viste seg å være i tråd med CDC’s retningslinje; frekvens på bytte av infusjonssett ved kontinuerlig infusjon av parenteral ernæring og type bandasje som benyttes på SVK’s innstikkssted. Utover dette viste selvrapportert praksis seg å være sprikende.
Konklusjon: Studien viste at praksis tilknyttet stell og bruk av SVK er uensartet og i varierende grad i tråd med CDC’s retningslinje.
Innledning
Sentralt venekateter (SVK) er nødvendig for hemodynamisk monitorering, tilgang for medikamenter, væsker og ernæring hos kritisk syke pasienter i intensivavdeling. Ved innsetting av SVK blir hudens naturlige barriere mot mikroorganismer brutt og det gir en økt risiko for infeksjon. Blodbaneinfeksjoner påført via SVK utgjør en stor andel av sykehusinfeksjoner (1). En rapport utarbeidet av helsemyndighetene i USA viste at antall infeksjoner i intensivavdelinger lå mellom 1,6 til 6,8 per 1000 kateterdager (2). Videre fant en belgisk studie et gjennomsnitt på 5,3 infeksjoner per 1000 kateterdager i intensivavdeling (3). SVK-blodbaneinfeksjon kan føre til forlenget intensivopphold, økt mortalitet og økte kostnader for helsetjenesten (3–7).
I Norge finnes det, ifølge Pasientsikkerhetsprogrammet, ikke statistikk på antall blodbaneinfeksjoner tilknyttet SVK. Det betyr at vi ikke har noe å måle vår praksis opp mot. Pasientsikkerhetsprogrammet «I trygge hender» har forebygging av infeksjon ved SVK, som ett av sine satsingsområder. Forskning har vist at ved å innføre de tiltak som Pasientsikkerhetsprogrammet jobber for, kan antall infeksjoner reduseres betydelig (6–8).
Internasjonalt er det utført flere studier i forhold til intensivsykepleiers kunnskap og praksis tilknyttet stell og bruk av SVK (9–12). En europeisk studie samlet inn 3405 spørreskjemaer fra 26 europeiske land, hvorav 16 skjemaer var fra norske respondenter (9). Resultat fra denne studien samt andre studier viste at kunnskap eller praksis var mangelfull, og at det er viktig å fokusere på å forebygge infeksjon ved daglig stell og bruk av SVK (8–12). Ved å kvalitetssikre hele forløpet fra innleggelse av SVK til det seponeres, kan man redusere antall blodbaneinfeksjoner ned mot 0 per 1000 kateterdager (8,13).
Denne studien hadde til hensikt å kartlegge dagens praksis tilknyttet stell og bruk av SVK i intensivavdelinger i Norge, med vekt på å forebygge blodbaneinfeksjoner. Studien vil kunne gi økt oppmerksomhet rundt sykepleiers rutiner ved stell og bruk av SVK, samt at resultatene fra studien vil kunne bidra til økt vektlegging av kunnskapsbasert praksis. Det er tidligere ikke utført noe studie i Norge for å kartlegge intensivsykepleiers praksis tilknyttet SVK.
Metode
Design
En kvantitativ tverrsnittstudie med deskriptiv design ble benyttet. En tverrsnittstudie er godt egnet for å beskrive praksis med ulike variabler innen et begrenset tidsrom og vise sammenhenger mellom ulike variabler (14).
Utvalg
Sju intensivavdelinger ble kontaktet per telefon og seks av disse var villige til å delta. Ved de seks intensivavdelingene var det totalt 390 sykepleiere som mottok spørreskjema.
Spørreskjema
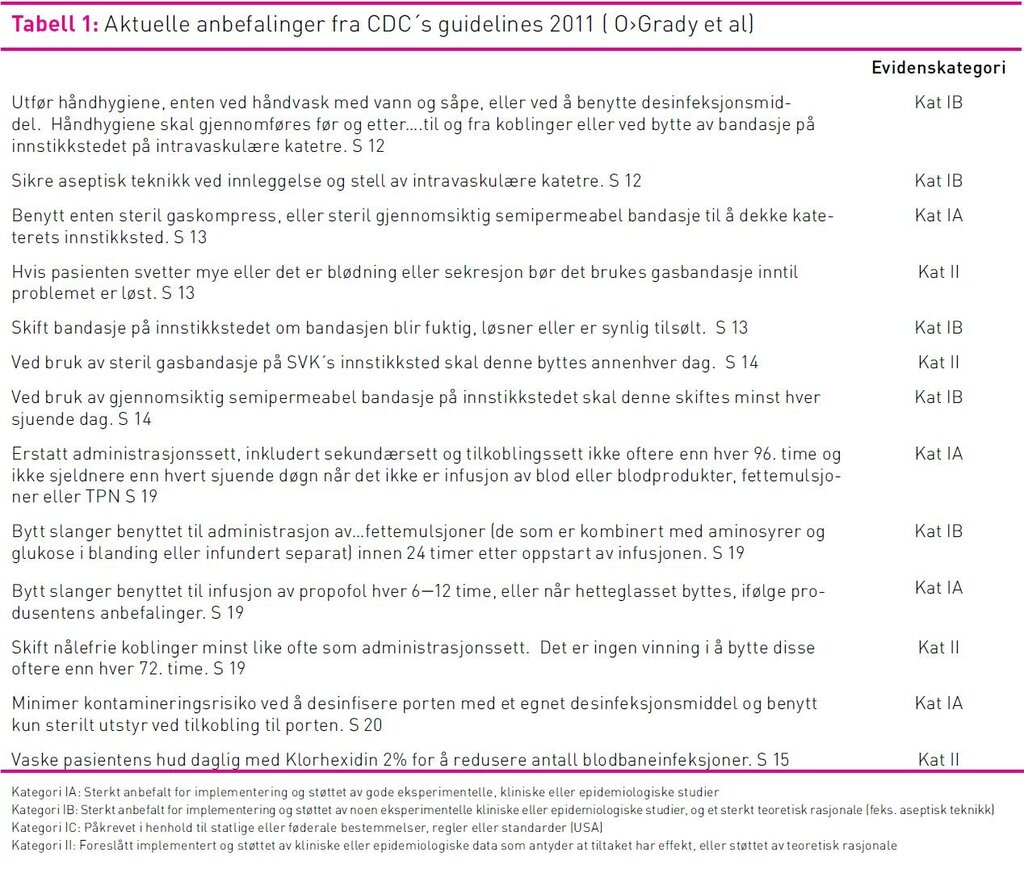
Ingen validerte spørreskjemaer som passet til å kartlegge intensivsykepleiers praksis tilknyttet stell og bruk av SVK ble funnet. Det ble derfor utviklet et strukturert spørreskjema med utgangspunkt i CDC’s «Guidelines for The Prevention of Intravascular Catheter-Related Infections, 2011» (4). Ved utvikling av spørreskjemaer er det nyttig å se på relevante skjemaer som er benyttet tidligere. Ved å bruke spørsmål som er benyttet i tidligere studier, vil man ha mulighet til å sammenlikne sine resultater med tidligere funn (15). I spørreskjemaet ble det stilt spørsmål som var relevante for norske forhold. For eksempel ble det ikke stilt noe spørsmål om man vasket pasienten daglig med Klorhexidin 2 prosent for å redusere bakteriefloraen på pasientens hud, fordi Klorhexidin 2 prosent ikke er tilgjengelig i Norge. I innledningen av spørreskjemaet ble det presisert at respondenten skulle besvare alle spørsmål ut fra en normal situasjon og ikke en akutt situasjon. Spørreskjemaet inneholdt spørsmål om håndhygiene, aseptisk teknikk, hyppighet av SVK-stell og frekvens på bytte av infusjonssett i forhold til forskjellige typer kontinuerlige infusjoner. En likertskala fra 1–5 ble brukt for de fleste spørsmål: 1=alltid, 2=som oftest, 3=av og til, 4=sjelden, 5=aldri. Når det gjaldt hyppighet av SVK-stell i form av at det skiftes helt inn til kateterkoblingen var svaralternativene: 1=daglig, 2=hver andre dag, 3=hver tredje dag, 4=hver fjerde dag, 5=hver sjuende dag og 6=annet. Demografiske eller bakgrunnsspørsmålene omfattet alder, kjønn, utdannelse, års erfaring fra intensivavdeling, stillingsbrøk og arbeidsplass. Spørsmål i et spørreskjema skal være lett forståelige og det bør ikke være rom for misforståelser. Et spørreskjema bør testes ut av noen som er i samme målgruppe som de spørreskjemaet er laget for (14,15). Spørreskjemaet ble gjennomgått av fem intensivsykepleiere. Hver enkelt sykepleier leste gjennom spørreskjemaet og svarte på spørsmålene. Forfatter stilte deretter spørsmål om forståeligheten av spørsmålene og om det var noe som kunne misforstås. Etter tilbakemeldinger ble enkelte spørsmål endret for å kvalitetssikre skjemaet. Aktuelle anbefalinger fra CDC’s guidelines 2011 er vist i tabell 1.
Datainnsamling
Spørreskjemaene ble sendt ut via nettskjemadatabasen ved universitetets senter for informasjonsteknologi (USIT) i Oslo høsten 2012. Kun 59 sykepleiere returnerte skjema via USIT, samt at flere rapporterte at de hadde vanskeligheter med å logge seg inn på nettskjemaet. For å unngå vanskelighetene med nettskjema og i et forsøk på å øke responsraten, besluttet vi å konvertere til papirskjema. For å sikre at alle fikk papirskjema med frankerte returkonvolutter, leverte vi disse personlig ved alle seks intensivavdelinger. Siden de innkomne nettskjemaene ikke kunne knyttes til respondentene, ble det ved utlevering av papirskjema presisert at de som hadde sendt inn nettskjema ikke skulle fylle ut papirskjema. Det ble sendt ut to påminnelser i løpet av datainnsamlingsperioden på to måneder. Det kom inn 145 papirskjema, totalt 204 besvarelser som gir en svarrespons på 52,4 prosent.
Analyse
For analyse brukte vi IBM SPSS, versjon 20. Dataene ble lagt inn i SPSS manuelt og sjekket for tastefeil to ganger. Vi utførte deskriptiv analyse med frekvens og prosentandeler for kartlegging av selvrapportert praksis. Krysstabeller med kjikvadrat test ble benyttet for å teste forskjeller mellom grupper på dikotome data, som kjønn, spesialutdanning og type sykehus. Alder ble også gjort om til dikotom variabel, ved å skille over og under 45 år. Resultatene av kontinuerlige variabler blir presentert i gjennomsnitt og standard avvik. Dikotome variabler blir presentert i antall og prosent. Statistisk signifikansnivå ble satt til p = 0,05.
Manglende data
Det var lite manglende data i materialet (<10 prosent). I det demografiske materialet var det seks som ikke oppga alder og tre som ikke oppga stillingsprosent.
Etiske hensyn
Denne studien faller utenfor helseforskningslovens virkeområde fordi man ikke skulle innhente personlige data. Tillatelse ble innhentet hos Norsk samfunnsvitenskapelig datatjeneste. Dette var nødvendig fordi e-postadresser til ansatte ved de aktuelle intensivavdelinger skulle innhentes. E-postadressene var ikke mulig å koble til de besvarte spørreskjemaene. Dette ble ivaretatt av USIT. Når det gjaldt papirskjemaene var disse uten id-nummer og ikke sporbare. Ved utsendelse av spørreskjema, sendte vi med et informasjonsbrev om studien. Her ble det presisert at undersøkelsen var helt anonym og at samtykke ble ansett som innhentet ved retur av utfylt spørreskjema.
Resultater
Svarresponsen varierte fra 38 prosent til 73 prosent ved de seks intensivavdelingene og ble totalt 52,4 prosent. Det var ingen signifikant forskjell i svarrespons ut fra om man jobbet på universitetssykehus eller lokal/regional sykehus. Av respondentene var nesten alle (93 prosent) intensivsykepleiere og de fleste jobbet full stilling. Ytterligere informasjon om demografiske/bakgrunnsdata finnes i tabell 2.
Håndhygiene, aseptisk teknikk
Studien viste at 34 prosent «alltid» utfører håndhygiene før de skal koble til en infusjon eller gi et medikament med en sprøyte i SVK. Når spørsmålet om håndhygiene ble stilt i sammenheng med teknikker som benyttes for å jobbe aseptisk, var det 54 prosent som oppga at de har rene hender når de skal koble til en infusjon. Nærmere 88 prosent av respondentene oppga at man vektlegger aseptisk teknikk i avdelingen, men bare 37,7 prosent oppga å benytte aseptisk non-touch teknikk ved manipulering av koblinger på SVK. Ved manipulering av koblinger og treveiskraner på SVK, oppga 46,8 prosent at de bruker en kompress med Klorhexidinsprit og 22 prosent oppga å bruke kompress med desinfeksjonssprit 70 prosent. Det var signifikant flere i aldersgruppen over 45 år (62 prosent) som benyttet kompress med Klorhexidinsprit enn de under 45 år (33 prosent). På spørsmål om man setter på ny steril propp etter å ha koblet fra en infusjon eller gitt et medikament i SVK, svarte 70 prosent «alltid». En av avdelingene brukte toveiskopling og der var propp uaktuelt, den gruppen utgjorde 8,8 prosent av respondentene.
Hyppighet av SVK-stell
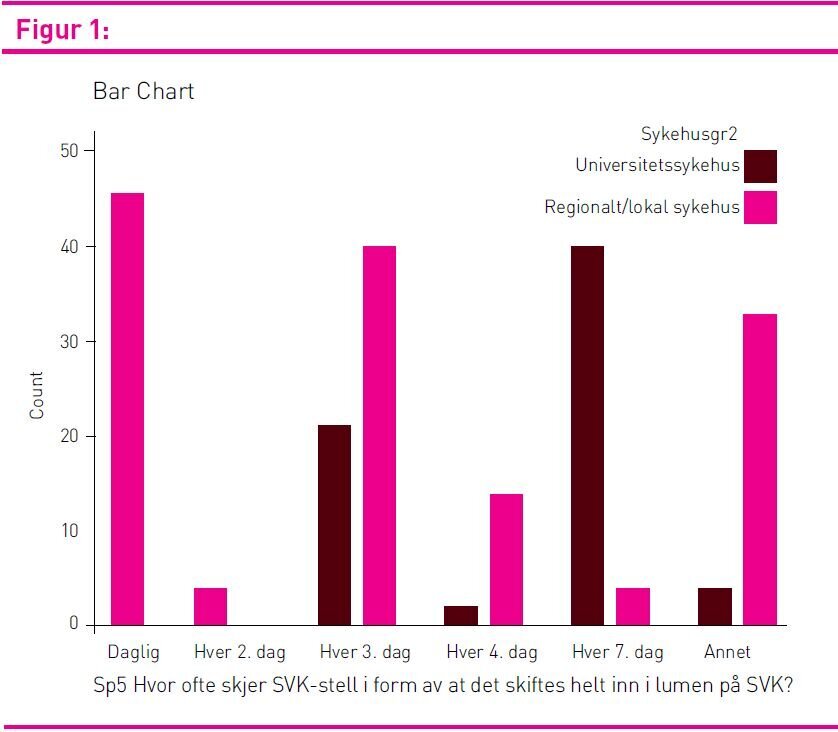
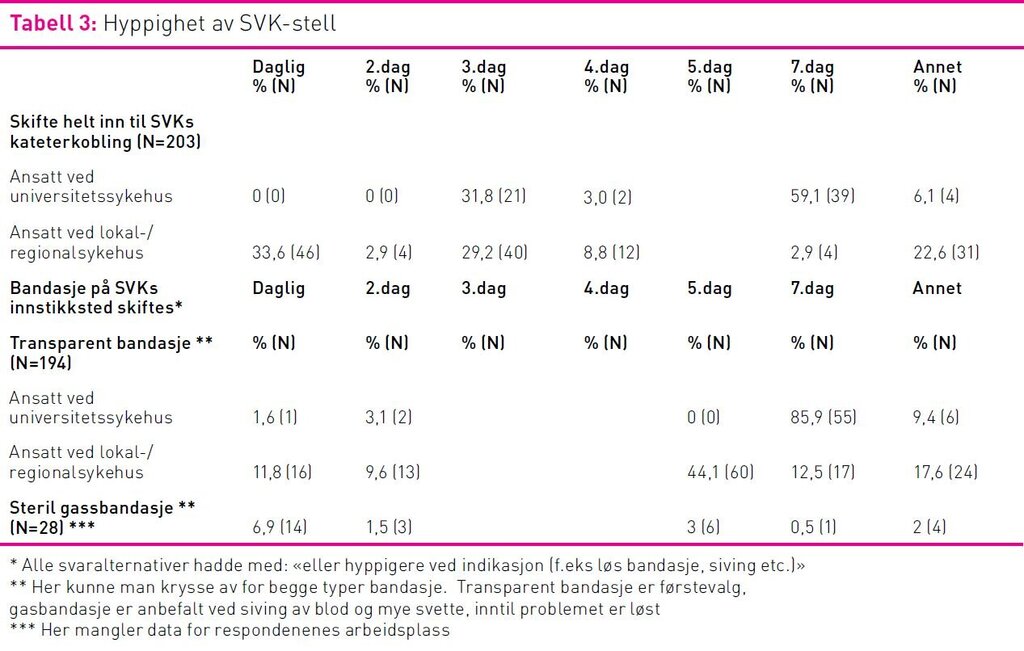
Det var stor spredning i praksis i forhold til hvor ofte SVK-stell blir gjennomført i form av å skifte helt inn til kateterkoblingen, fra daglig til hver sjuende dag. Ved universitetssykehusene var det 32 prosent som skiftet hver tredje dag og nær 60 prosent som oppga å skifte helt inn hver sjuende dag, mens de som jobbet ved lokal- eller regionsykehus hadde en større spredning i sin praksis (p < 0,05), se figur 1.
86 prosent av de ansatte ved universitetssykehusene oppga at bandasje på SVK-innstikkssted ble skiftet hver sjuende dag eller tidligere ved indikasjon. Svarene fra ansatte ved lokal- eller regionsykehusene viste derimot en større spredning i praksis (p < 0,05). For ytterligere info, se tabell 3.
Bytte av infusjonssett ved kontinuerlig infusjon
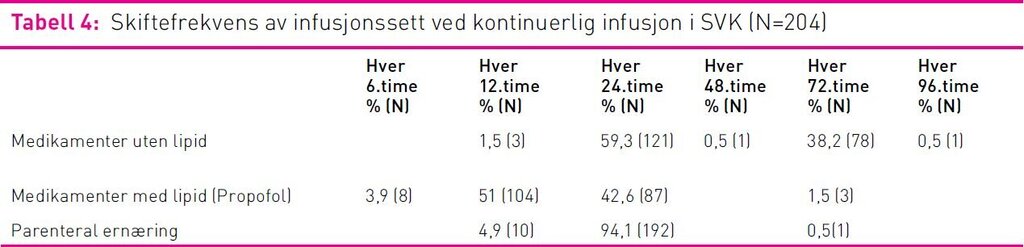
Praksis ved bytte av infusjonssett ved kontinuerlig infusjon varierte (tabell 4). Ved infusjon av medikament uten lipid var det 82 prosent av dem som jobbet ved lokalsykehus som byttet infusjonssett hver 24. time og 85 prosent av dem som jobbet ved universitetssykehus byttet hver 72. time. Ved infusjon av parenteral ernæring skiftet 94 prosent infusjonssett hver 24. time. Ved infusjon av Propofol® skiftet 55 prosent infusjonssett med seks til tolv timers mellomrom. Når det gjaldt tilhørende treveiskran var det kun 32 prosent som byttet den hver sjette til tolvte time. For ytterligere informasjon angående bytte av infusjonssett, se tabell 4.
Diskusjon
Områder som var i tråd med CDC’s guidelines
Det var to områder som i stor grad var i overensstemmelse med CDC’s guidelines. Det ene var hvor ofte infusjonssett byttes ved kontinuerlig infusjon av parenteral ernæring. Det at 94 prosent skifter infusjonssett med anbefalt frekvens, kan bety at man har fokusert mye på faren for kontaminering og oppvekst av bakterier i parenteral ernæring. Det var mye forskning på dette temaet på 70- og 80-tallet (16,17). Det er grunn til å tro at resultatene fra disse studiene har ført til økt oppmerksomhet på området. Det andre området var type bandasje som benyttes på SVK’s innstikkssted, 95,6 prosent oppga å bruke transparent bandasje. CDC’s guidelines anbefaler transparent semipermeabel bandasje som førstevalg. Denne gir mulighet til å inspisere innstikksstedet via den gjennomsiktige bandasjen, og den må ikke byttes så ofte som gasbandasjen. Gasbandasje anbefales imidlertid ved siving av blod og mye svette. De innsamlete data tyder på at gasbandasje i liten grad anses som et alternativ. Det var kun 28 respondenter som oppga gasbandasje som et alternativ, og av disse var det 9 som oppga gasbandasje som eneste alternativ. Dette kan tyde på at det ikke er kjent i Norge at gasbandasje er anbefalt til bruk på innstikkssted ved siving av blod og mye svette inntil problemet er løst (tabell 1). Forskning som er gjort i forhold til disse to typene bandasjer har ikke gitt noen signifikant forskjell i antall infeksjoner (18). Utover de to nevnte områdene viste kartlagt praksis i varierende grad å være i tråd med CDC’s guidelines. Det er i overensstemmelse med sammenliknbare studier utført i andre land (9–12).
Håndhygiene, aseptisk teknikk
Det at kun 34 prosent oppga å alltid utføre håndhygiene før de skal koble til en infusjon eller sette et medikament fra en sprøyte i SVK, er ikke i tråd med forventet standard. I en intensivavdeling kan ting skje fort, og om man må gi legemiddeldosen manuelt, kan det føre til at man ikke rekker å desinfisere hender før man handler. Det ble imidlertid opplyst på spørreskjemaet, at det skulle fylles ut med tanke på en normal situasjon og ikke en akutt situasjon. Det skal være tilrettelagt med god tilgang med dispensere med hånddesinfeksjonsmiddel rundt pasientsengene slik at retningslinje i forhold til håndhygiene skal være enkel å etterleve (19). Når spørsmålet om håndhygiene ble stilt på en litt annen måte, var det 54 prosent som oppga å ha rene hender ved manipulering av koblinger og kraner på SVK. En mulig forklaring kan være at mange sykepleiere (66 prosent) ikke ser behovet for rene hender ved tilkopling av infusjon. At 54 prosent av sykepleierne hadde rene hender ved manipulering av koblinger og kraner er i tråd med undersøkelser som Folkehelseinstituttet viser til (19). Dette kan i så måte være representativt. Håndhygiene skal utføres både før og etter at man er i kontakt med koblinger og kraner, og ved skifte av bandasje på innstikkssted (tabell 1). Den mest vanlige årsaken til SVK-blodbaneinfeksjon er forurensing av koblinger og kraner på SVK. Dette skjer ved at mikroorganismer fra sykepleierens hender eller pasientens hud kommer i kontakt med inngangsporter, eller at koplingen på sprøyte eller infusjonsslange blir kontaminert (20). Skal man arbeide aseptisk må man benytte aseptisk non-touch teknikk og sterilt utstyr (21–23). God håndhygiene kombinert med aseptisk teknikk er enkle og effektive tiltak i forhold til å forebygge SVK-blodbaneinfeksjoner (4,24). Studier har vist at ved å innføre standardisering av aseptisk non-touch teknikk reduseres risikoen for å bli påført infeksjon (24–26). De innsamlede dataene fra seks intensivavdelinger tyder på at standarden tilknyttet håndhygiene, aseptisk non-touch teknikk og desinfisering av nøkkelpunkter bør styrkes.
Hyppighet av SVK-stell
Det ble avdekket stor spredning i praksis i forhold til hvor ofte SVK-stell ble gjennomført i form av å skifte helt inn til kateterkoblingen (tabell 3). Studien viser at en stor andel av dem som jobbet ved universitetssykehus skiftet helt inn til kateterkoblingen hver sjuende dag. CDC’s guidelines anbefaler å bytte inn til kateteret ikke oftere enn hver 96. time og ikke sjeldnere enn hver sjuende dag. Hver sjuende dag anbefales imidlertid kun om man benytter SVK som er innsatt med antimikrobielle midler (27). Det ble ikke spurt om hvilke SVK som benyttes, men det er grunn til å tro at det er vanlige kateter uten bakteriehemmende middel som benyttes i Norge.
Når det gjaldt bytte av bandasje på innstikksstedet oppga de fleste respondentene ved universitetssykehusene hver sjuende dag eller hyppigere ved indikasjon. Respondentene ved de andre sykehusene skiftet bandasje langt hyppigere. Her var praksis ved universitetssykehusene i stor grad i tråd med CDC’s retningslinje.
Bytte av infusjonssett ved kontinuerlig infusjon
Resultatene fra selvrapportert praksis viser at infusjonssett i for stor grad byttes hver 24. time uavhengig av hva som infunderes. Intensivsykepleiere ved lokal- eller regionsykehus byttet hyppigere infusjonssett enn intensivsykepleiere ved universitetssykehus. Studier som viser at det ikke ble påvist flere SVK-blodbaneinfeksjoner ved bytte av infusjonssett og tilhørende kraner eller koblinger hver sjuende dag, er utført på katetre med antimikrobielle midler (27). Det betyr at ved bruk av et vanlig SVK så er CDC’s anbefaling ikke oftere enn hver 96. time.
Når det gjaldt bytte av infusjonssett ved kontinuerlig infusjon av Propofol®, var det cirka halvparten som skiftet sett i henhold til anbefalt frekvens. Propofol® er en fettemulsjon uten konserveringsmidler, og mikrober som kommer i kontakt med dette legemiddelet har gode vekstforhold (28–29). Ut fra de innsamlede data kan det se ut som man ikke har fokusert tilstrekkelig på at infusjonssett, treveiskraner og koblinger, skal byttes hyppigere ved infusjon av lipidholdige medikamenter. I CDC’s guidelines står det at man skal bytte infusjonssett og tilhørende kraner hver sjette til tolvte time ved infusjon av Propofol®.
Oppsummering
Prosedyren rundt stell av SVK krever mye tid og ressurser. Denne studien viser at en stor del av respondentene utførte prosedyren hyppigere enn CDC’s guidelines anbefaler. Dette gjaldt både bytte av infusjonssett, treveiskraner eller toveiskoplinger og bandasje på innstikkssted. Hyppig manipulering av treveiskraner og koblinger, øker faren for at mikroorganismer får tilgang til kateterets innside og blodbane (4,20). Det kan være at mange sykepleiere ikke er oppmerksom på risikoen for å påføre pasienten en SVK-blodbaneinfeksjon.
Denne studien tyder på at praksis tilknyttet stell og bruk av SVK er sprikende og i for liten grad kunnskapsbasert. Som beskrevet har intensivsykepleiere ved universitetssykehusene i større grad en praksis i tråd med CDC’s guidelines, enn intensivsykepleiere ved lokal- eller regionsykehus. Forklaringen på dette kan være at universitetssykehus har større tilgang på ressurser knyttet opp mot forskning, fagutvikling og undervisning.
Det bør settes inn ressurser i forhold til undervisning og økt oppmerksomhet på områdene vi har tatt opp i denne artikkelen. Det er utført flere studier i forhold til effekten av å innføre undervisning, trening og vektlegging over tid i forhold til å forebygge SVK-blodbaneinfeksjoner. Disse studiene viser at antall infeksjoner synker signifikant og holder seg på et lavt nivå over tid om man fortsetter å fokusere på disse tiltakene i avdelingen (1,20,24,30–33). Ved å følge CDC’s anbefalinger som er grunnlagt på massiv forskning, kan man redusere antall SVK-blodbaneinfeksjoner. Man vil frigi tid til andre formål ved at tidkrevende prosedyrer ikke utføres så hyppig, og man vil spare ressurser og miljø i form av redusert forbruk av utstyr.
Metodekritikk
Utvalget ble tatt ut fra et hensiktsmessig ståsted for at avdelingene skulle kunne nås fysisk av forfatter. Denne studien har et begrenset utvalg og funnene kan dermed ikke generaliseres til å gjelde ved alle intensivavdelinger i Norge. Tidligere sammenliknbare studier har imidlertid liknende resultat (9–12) og dette kan styrke den ytre validiteten av funnene.
En svarprosent på 52,4 prosent er lavt, men ikke uvanlig ved spørreskjemaundersøkelser. Det er omdiskutert hva som er tilstrekkelig responsrate. Noen mener at alt under 70 prosent er uakseptabelt (14), mens andre kan akseptere 50 prosent eller lavere (34). Ved lav svarrespons vil analysene basert på surveydata være beheftet med risiko for vurderingsskjevhet (14). En høyere svarrespons vil kunne ha gitt et annet resultat. Vi vet ikke noe om de sykepleierne som svarte er de mest engasjerte, men om det var tilfelle kunne en høyere svarrespons gitt en enda større spredning i kartlagt praksis. Det kan også være at avdelinger med en praksis som i større grad er i overensstemmelse med CDC’s gudielines, ikke er inkludert i denne studien.
Ved utfylling av spørreskjemaer kan det være at respondentene ikke oppfatter spørsmålene slik som det var ment ved utvikling av spørreskjemaet. Begrepet aseptisk non-touch teknikk er muligens et ukjent begrep og det kan tenkes at flere hadde svart positivt på spørsmålet om det hadde stått aseptisk teknikk. Diskrepansen i forhold til hvor mange som svarte positivt på at det var fokus på aseptisk teknikk i avdelingen, og som svarte negativt på spørsmål om de benyttet non-touch teknikk, kan tyde på det.
Konklusjon
Praksis rundt stell og bruk av SVK var i varierende grad i overensstemmelse med CDC’s guidelines. Praksis var sprikende både innad i avdelingene og mellom sykehusene. En nasjonal retningslinje kan være et hensiktsmessig arbeidsredskap for å oppnå og sikre ensartet praksis ved sykehusene i Norge. Det er behov for videre forskning innen dette feltet for å følge utviklingen i praksis.
Referanser
1. Eggimann P. Prevention of intravascular catheter infection. Curr Opin Infect Dis. 2007; 20:360–9.
2. Edwards JR, Peterson KD, Andrus ML, Tolson JS, Goulding JS, Dudeck MA, et al. National Healthcare Safety Network (NHSN) Report, data summary for 2006, issued June 2007. Am J Infect Control. 2007; 35:290–301.
3. Warren DK, Quadir WW, Hollenbeak CS, Elward AM, Cox MJ, Fraser VJ. Attributable cost of catheter-associated bloodstream infections among intensive care patients in a nonteaching hospital. Crit Care Med. 2006; 34:2084–9.
4. O›Grady NP, Alexander M, Burns LA, Dellinger EP, Garland J, Heard SO, et al. Guidelines for the prevention of intravascular catheter-related infections. Am J Infect Control. 2011; 39:S1–34.
5. Dimick JB, Pelz RK, Consunji R, Swoboda SM, Hendrix CW, Lipsett PA. Increased resource use associated with catheter-related bloodstream infection in the surgical intensive care unit. Arch Surg. 2001; 136:229–34.
6. Berenholtz SM, Pronovost PJ, Lipsett PA, Hobson D, Earsing K, Farley JE, et al. Eliminating catheter-related bloodstream infections in the intensive care unit. Crit Care Med. 2004; 32:2014-2020.
7. Blot Sl, Depuydt P, Annemanns L, et al. Clinical and economic outcomes in critically ill patients with nosocomial catheter related bloddstream infections. Clin Infect Dis 2005; 41:1591-1598
8. Pronovost PJ, Goeschel CA, Colantuoni E, Watson S, Lubomski LH, Berenholtz SM, et al. Sustaining reductions in catheter related bloodstream infections in Michigan intensive care units: observational study. BMJ. 2010;340:c309.
9. Labeau SO, Labeau SO, Vandijck DM, Rello J, Adam S, Rosa A, et al. Centers for Disease Control and Prevention guidelines for preventing central venous catheter-related infection: results of a knowledge test among 3405 European intensive care nurses. Crit Care Med. 2009; 37:320-323.
10. Rickard CM, Courtney M, Webster J. Central venous catheters: a survey of ICU practices. J Adv Nurs. 2004; 48:247-256.
11. Labeau S, Labeau S, Vereecke A, Vandijck DM, Claes B, Blot SI. Critical care nurses› knowledge of evidence-based guidelines for preventing infections associated with central venous catheters: an evaluation questionnaire. Am J Crit Care. 2008; 17:65-72.
12. Koutzavekiaris I, Vouloumanou EK, Gourni M, Rafailidis PI, Michalopoulos A, Falagas ME. Knowledge and practices regarding prevention of infections associated with central venous catheters: a survey of intensive care unit medical and nursing staff. Am J Infect Control. 2011; 39:542-547.
13. Gastmeier P, Geffers C. Prevention of catheter-related bloodstream infections: analysis of studies published between 2002 and 2005. The Journal of hospital infection. 2006; 64:326-335.
14. Polit DF, Beck CT. Nursing research. 9th ed. ed. Philadelphia, Pa.: Wolters Kluwer Health; 2012. XIV 802 p.
15. Bradburn N, Seymour S, Wansink B. Asking Questions. The definitive Guide to Questionnaire Design. Jossey-Bass; 2004
16. Melly M, Meng HC, Schaffner W. Microbial Growth in Lipid Emulsions Used in Parenteral Nutrition. Arch Surg. 1975; 110:1479-1481.
17. Gilbert M, Gallagher C, Eads M, Elmore M. Microbial Growth Patterns in a Total Parenteral Nutrition Formulation Containing Lipid Emulsion. Journal of Parenteral and Enteral Nutrition. 1985; 10:494-497.
18. Webster J, Gillies D, O›Riordan E, Sherriff KL, Rickard CM. Gauze and tape and transparent polyurethane dressings for central venous catheters. Cochrane Database Syst Rev. 2011
19. Nasjonal veileder for håndhygiene. Oslo: Nasjonalt folkehelseinstitutt; 2004.
20. Vandijck DM, Labeau SO, Secanell M, Rello J, Blot SI. The role of nurses working in emergency and critical care environments in the prevention of intravascular catheter-related bloodstream infections. Int Emerg Nurs. 2009; 17:60-8.
21. Rowley S, Rowley S. Aseptic non-touch technique. Nurs Times. 2001; 15-21; 97:VI-VIII.
22. Rowley S, Clare S. ANTT: a standard approach to aseptic technique. Nurs Times. 2011; 13-19;107:12-14.
23. Godfrey K, Godfrey K. Implement the ANTT national standard today. Nurs Times. 2011; 13-19;107:11.
24. Coopersmith CM, Coopersmith CM, Rebmann TL, Zack JE, Ward MR, Corcoran RM, et al. Effect of an education program on decreasing catheter-related bloodstream infections in the surgical intensive care unit. Crit Care Med. 2002; 30:59-64.
25. Rowley S, Rowley S, Clare S. Improving standards of aseptic practice through an ANTT trust-wide implementation process: a matter of prioritisation and care. J Infect Prev. 2009; 10:18-23.
26. Eggimann P, Harbarth S, Constantin MN, Touveneau S, Chevrolet JC, Pittet D. Impact of a prevention strategy targeted at vascular-access care on incidence of infections acquired in intensive care. Lancet. 2000; 27;355:1864-1868.
27. Rickard CM, Lipman J, Courtney M, Siversen R, Daley P. Routine changing of intravenous administration sets does not reduce colonization or infection in central venous catheters. Infect Control Hosp Epidemiol. 2004; 25:650-655.
28. Muller AE, Huisman I, Roos PJ, Rietveld AP, Klein J, Harbers JB, et al. Outbreak of severe sepsis due to contaminated propofol: lessons to learn. The Journal of hospital infection. 2010; 76:225-230.
29. Haddad S, Tamim H, Memish ZA, Arabi Y. Association of preservative-free propofol use and outcome in critically ill patients. Am J Infect Control. 2011; 39:141-147.
30. Pronovost P, Needham D, Berenholtz S, Sinopoli D, Chu H, Cosgrove S, et al. An intervention to decrease catheter-related bloodstream infections in the ICU. N Engl J Med. 2006; 28;355:2725-2732.
31. Dumont C, Dumont C, Nesselrodt D. Preventing CLABSI central line-associated bloodstream infections. Nursing. 2012; 42:41-47.
32. Helder OK, Latour JM. Reduction of catheter related bloodstream infections in intensive care: one for all, all for one? Nurs Crit Care. 2009; 14:107-108.
33. Warren DK, Zack JE, Mayfield JL, Chen A, Prentice D, Fraser VJ, et al. The effect of an education program on the incidence of central venous catheter-associated bloodstream infection in a medical ICU. Chest. 2004; 126:1612-1618.
34. Lund T, Haugen R, Fønnebø B. Forskningsprosessen. [Oslo]: Unipub; 2006. IV 188 p



















0 Kommentarer