Livskvalitet, depressive symptomer og funksjonssvikt hos personer med demens
Sammendrag
Bakgrunn:
Det er usikkert om sammenhengen mellom livskvalitet, depressive symptomer og funksjonssvikt er like sterk hos personer med demens som hos dem uten demens.
Hensikt:
Å undersøke sammenhengen mellom livskvalitet, depressive symptomer, funksjonssvikt og grad av demens.
Metode:
Opplysninger om 223 pasienter med demens i sykehjem ble innhentet gjennom intervju av pasientenes primærpleiere. Livskvalitet ble kartlagt med Quality of life in late stage dementia scale (QUALID), symptomer på depresjon med Cornell skala, funksjonsevne med Lawtons ADL skala og grad av demens med Klinisk demensvurdering.
Resultater:
Korrelasjonsanalyser viste at livskvalitet var signifikant assosiert til depressive symptomer, grad av demens og tap av funksjonsevne. Spearman’s korrelasjon varierte mellom 0,37 og 0,53. En trinnvis lineær regresjonsanalyse viste at fire av fem subskalaer i Cornell skalaen, affekt-, adferds-, retardasjon – og syklisk subskala var signifikant assosiert med QUALID-skåren. Den fysiske sub skalaen var det ikke fordi sub skalaene retardasjon og fysisk korrelerte sterkt. Tap av funksjonsevne og grad av demens var også signifikant relatert til redusert livskvalitet.
Konklusjon:
Livskvalitet hos personer med demens påvirkes av depresjonssymptomer, spesielt kjernesymptomer for depressiv lidelse, og funksjonsnivå.
Referer til artikkelen
Mjørud M, Engedal K, Ytrehus S. Livskvalitet, depressive symptomer og funksjonssvikt hos personer med demens. Sykepleien Forskning. 2011;6(2):176-184. DOI: 10.4220/sykepleienf.2011.0101
Introduksjon
I denne studien har vi sett på hvordan depressive symptomer og funksjonssvikt virker inn på livskvalitet hos personer med demens.
Livskvalitet er et multidimensjonalt begrep som inneholder både subjektive og objektive verdier (1-6), men det er en persons subjektive tolkning av en objektiv opplevelse som virkelig definerer hva livskvalitet er (7). Ulike faktorer påvirker livskvalitet hos personer med demens (8-12), blant annet får de utover i sykdommen problemer med å uttrykke tanker og følelser, og hukommelsen reduseres (13). Dette reduserer personens egen mulighet til selv å beskrive hvordan livet oppleves. Det er derfor viktig at de som arbeider med personer med demens i sykehjem har kompetanse om hva som kan påvirke livskvaliteten til denne pasientgruppen (14).
Mange studier viser at det er sammenheng mellom depresjon og livskvalitet (15-17). Det er imidlertid usikkert om sammenhengen mellom depressive symptomer og livskvalitet er like sterk hos personer med demens som hos dem med normal kognisjon. Det er flere grunner til dette. Depresjon hos personer med demens kan forårsakes av patologiske endringer i hjernen på grunn av demensutvikling (18-20). I tillegg kan den kliniske manifestasjonen av depresjon ved demens være annerledes enn hos dem uten demens. Depressive symptomer som angst, irritabilitet, agitasjon og manglende glede og motivasjon til å delta i aktiviteter er hyppig forekommende hos personer med demens (18, 21-24). De typiske depressive symptomene som følelse av håpløshet og skyldfølelse er mindre til stede (19, 25). Dette kan blant annet skyldes at pasienter med demens, særlig av moderat til alvorlig grad, har problemer med abstrakt tenkning, hukommelse og språkforståelse. På grunn av disse problemene er det også vanskelig å vurdere livskvalitet hos denne gruppen (9, 26).
Det er videre usikkert i hvor stor grad svikt i evnen til å utføre dagliglivets aktiviteter virker inn på livskvalitet hos personer med demens. Flere studier har funnet at det ikke er sammenheng mellom livskvalitet og grad av funksjonssvikt blant personer med demens (10, 16, 27), mens andre studier finner at det er en sammenheng (6, 11, 28). I de ulike studiene ser man en tendens til at det oftere er sammenheng mellom funksjonsnivå og livskvalitet hos personer med demens når en annen enn pasienten gir informasjon. Denne sammenhengen ser man ikke i like stor grad dersom informasjon om livskvalitet og funksjonssvikt er selvrapportert (8, 26, 29). Problemstillingen om sammenhengen mellom livskvalitet hos personer med demens og depressive symptomer, funksjonssvikt og grad av demens er fortsatt aktuell. Ifølge dette er hensikten med studien er å undersøke om livskvalitet hos personer med demens er påvirket av depressive symptomer, grad av svikt i evnen til å utføre aktiviteter i dagliglivet (activities in daily living, ADL) og grad av demens.
Metode
Pasientene
I denne undersøkelsen er data fra 223 sykehjemspasienter med demens inkludert. Utvalgskriteriene for deltakelse var at pasientene hadde hatt fast opphold i sykehjem, hadde bodd der i minst fire uker og at det forelå samtykke til å delta.
Deltakerne var undersøkt tidligere i tre ulike tverrsnittsundersøkelser: I studie A ble Cornell skala testet for reliabilitet og validitet i norske sykehjem og sykehus. Fra denne studien inkluderte vi 29 pasienter fra ett sykehjem (30). Fra studie B inkluderte vi 84 pasienter fra to sykehjem som var med i et prosjekt i regi av Nasjonalt kompetansesenter for aldring og helse (Mjørud et al, upublisert). Fra studie C inkluderte vi 110 pasienter fra syv sykehjem (Røen I, 2009) (31) som var med i prosjekt i regi av Alderspsykiatrisk forskningssenter ved Sykehuset Innlandet. Alle data ble samlet inn mellom 2008 og 2009.
Datainnsamlingen
To forskningssykepleiere som hadde fått opplæring og trening i bruk av skalaene som ble benyttet i datainnsamlingen intervjuet pasientens primærsykepleiere for utfylling av skalaene. Følgende skalaer, som beskriver pasientene ble benyttet:
Quality of life in late stage dementia scale (QUALID) (9) måler livskvalitet hos personer med demens. Den består av 11 ledd, som alle beskriver en type observerbar adferd. Pasientens primærpleier blir bedt om å vurdere pasientens adferd på de 11 leddene den siste uken. Hvert ledd har fem svaralternativer, fra sjelden til mesteparten av dagen. Minimum skåre er 11 poeng, som indikerer god livskvalitet. Maksimum skår er 55 poeng, som indikerer dårlig livskvalitet. QUALID er oversatt til både svensk og norsk etter standard prosedyre med frem- og tilbakeoversettelse, og har vist seg å være et pålitelig verktøy (31, 32).
Clinical Dementia Rating Scale/Klinisk Demens Vurdering (CDR/KDV) (33) er et graderingsverktøy for demens. Seks områder kartlegges: hukommelse, orienteringsevne, problemløsning, samfunnsaktiviteter, hjemmemiljø og personlig omsorg. Leddene skåres fra 0–3, hvor 0 er helt frisk, 0,5 er mulig svikt, 1 er mild, 2 moderat og 3 alvorlig svikt. Demens ble definert som en skåre på KDV på 1 eller høyere. Andre studier i sykehjem viser at det er høyt samsvar mellom klinisk demensdiagnose og en KDV-skåre på 1 og høyere (34). Totalskåren er som for de seks kategoriene 0, 0,5, 1, 2 og 3 og indikere ingen kognitiv svikt, mulig demens, mild, moderat og alvorlig grad av demens. Man kan også regne ut totalskåren som da vil variere fra 0 til 18. Ifølge flere tidligere undersøkelser er det høygradig korrelasjon (Pearson r 0,9) mellom den kategoriske skåren og totalskåren (15, (35). I vår studie var Spearman’s rho 0,91 mellom KDV kategorisk skåre og totalskåren.
Cornell scale for depression in dementia (Cornell) (36) er den mest brukte skalaen til vurdering av depressive symptomer hos personer med demens. Skalaen består av 19 ledd. Det er tre mulige svarverdier, 0, 1 og 2 avhengig av hvor ofte symptomene er til stede. Det er også et fjerde alternativ der skåring ikke er mulig. Skåringen baseres på symptomer og tegn på depresjon som har vært til stede de siste to ukene, og det er pasientens primærpleier som blir bedt om å angi grad av depressive symptomer. Minimumskåren er 0 poeng, som indikerer ingen depressive symptomer. Maksimumskåren er 38 poeng som indikerer alvorlig grad av depresjon. Grenseverdi for depressiv lidelse er ifølge en stor og solid norsk undersøkelse 8 poeng (30). På basis av Barca og medarbeideres faktoranalyse av skalaen er det definert fem subskalaer (19). Disse subskalaene er: affekt subskala (selvmordstanker, pessimisme, dårlig selvtillit, tristhet, angst og vrangforestillinger) og fire ikke-affekt subskalaer kalt fysisk subskala (redusert appetitt, vekttap, tap av energi og tap av interesser), syklisk subskala (hyppige oppvåkninger i løpet av natten, vanskeligheter med å sovne og tidligere morgenoppvåkninger enn vanlig), retardasjons subskala (retarderte bevegelser, manglende evne til å glede seg og tap av interesser) og adferds subskala (døgnvariasjoner i humøret, irritabilitet og agitasjon). Cornellskalaen registrerer også symptomet «uttalte kroppslige plager». Dette symptomet tilhørte ingen av de fem subskalaene (19).
Med en grenseverdi for depresjon på 8 poeng er skalaens sensitivitet for å avdekke en depressiv lidelse ifølge ICD-10-kriteriene 68 prosent og spesifisitet 74 prosent ifølge Barca og medarbeidere (30).
Physical self-maintenance scale (PSMS) (37) er en seksleddet skala som kartlegger pasientens funksjonsevne i personlige aktiviteter i dagliglivet (P-ADL). Det er basisfunksjoner som kartlegges, som fungering i spisesituasjoner, ved egenpleie og fysisk bevegelse. Hvert av punktene skåres fra 1-5, jo høyere skåre, jo lavere funksjonsevne. Minimumsskåre er 6 og maksimumskåre er 30. Fra journalen ble informasjon om pasientens kjønn og alder hentet.
Etikk
Alle tre studiene er godkjent av Regional etisk komité for helsefaglig forskning i Helse Sør-Øst (REK Helse sør øst). I denne sammenstillingen ble kun anonyme data benyttet og REK ga sin godkjenning til dette. Informert samtykke ble innhentet i de opprinnelige studiene, enten fra pasienten eller fra nærmeste pårørende i de tilfellene pasienten ikke hadde samtykkekompetanse.
Statistikk
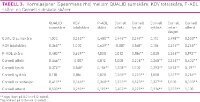
Data ble analysert ved bruk av statistisk program for sosial forskning (SPSS), versjon 16. Variablene, QUALID sum skåre, Cornell sum skåre, KDV, P-ADL, alder og kjønn ble undersøkt for normal- og skjevfordeling, gjennomsnitts-verdier, standardavvik og median. Vi undersøkte distribusjon av de kontinuerlige variablene, QUALID sum skåre, KDV, P-ADL og Cornell sum skåre, med histogrammer, box-plots og Q-Q plots. Skårene for KDV og P-ADL var normalfordelte, og skårene for Cornell sum skåre og QUALID sum skåre var nesten normalfordelte. For korrelasjonsanalyser brukte vi derfor Spearman's rho. Vi utførte først en korrelasjonsanalyse mellom QUALID sum skåre, Cornell sum skåre, KDV totalskår, P-ADL skåre og alder. KDV totalskår ble brukt for å få større spredning i materialet. Korrelasjonsanalysen mellom QUALID sum skåre, Cornell sum skåre, KDV totalskår, P-ADL skåre og alder viste en høy korrelasjon mellom QUALID sum skåre og Cornell totalsum (Spearman’s rho 0,64). Vi utførte derfor nye korrelasjonsanalyser (Spearman’s rho), mellom Cornells fem subskalaer og QUALID sum skåre.
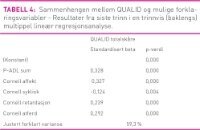
Det neste steget i analyseplanen var å utføre en trinnvis multippel lineær regresjonsanalyse med QUALID sum skåre som avhengig variabel. Fordi Cornell sum skåre og QUALID sum skåre korrelerte høygradig brukte vi ikke Cornell sum skåre som uavhengig variabel, men skårene på de fem ulike sub skalaene, hvor korrelasjonen med QUALID var fra 0,11 til 0,53. I tillegg ble kjønn, alder, KDV totalskår og P-ADL skåre benyttet som uavhengige variabler. Flere av forklaringsvariablene korrelerte høyt med hverandre og av den grunn utførte vi en trinnvis regresjonsanalyse. Vi utførte denne både framlengs og baklengs og gjorde det både manuelt og lot SPSS-programmet styre analysen. Resultatene ble de samme.
Ettersom skårene på QUALID og Cornell var nesten normalfordelte og med Cooks distansen under 1 og hverken box-plots eller Q-Q plots var avvikende, så vi det ikke som nødvendig å logaritmisere noen av skårene til bruk i regresjonsanalysen.
Resultater
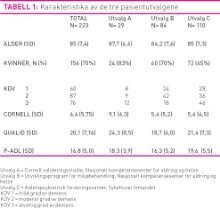
Karakteristika for de 223 pasientene er gjengitt for hele gruppen og separat for hver gruppe (A-C) i tabell 1. I alt var 156 (70 prosent) kvinner og gjennomsnittsalderen var 85 år (7,4 SD). Av alle skåret 60 (28 prosent) 1 på KDV, 87 (39 prosent) 2 på KDV og 76 (33 prosent) 3 på KDV. Gjennomsnittlig QUALID skåre var 20,1 (SD 7,16). Gjennomsnittlig Cornell skåre var 6,4 (SD 5,75) og gjennomsnittlig P-ADL skåre var 16,8 (SD 5,0). Resultatene for korrelasjonsanalysene er vist i tabell 2 og tabell 3. I tabell 4 har vi gjengitt resultatene for det siste trinnet i den trinnvise (baklengs) multiple lineære regresjonsanalysen. Når både KDV og P-ADL skåre ble inkludert i regresjonsanalysen samtidig, mistet variabelen KDV sin signifikans som forklaringsvariabel, noe som tyder på samvariasjon (tabell 3) mellom de to variablene. Det samme skjedde når vi inkluderte både Cornell fysisk- og retardasjon subskala. På grunn av sterk samvariasjon (tabell 3) mistet fysisk subskala sin signifikans som forklaringsvariabel for QUALID sum skåre.

Diskusjon
Hovedresultatet av analysene viser at depressive symptomer og grad av funksjonssvikt påvirker livskvalitet hos personer med demens. Grad av demens gjør det også, men sammenhengen mellom livskvalitet og grad av demens påvirkes av pasientenes funksjonsevne.
Våre resultater samsvarer med flere andre studier, som indikerer at personer med demens med mange depressive symptomer har dårligere livskvalitet (5, 8, 10, 12, 15, 16) enn dem uten depresjon. Resultatene indikerer også at livskvalitet målt med QUALID i høy grad faktisk måler grad av depresjonssymptomer. Men en høy Cornell sum skåre betyr ikke nødvendigvis at personen med demens har en depressiv lidelse. Cornellskalaens gyldighet er kun middels god, muligens fordi demens- og depresjonssymptomer overlapper.
Både korrelasjonsanalysen og den trinnvise multiple lineære regresjonsanalysen viser at det er affekt (beta 0,33) og adferd (beta 0,29) subskalaene for depresjon, ved siden av funksjonssvikt (P-ADL) som påvirker QUALID mest. «Affekt subskalaen» inneholder typiske kjernesymptomer på depresjon som tristhet, pessimisme, selvmordstanker og dårlig selvtillit. «Retardasjon subskalaen» er også signifikant assosiert (beta 0,18) til redusert livskvalitet målt med QUALID. Denne subskalaen inneholder symptomene «tap av interesser» og «manglende evne til å glede seg», to klassiske symptomer som sees ved en depressiv lidelse. Det kan bety at redusert livskvalitet hos personer med demens er assosiert med en depressiv lidelse. «Adferds subskalaen» inneholder symptomer som er knyttet til kognitiv svikt og demenssykdom. Symptomene kan være uttrykk for urolig adferd hos personer med demens, og ses ofte når personen ikke forstår sine omgivelser. Flere studier finner likevel at irritabilitet er et vanlig symptom på depresjon hos personer med demens (18, 20). Våre funn støtter derfor opp under de nye foreslåtte kriteriene for depresjon ved demens, «the provisional criteria for depression in Alzheimer's disease» der irritabilitet regnes som et symptom på depresjon (38). Det kan imidlertid diskuteres om sammenhengen mellom adferd, affekt og livskvalitet i våre funn gir en riktig beskrivelse av hvordan personen med demens selv opplever sin situasjon. Selv om flere proxybaserte studier finner en signifikant sammenheng mellom adferd og livskvalitet, ser man i studier hvor personen med demens selv har gitt opplysninger om sin livskvalitet, at denne sammenhengen minsker eller forsvinner (29, 39, 40). Dette kan ha sammenheng med redusert innsikt i egen situasjon, men kan også være et uttrykk for at adferd som pleiepersonell opplever som problematisk, ikke er det for personen med demens (8, 41).
Den sykliske subskalaen korrelerer ikke med hverken QUALID eller KDV i korrelasjonsanalysen og i den trinnvise regresjonsanalysen, justert for de andre variablene, er den negativt assosiert med QUALID skåren, jo færre symptomer jo høyere skåre på QUALID, det vil si dårligere livskvalitet. Dette kan virke noe underlig fordi det er nærliggende å tro at god søvn er bra for god livskvalitet. En forklaring på den manglende sammenhengen med livskvalitet (tabell 3) kan være at søvnforstyrrelser forårsakes av somatisk sykdom (19). Den manglende korrelasjonen med KDV kan bety at de sykliske symptomene heller ikke har noe med demens å gjøre, noe som styrker antakelsen om at det kan være somatiske plager som forstyrrer søvnen. Den fysiske subskalaen, som korrelerer med QUALID skåren i korrelasjonsanalysen blir ikke signifikant i den trinnvise regresjonsanalysen. Det betyr ikke at symptomene i den fysiske subskalaen ikke har betydning for livskvalitet, men at en annen variabel som samvarierer med den fysiske subskalaen «går foran» i regresjonsanalysen. Dette er subskalaen retardasjon, som korrelerer høyt med den fysiske subskalaen; Spearman’s rho 0,57.
I våre analyser er kjønn ikke signifikant korrelert med livskvalitet. Dette er i samsvar med andre studier (5, 8, 17). Sammenhengen mellom alder og livskvalitet er uklar i vår studie. Flere studier finner ikke sammenheng mellom alder og livskvalitet (5, 42, 43), mens andre studier har funnet en signifikant sammenheng mellom alder og livskvalitet (16).
I korrelasjonsanalysen er P-ADL skåre og KDV totalsum statistisk signifikant assosiert til QUALID skåre, mens kun P-ADL skåre er signifikant assosiert til livskvalitetsmålet i den trinnvise regresjonsanalysen. Dette betyr at pasientens funksjonsevne er en viktig faktor for livskvalitet hos personer med demens. Funnet er i overensstemmelse med tidligere studier (6, 11, 15, 44), og er ikke overraskende. Tap av egenomsorgsevne og autonomi er faktorer som man ut fra «common senses» forstår influerer på en persons livskvalitet.
Flere studier viser at personer med demens kan ha god livskvalitet uavhengig av grad av demens (10, 16, 27, 40, 45). Våre resultater er derfor i samsvar med annen forskning. Hoe (2009) finner at grad av kognisjon henger sammen med livskvalitet. I den studien forklares dog sammenhengen med at det er opplevelsen av sykdommens progresjon som forverrer livskvaliteten og ikke reduksjonen i kognisjon (17). Hos personer med moderat grad av demens finner Hurt (2010) bedre livskvalitet hos personer med redusert innsikt i egen situasjon (12), noe som støtter funnene til Hoe og medarbeidere. Antakelig er det slik at flere faktorer som individets tilpassingsevne, personlighet, innsikt i egen situasjon og tidligere mestringsstrategier og funksjonsevne (vår studie) avgjør hvordan livskvaliteten påvirkes av demenssykdommen (27). Det kjente ordtaket om at «det er ikke hvordan man har det, men hvordan man tar det», får dermed støtte. Lav representasjon av pasienter med alvorlig grad av demens kan ikke forklare den manglende sammenhengen mellom livskvalitet og grad av demens når vi justerer for pasientenes funksjonsevne. Mer enn 70 prosent hadde moderat eller alvorlig grad av demens. Denne gruppen pasienter har ofte store kommunikasjons- og hukommelsesproblemer, og er vanskelig å vurdere. De trenger hjelp til å uttrykke sine tanker og følelser, og pleierne må tolke uttrykkene deres (46, 47). Det kan føre til feilvurderinger.
Studien har noen svakheter. Bruk av pleiepersonell som informanter og ikke pasientene selv, er selvfølgelig en svakhet ettersom livskvalitet i prinsippet er en subjektiv opplevelse. Men, det byr på store metodiske problemer å måle livskvalitet hos personer med moderat til alvorlig grad av demens ved å intervjue personene selv på grunn av omfattende kognitiv svikt. Proxybasert informasjon er derfor nødvendig for å undersøke denne pasientgruppen. Imidlertid vet vi at det fins en tendens til at ulike forklaringsvariabler og livskvalitet er mer assosiert til hverandre ved å bruke proxybaserte data, sammenlignet med selvrapportering. Det kan skyldes at pleiere skårer ut fra egen oppfatning av pasientens liv, ikke hvordan pasienten selv opplever livet sitt (17, 26, 39, 43, 48). På den måten kan vi få et noe fordreid bilde av pasientens virkelighet.
Andre svakheter med studien er de ulike måter å registrere demens hos alle pasientene. Kun i en av de tre studiene som analysene bygger på, ble pasientene diagnostisert med hensyn til en demenssykdom. Imidlertid vet vi at det fins et sterkt samsvar mellom KVD-skåre på 1 og høyere og diagnosen demens blant pasienter i sykehjem (34, 49). Ettersom vi finner en sterk sammenheng mellom livskvalitet og kjernesymptomene for en depressiv lidelse, hadde det også vært en fordel om pasientene hadde vært diagnostisert med hensyn til en depresjonsdiagnose. Dette ble dessverre ikke gjort. Det kan også diskuteres om Cornell kan brukes til å måle depressive symptomer hos denne skrøpelige pasientgruppen eller om den måler demenssymptomer (19, 50). I mangel av et annet skjema, er det likevel Cornell som brukes i de fleste studier. Endelig vil vi også peke på at de inkluderte pasientene i studien ikke er tilfeldig utvalgte, noe som gjør at vi ikke med sikkerhet kan si at resultatene er representative for sykehjemsbeboerne i Norge. Styrken med studien er bruk av validerte evalueringsskjema. Alle skjemaene som ble brukt i denne studien har vært brukt i mange nasjonale og internasjonale studier, og alle er validert for norske forhold.
Konklusjon
Funnene i denne studien gjelder kun for de sykehjemmene vi har studert. Vi har brukt data fra ti ulike sykehjem, men utvalget er ikke representativt. Livskvalitet hos personer med demens påvirkes av symptomer for depressiv lidelse og funksjonsnivå. Mange symptomer som kan oppfattes som uttrykk for demens, kan være uttrykk for en depressiv lidelse og må møtes som det. Pleiere i sykehjem bør være oppmerksomme på de vanlige depressive symptomene ved en demenssykdom, slik at pasientene kan få riktig behandling.
Referanser
1. Ettema TP, Dröes RM, Lange J, Mellenbergh GJ, Ribbe MW. A review of quality of life instruments used in dementia. Quality of Life Research 2005;14:675-86.
2. Brooker D. What makes life worth living? Aging & mental health 2008;12:525-7.
3. Clark PG. Autonomy, Personal empowerment and Quality of life in long-term care. the Jounal of applied Gerontology 1988;7:279-97.
4. Harrison C. Personhood, Dementia and the integrity of a life. Canadian Journal on Aging/La Revue canadienne du viellissement 1993;12:428-40.
5. Menne HL, Judge KS, Whitlatch CJ. Predictors of quality of life for individuals with dementia: implications for intervention. Dementia 2009;8:543-60.
6. Moyle W, McAllister M, Venturato L, Adams T. Quality of life and dementia. The voice of the person with dementia. Dementia 2007;6:175-91.
7. Brod M, Stewart AL, Sands L. Conceptualization of Quality of Life in dementia. Jounal of Mental Health1999;5:7-19.
8. Banerjee S, Samsi K, Charles DP, Alvir J, Treglia M. What do we know about quality of life in dementia? A review of the emerging evidence on the predictive and explanatory value of disease specific measures of health related quality of life in people with dementia. Int J Geriatr Psychiatry. [review article]. 2009;24:15-24.
9. Weiner MF, Martin-Cook K, Svetlik DA, Saine K, Foster B, Fountaine CS. The Quality of life in Late-stage dementia (QUALID) scale. J Am Med Dir Assoc2000:114-6.
10. Selwood A, Thorgrimsen L, Orrell M. Quality of life in dementia. A one year follow up. . Int J Geriatr Psychiatry 2005:232-7.
11. Ballard C, O›Brien J, James I, Mynt P, Lana M, Potkins D, et al. Quality of life for people with dementia living in Residential and nursing home care: the impact of performance on Activities of daily living, behavioral and psychological symptoms, language skills, and psychotropic drugs. International Psychogeriatrics 2001;13:93-106.
12. Hurt CS, Banerjee S, Tunnard C, Whitehead DL, Tsolaki M, Mecocci P, et al. Insight, cognition and quality of life in Alzheimer›s disease. J Neurol Neurosurg Psychiatry 2010;81:331-6.
13. Engedal K, Haugen PK. Demens- fakta og utfordringer. 3 ed. Sem: Nasjonalt kompetansesenter for aldring og helse; 2004.
14.SHdir aP. Glemsk, men ikke glemt! om dagens situasjon og framtidas utfordringer for å styrke tjenestetilbudet til personer med demens. In: Helsedirektoratet So, editor. Oslo: Oslo forlagstrykkeri AS; 2007.
15. Logsdon RG, Gibbons LE, McCurry SM, Teri L. Quality of life in Alzheimer›s disease: patient and caregiver reports. J Ment Health Aging 1999;5:21-32.
16. Banerjee S, Smith SC, Lamping DL, Harwood RH, Foley B, Smith P, et al. Quality of life in dementia: more than just cognition. An analysis of associations with quality of life in dementia. J Neurol Neurosurg Psychiatry 2006;77:146-8.
17. Hoe J, Hancock G, Livingston G, Woods B, Challis D, Orrell M. Changes in the Quality of life of people with dementia living in care homes. Alzheimer Disease and associated disorders 2009;23:285-90.
18. Selbæk G, Kirkevold Ø, Engedal K. The prevalence of psychiatric symptoms and behavioural disturbances and the use of psychotropic drugs in Norwegian nursing homes. Int J Geriatr Psychiatry 2006.
19. Barca ML, Selbæk G, Laks J, Engedal K. The pattern of depressive symptoms and factor analysis of the Cornell scale among patients in Norwegian nursing homes. Int J Geriatr Psychiatry 2008;23:1058-65.
20. Verkaik R, Francke AL, Meijel Bv, Ribbe MW, Bensing JM. Comorbid Depression in Dementia on Psychogeriatric nursing home Wards: Which Symptoms are Prominent? The American journal of Geriatric Psychiatry 2009;17:565-73.
21. Rozzini R, Boffeli S, Franzoni S. Prevalence and predictors of depressive symptomes in a nursing home. Int J Geriatr Psychiatry1996;11:629-34.
22. Ames D. Depressive disorders among elderly people in long-term institutional care. Aust N Z J Psychiatry 1993;27:379-91.
23. Anstey KJ, Von Sanden C, Sargent-Cox K, Luszcz MA. Prevalence and risk factors for depression in a longitudinal, population-based study including individuals in the community and residential care. Am J Geriatri Psychiatry 2007;15:497-505.
24. Jongenelis K, Pot AM, Eissis AM. Depression among older nursing home patients. A review. Tijdschr Gerontol Geriatr 2003;34:52-9.
25. Rosenberg PB, Lyketsos CG. Depression in Alzheimer disease. In: Evans DL CD, Lewis L, editor. The Physicians guide to depression & bipolar disorders: The McGraw-Hill; 2006. p. 303–32.
26. Cahill S, Begley E, Topo P, Saarikalle K, Macijauskiene J, Budraitiene A, et al. I know where this is going and I know it won›t go back: Hearing the individual›s voice in dementia quality of life assessments. Dementia 2004;3:313-30.
27. Lyketsos CG, Gonzales-Salvador T, Chin JJ, Baker A. A follow-up study of change in quality of life among persons with dementia residing in a long-term care facility. Int J Geriatr Psychiatry 2003;18:275-81.
28. Hoe J, Hancock G, Livingston G, M. O. Quality of life of people with dementia in residential care homes. Br J Psychiatry 2006 May; 188:460-4.
29. Kolanowski A, Hoffman L, Hofer SM. Concordance of self-report and informant assessment of emotional well-being in nursing home residents with dementia. The Journals of Gerontology 2007;62B:20-7.
30. Barca ML, Engedal K, Selbæk G, the cornell study group. A reliability and validity study of the Cornell Scale among elderly inpatients, using various clinical criteria. Dementia and Geriatric Cognitive disorders 2010;29:438-47.
31. Røen I. Livskvalitet hos personer med demens. Oversettelse og testing av reliabilitet og validitet av den norske versjonen av « Quality of Life in Late-Stage dementia (QUALID) scale». [Master oppgave]. In press 2009.
32. Falk H, Persson LO, Wijk H. A psychometric evaluation of a Swedish version of the Quality of life in Late-stage dementia (QUALID) scale. International Psychogeriatrics 2007;19:1040-50.
33. Hughes CP, Berg L, Danziger WL, Coben LA, Martin RL. A new clinical scale for the staging of dementia. Br J Psychiatry 1982;140:566-72.
34. Engedal K, PK. Haugen. The prevalence of dementia in a sample of elderly Norwegians. Int J Geriatr Psychiatry 1993;8:565-70.
35. Barca ML, Engedal K, Laks J, Selbæk G. A 12 months follow-up study of depression among nursing-home patients in Norway. J Affect Disord 2009.
36. Alexopoulos GS, Abrams RC, Young RC, Shamoian CA. Cornell Scale for Depression in Dementia. Biol Psychiatry1988;23:271-84.
37. Lawton MP, Brody EM. Assessment of older people: self -maintaining and instrumental activities of daily living. . Gerontologist 1969;9:179-86.
38. Olin JT, Katz I, Meyers BS, Schneider LS, Lebowitz BD. Provisional Diagnostic Criteria for Depression of Alzheimer Disease. Am J Geriatri Psychiatry 2002;10:129-41.
39. Kane RL, Rosalie AK, Bershadsky B, Degenholtz H, Kling K, Totten A, et al. Proxy sources for information on nursing home residents quality of life. The Journals of Gerontology 2005;60B:318-25.
40. J. H, Hancock G, Livingston G, Orrell M. Quality of life of people with dementia in residential care homes. Br J Psychiatry 2006 May; 188:460-4.
41. Snow AL, Graham DP, Molinari VA. Factors affecting Deficit awareness in persons with dementia. Dementia and Geriatric Cognitive disorders 2005;20:133-9.
42. Fuh J, Wang S. Assessing quality of life in Taiwanese patients with Alzheimer›s disease. Int J Geriatr Psychiatry 2006;21:103-7.
43. Ready RE, Ott BR, Grace J. Patient versus informant perspectives of quality of life in mild cognitive impairment and Alzheimer›s disease. Int J Geriatr Psychiatry 2004;19:256-65.
44. Barca ML, Selbæk G, Laks J, Engedal K. Factors associated with depression in Norwegian nursing homes. Int J Geriatr Psychiatry 2008.
45. Hoe J, Katona C, Roch B, Livingston G. Use of the QOL-AD for measuring quality of life in people with severe dementia- the LASER-AD study. Age & Ageing 2005;34:130-5.
46. Volicer L, Camberg L, Hurley AC, Ashley J, Woods P, Ooi WL, et al. Dimensions of decreased psychological well-being in Advanced Dementia. Alzheimer Disease and associated disorders1999;13:192-201.
47. Bourbonnais A, Ducharme F. The meaning of screams in older people living with dementia in a nursing home. International Psychogeriatrics 2010.
48. Novella JL, Jochum C, Jolly D, Morrone I, Ankri J, Bureau F, et al. Agreement between patients› and proxies› reports of quality of life in Alzheimer›s disease. Quality of Life Research 2001;10:443-52.
49. Nygaard HA, Ruths S. Missing the diagnosis: senile dementia in patients admitted to nursing homes. Scand J Primary Health care 2003;21:148-52.
50. Kurlowicz LH, Evans LK, Strumpf NE, Maislin G. A psychometric evaluation of the cornell scale for depression in dementia in a frail, nursing home population. Am J Geriatri Psychiatry 2002;10:600-8.

















0 Kommentarer