Verktøy for tidlig oppdagelse av forverring hos eldre utenfor sykehus – en systematisk kartleggingsoversikt
Sammendrag
Bakgrunn: Mange eldre er sårbare og ekstra utsatt for forverret somatisk tilstand. Det krever høy observasjonskompetanse hos helsepersonell. Verktøy for tidlig oppdagelse av forverret tilstand brukes i stadig økende grad, også utenfor sykehus, men kunnskapsgrunnlaget i dag er primært basert på forskning fra sykehuspopulasjonen.
Hensikt: Identifisere og beskrive forskning på verktøy for tidlig oppdagelse av forverret tilstand hos eldre pasienter utenfor sykehus.
Metode: Kartleggingsoversikten fulgte Joanna Briggs Institutes metodologi for kartleggingsoversikter. Vi publiserte protokollen for studien i Open Science Framework. Et systematisk litteratursøk i relevante og utvalgte databaser i mai 2021 danner grunnlaget for oversikten. To personer screenet alle artiklene uavhengig av hverandre etter forhåndsdefinerte inklusjons- og eksklusjonskriterier. Vi har trukket ut data i henhold til forskningsspørsmålet og har summert og presentert dem i tabeller og grafer.
Resultater: I alt har vi inkludert 45 studier i kartleggingsoversikten. Det har vært en markant økning i studier som undersøker bruk av verktøy for tidlig oppdagelse av forverret tilstand de siste årene. Et fåtall av disse studiene har studert eldre særskilt, og de fleste omhandler ambulansetjenester. Hele 14 ulike verktøy for tidlig oppdagelse av forverret tilstand er identifisert i de inkluderte studiene, også kalt EWS (Early Warning Score). De mest brukte verktøyene er MEWS, NEWS og NEWS2. Kvalitative studier om bruk av slike verktøy kan tyde på at de er nyttige som beslutningsstøtte for helsepersonell som skal vurdere forverring av pasienters tilstand.
Konklusjon: Denne studien viser en stor økning i antallet studier som omhandler verktøy for tidlig oppdagelse av forverret tilstand utenfor sykehus de senere årene. Dette reflekterer trolig både økt oppmerksomhet på og behov for slike verktøy som beslutningsstøtte. Likevel er det overraskende få studier som har fokusert særskilt på eldre og kommunale helsetjenester. Det er et paradoks når verktøyene anbefales brukt i nasjonale faglige råd med svakt kunnskapsgrunnlag. Vi anbefaler å bruke slike verktøy, og det eksisterer et kunnskapshull som bør prioriteres.
Referer til artikkelen
Steinseide E, Potrebny T, Ciliska D, Graverholt B. Verktøy for tidlig oppdagelse av forverring hos eldre utenfor sykehus – en systematisk kartleggingsoversikt. Sykepleien Forskning. 2022;17(88361):e-88361. DOI: 10.4220/Sykepleienf.2022.88361
Eldre pasienter med underliggende sykdom er en sårbar gruppe som er ekstra utsatt for forverring av sin somatiske tilstand (1). De eldre har ofte uspesifikke symptomer ved utvikling av sykdom, og symptomene kan komme fra helt andre organsystemer enn der den akutte sykdommen finnes (2).
I tillegg blir ofte akutt sykdom hos eldre preget av funksjonstap, noe som kan bli mistolket som et pleieproblem og ikke sykdom (1). Alvorlig sykdom kan utvikle seg raskt hos eldre og krever observasjonskompetanse for å tidlig kunne identifisere forverring av en tilstand (2).
Mangel på sådan kan føre til at tilstander og sykdommer ikke blir diagnostisert, noe som utgjør en alvorlig risiko for nedsatt pasientsikkerhet. Akutt funksjonssvikt hos eldre kan være uoppdaget, og tegn på alvorlig sykdom kan i verste fall overses (1).
Hos eldre er det derfor ekstra viktig med høy observasjonskompetanse som et ledd i pasientsikkerhetsarbeid. Det er i tråd med kommunehelsetjenestens ansvar for å levere tjenester som er trygge, og som fortrinnsvis bygger på kunnskapsbaserte retningslinjer (3–5).
En stor andel av ansatte i kommunehelsetjenesten er ufaglærte, og sykepleiere er ofte alene med ansvaret for mange pasienter (6). Å kunne observere og vurdere kritisk sykdom er en viktig kunnskap hos sykepleiere (7), og de skal kunne reagere og handle når pasientene får forverret tilstand (8).
Usikkerhet rundt kliniske observasjoner og vurderinger er blant annet bekreftet i oversikten til Preston og Flynn (8). En kartlegging av grunnleggende observasjonskompetanse i norsk kommunehelsetjeneste av Bing-Jonsson og medarbeidere (9) viser at kompetansen til helsepersonell i kommunehelsetjenesten er varierende når det gjelder observasjon, grunnleggende kartlegging og måling av vitale mål.
Fra sykehus vet vi at en tredel av dødsfall kunne vært forebygget fordi de skjer på bakgrunn av mangelfull klinisk monitorering av pasientene (10). Omtrent halvparten av pasientskader oppstår i kommunehelsetjenesten, hvor eldre utgjør den største pasientgruppen (4).
Eldre pasienter er en heterogen gruppe som består av alt fra hjemmeboende med mindre medisinske utfordringer til skrøpelige sykehjemsbeboere med flere diagnoser og funksjonssvikt (11).
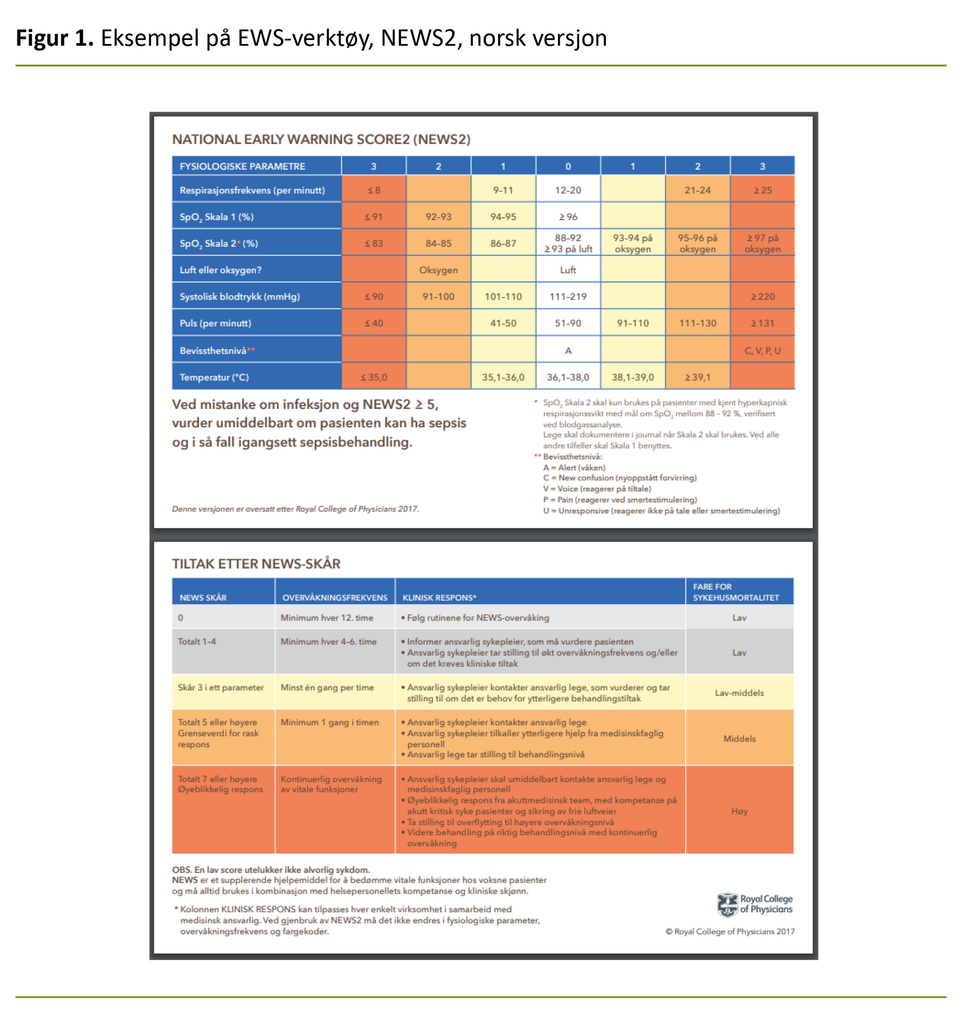
I Norge er kanskje National Early Warning Score (NEWS/NEWS2) (figur 1) og Modified Early Warning Score (MEWS) de mest kjente og benyttede verktøyene for tidlig oppdagelse av forverret tilstand. På engelsk brukes fellesbetegnelsen Early Warning Score (EWS).
EWS-verktøy er utviklet for å standardisere og kvalitetssikre oppdagelse av og respons på klinisk forverret tilstand (12). Eldre pasienter får ofte atypiske symptomer, og overvåkning av eventuelle endringer i vitale tegn er essensielt for tidlig oppdagelse av forverret tilstand (2).
Felles for disse verktøyene er at vanlige observasjoner av fysiologiske parametere som blodtrykk, puls, respirasjonsfrekvens og temperatur utgjør grunnlaget for en skår etter et standardisert oppsett.
Ulike skårer utløser forskjellig respons, som videre fungerer som beslutningsstøtte for helsepersonell (13). Å bruke EWS til støtte for klinisk vurdering er anerkjent internasjonalt og nasjonalt og anbefales i retningslinjer og faglige råd (14–16).
Tidligere forskning på bruk av verktøyet utenfor sykehus er i hovedsak gjort på pasientutfall i ambulanser. Eldre i andre settinger, for eksempel sykehjem, er sjeldnere beskrevet (13, 14, 17, 18). Det vil være nyttig å få en oversikt over hvilke aspekter rundt denne tematikken som er belyst av forskning, og hvilke som ikke er det.
Hensikten med studien
Hensikten med denne kartleggingsoversikten er å identifisere, fremstille og beskrive forskning på verktøy for tidlig oppdagelse av forverret tilstand hos eldre utenfor sykehus.
Metode
Protokollen for denne kartleggingsoversikten ble publisert på den åpne plattformen Open Science Framework i august 2020 (19). Vi gjennomførte studien i tråd med Joanna Briggs Institutes metodologi for kartleggingsoversikter (20), som igjen bygger på Arksey og O'Malleys (21) mye brukte rammeverk.
Metoden egner seg for å fremskaffe en profil over eksisterende forskningslitteratur på et gitt tema og identifisere eventuelle kunnskapshull. Gjennom ni eksplisitte metodiske trinn kartla og fremstilte vi en oversikt over forskning på bruk av verktøy for tidlig oppdagelse av forverret tilstand hos eldre utenfor sykehus.
Inklusjonskriterier
Vi brukte rammeverket Patient Context Concept (PCC) for å spesifisere kartleggingsoversiktens populasjon, kontekst og konsept (20). Disse elementene reflekteres i kartleggingsoversiktens inklusjonskriterier, som videre er grunnlaget for et systematisk litteratursøk.
Vi inkluderte studier hvor populasjonen (P) var over 65 år. Vi inkluderte også studier som omhandlet personer over 65 år, men som ikke var begrenset til det. I de tilfellene forsøkte vi å hente ut data relatert til eldre.
Videre inkluderte vi studier hvis de var gjennomført i kontekster (C) utenfor sykehus, for eksempel sykehjem, hjemmebaserte tjenester, legesenter eller ambulanse. Hvis vi fant studier som foregikk både utenfor og i sykehus, inkluderte vi dem om de inneholdt vitale målinger utenfor sykehus.
Ut over disse inkluderte vi kvalitative studier der helsepersonell var definert som studiepopulasjon dersom helsepersonellet arbeidet med eldre pasienter, som sykehjem og hjemmesykepleie.
Konseptet (C) i denne kartleggingsoversikten er verktøy for tidlig oppdagelse av forverret tilstand. Vi gjorde ingen avgrensing til bestemte verktøy, men det måtte dreie seg om et verktøy for å oppdage klinisk forverret tilstand som baserer seg på vitale mål. Vi inkluderte alle typer primærstudier uavhengig av studiedesign.
Litteratursøk
Vi utførte et tredelt og iterativt litteratursøk (20) mellom 1. august og 30. oktober 2020 og en oppdatering av søk 27. mai 2021. Tredelingen innebar først et innledende søk i to databaser med påfølgende analyse av titler og sammendrag i den hensikt å identifisere ytterligere relevante søketermer.
Deretter gjennomførte vi hovedsøket i følgende databaser: Medline Ovid, Cinahl Ebsco, Cochrane Library Central, Epistemonikos og Embase Ovid. For hver database utarbeidet vi en egen søkestrategi i tråd med kartleggingsoversikten PCC.
Vi gjorde ingen avgrensinger for publiseringsår eller språk. Alle søkene ble kvalitetssikret av en universitetsbibliotekar. I tillegg gjennomførte vi et håndsøk, der vi gikk igjennom alle referanselister på inkluderte studier samt referanselister på relevante systematiske oversikter.
Videre søkte vi etter pågående studier i Prospero, ClinicalTrials.gov, WHO International Clinical Trials Registry Platform, EU Clinical Trials Register og The Open Science Framework (OSF). For å identifisere relevant litteratur som ikke finnes i databasene, søkte vi i tillegg i Google Scholar og OpenGrey. Se komplette søkestrategier i vedlegg 1.
Utvelgelse av studier
To personer screenet hele resultatet fra litteratursøket uavhengig av hverandre (EGS, BG og TP). I første omgang vurderte vi tittel og abstrakt opp mot inklusjonskriteriene.
I tilfeller der det var tydelig at en artikkel oppfylte inklusjonskriteriene, eller hvis det var uklart, innhentet vi disse i fulltekst, og to personer vurderte dem for inklusjon uavhengig av hverandre. Uenigheter løste vi gjennom diskusjoner eller ved å konsultere en tredjeperson (DC).
Datasamling og analyse
Vi utviklet et datasamlingsskjema på bakgrunn av inklusjonskriteriene med følgende variabler: referanse, opprinnelsesland, hensikt, studiedesign, studiepopulasjon, klinisk populasjon, alder klinisk populasjon, hvilket verktøy som ble brukt, og i hvilken situasjon, eventuelle pasientutfall, hvordan valideringsstudiene ble gjennomført, og tema i kvalitative studier.
Datasamlingsskjemaet ble pilotert på fem artikler av to personer uavhengig av hverandre. Deretter ble data fra de resterende inkluderte studiene trukket ut og samlet av en person (EGS) og kontrollert av en andreperson (BG og TP).
Vi brukte enkle deskriptive statistiske analyser (frekvenser, andeler og prosenter) for å beskrive de inkluderte studiene med tanke på kontekst, studiedesign og studiepopulasjon. For å vise hvilke verktøy som var brukt, og hvor ofte, benyttet vi diagram.
Resultatene fra kvalitative studier har vi beskrevet på bakgrunn av en enkel innholdsanalyse av temaene vi identifiserte i studiene.
Etikk
Dette er en kartleggingsoversikt og krever ikke særlig godkjenning av en etisk komité eller personvernombud.
Resultater
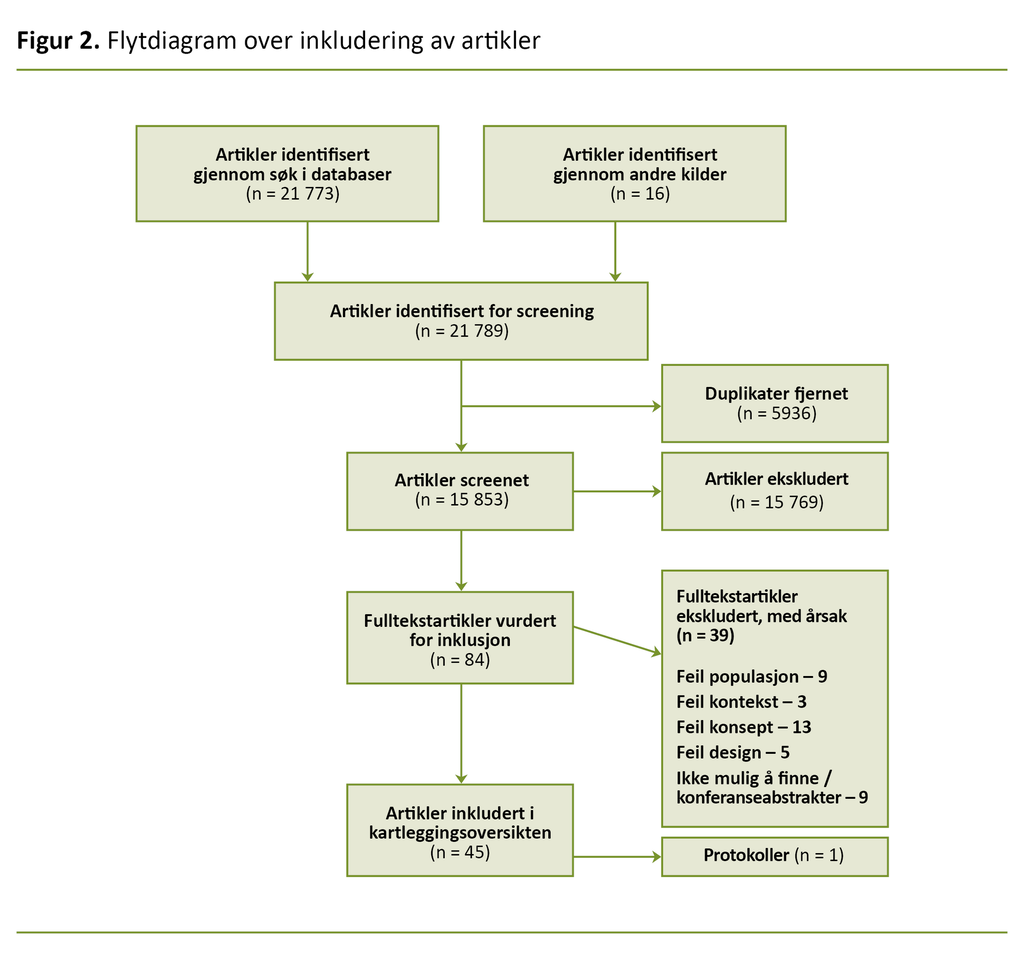
Totalt identifiserte vi 15 853 unike referanser gjennom litteratursøket. Vi endte til slutt opp med å inkludere 45 artikler etter at 84 artikler var lest i fulltekst (figur 2). En av disse var en protokoll over pågående studier (22).
De inkluderte studiene hadde i stor grad opprinnelse i europeiske land (n = 39), i hovedsak Storbritannia (n = 16). Fem av studiene var gjennomført i Asia og én i Nord-Amerika. Totalt 89 prosent av studiene er gjennomført i 2015 eller senere.
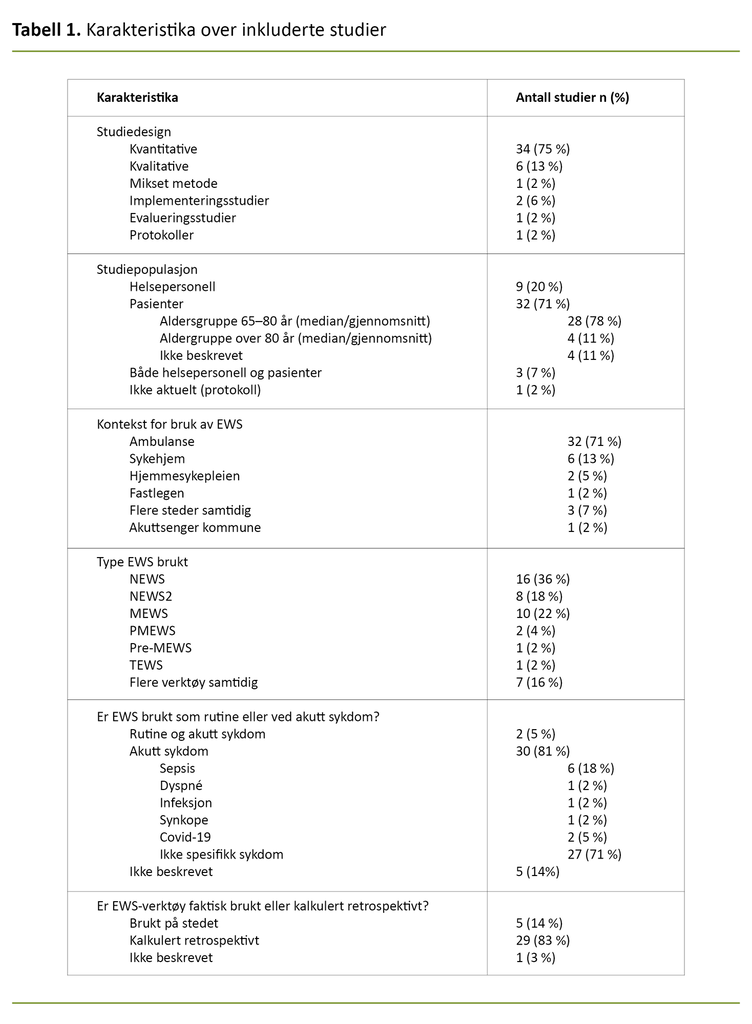
Videre hadde en stor andel av de inkluderte studiene ulike kvantitative design (n = 34), alle var observasjonsstudier, og ingen var eksperimentelle studier. De kvalitative studiene (n = 6) baserte seg på intervjuer, enten som fokusgruppeintervjuer eller individuelle intervjuer. Karakteristika over inkluderte studier har vi beskrevet i detalj i tabell 1.
Kun et lite antall av studiene hadde utelukkende inkludert eldre (n = 6) (23–28). Likevel var gjennomsnittsalderen (og/eller medianalderen) over 65 år i alle de inkluderte studiene. Noen få hadde en median- eller gjennomsnittsalder på over 80 år (n = 4) (26–29). Enkelte studier fokuserte utelukkende på sepsis (27, 30–35), mens de fleste studiene ikke var begrenset til en diagnose.
Den største andelen av studiene var gjennomført i ambulansetjenesten (n = 25). En mindre andel (n = 6) var gjennomført i sykehjem (23, 25, 26, 28, 36), på fastlegekontor (n = 1) (37), akuttsenger i kommunen (38) og to i hjemmesykepleien (n = 2) (29, 39).
Tre av studiene foregikk på tvers av ulike settinger (32, 40, 41). De kvalitative studiene og implementeringsstudiene hadde helsepersonell som studiepopulasjon.
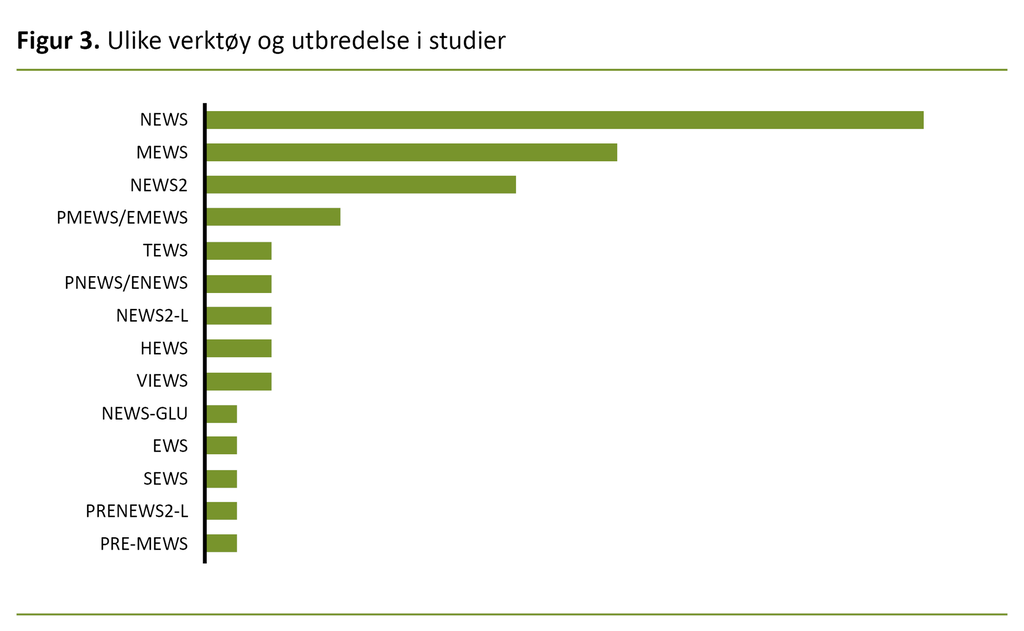
Vi identifiserte 14 ulike EWS-verktøy
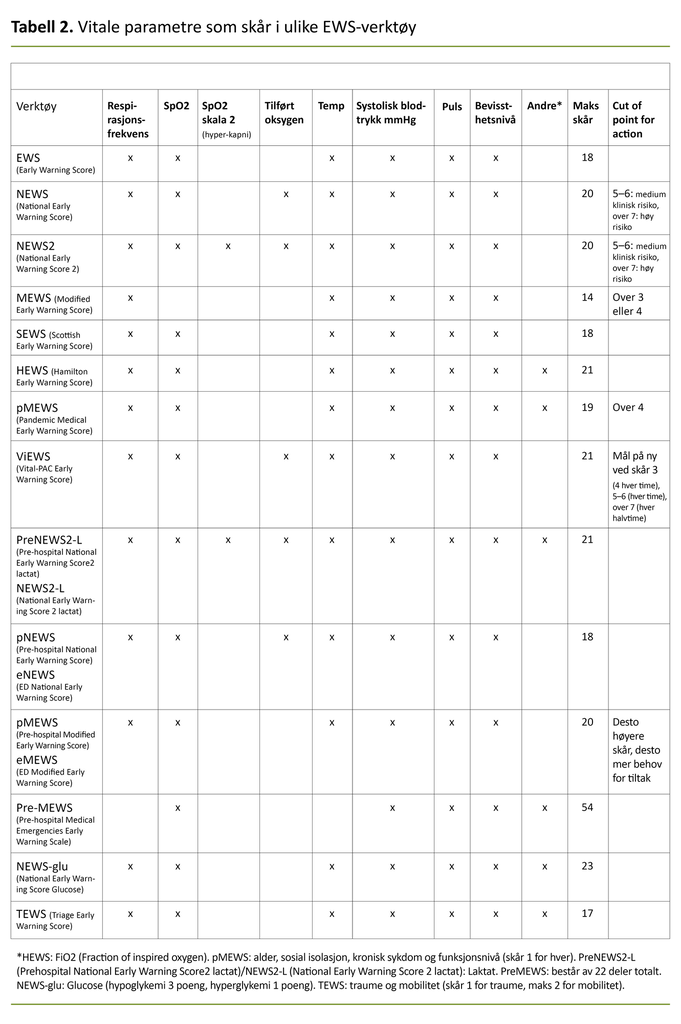
Vi identifiserte totalt 14 ulike EWS-verktøy, og mer enn halvparten av artiklene omhandlet NEWS eller NEWS2 (figur 3 og tabell 2). Kun et fåtall av studiene omhandlet faktisk bruk av verktøy (n = 5). I de fleste tilfellene var data hentet ut retrospektivt (24, 25, 27, 30, 31, 33–35, 42–62).
Langt på vei fant vi at EWS-skår ble gjort på klinisk indikasjon, altså når det var mistanke om akutt sykdom. Vi identifiserte kun én valideringsstudie, som undersøkte reliabilitet og validitet, for instrumentet pre-MEWS (63).
Det vanligste pasientutfallet i de kvantitative studiene var mortalitet (n = 23). Innleggelse på sykehus eller intensivavdeling (n = 15) og ytterligere forverring og komplikasjoner (n = 8) var også mye undersøkte utfall. Noen få studier hadde undersøkt om bruk av EWS påvirket tilsyn av lege (n = 2) og reinnleggelse (n = 2).
De kvalitative studiene fokuserte på erfaringer med bruk av EWS som beslutningsstøtte og i kommunikasjon. Temaer som trygghet og støtte i faglige vurderinger ble hyppigst rapportert (n = 7). Andre temaer som ble løftet frem i den kvalitative forskningen, var implementering, opplæring og utfordringer rundt det å bruke EWS riktig (29, 32).
Tabeller over de inkluderte studier har vi organisert etter henholdsvis kvantitative studier (vedlegg 2) (24–28, 30, 31, 33–35, 38, 42–62, 64–66), kvalitative studier (vedlegg 3) (23, 28, 36, 39–41, 67) og implementerings- og valideringsstudier (vedlegg 4) (29, 32, 63) samt protokoller (22).
I tillegg har vi laget en oversikt over artikler som vi leste i fulltekst og deretter ekskluderte, der vi oppgir årsaken til ekskluderingen (vedlegg 5).
Diskusjon
I denne kartleggingsoversikten har vi identifisert og beskrevet forskningsbasert kunnskap om bruk av verktøy for tidlig oppdagelse av forverret tilstand hos eldre utenfor sykehus. Vi identifiserte 14 ulike EWS-verktøy, alle med små variasjoner, og MEWS, NEWS og NEWS2 var mest brukt.
Forskningen på feltet består hovedsakelig av kvantitative observasjonsstudier og ellers noen kvalitative studier og et par implementeringsstudier. Det er en klar trend av økende forskning på EWS de senere årene, men fremdeles er det begrenset hvor mye som er relevant for eldre pasienter utenfor sykehus. Få studier er gjennomført på sykehjem og i hjemmetjenesten.
Det finnes lite forskning på EWS blant eldre
Det finnes overraskende lite forskning på bruk av EWS blant eldre og fra settinger hvor sykepleiere møter sårbare eldre, som sykehjem og hjemmebaserte tjenester.
Her i Norge har Helsedirektoratet anbefalt å bruke NEWS2 i de kommunale helse- og omsorgstjenestene siden 2018 gjennom pasientsikkerhetsprogrammet (5), og nylig ble tiltakspakken i «I trygge hender 24/7» videreført som nasjonale faglige råd (15).
Det betyr at nasjonale helsemyndigheter gir anbefalinger på det som synes å være et svakt kunnskapsgrunnlag. Likevel viser den økende trenden av studier at det er stor oppmerksomhet på å fremskaffe kunnskap om disse verktøyene, som igjen kan gjenspeile økt bruk og et tilsynelatende stort behov for verktøyene.
Alternativet til slike verktøy er skjønnsmessige vurderinger, manglende beslutningsgrunnlag og trolig upresis kommunikasjon om pasientens tilstand. Med bakgrunn i at observasjonskunnskapen til helsepersonell kan være mangelfull (9), vil det sannsynligvis være tryggere å bruke et slikt verktøy, vel å merke så lenge det brukes riktig (14).
Dessuten er kunnskapsgrunnlaget for å bruke EWS i spesialisthelsetjenesten tydeligere (13, 14, 68, 69), og muligens kan dette brukes indirekte som grunnlag også utenfor sykehus. For eksempel viser flere studier fra spesialisthelsetjenesten at det er effekt av å bruke EWS på pasientutfall som mortalitet (14, 68, 69).
Det er et åpenbart kunnskapshull som vedvarer
Denne kartleggingsoversikten viser at kunnskapsgrunnlaget for å anbefale bruk av EWS utenfor sykehus er svakt. Vi har identifisert et åpenbart kunnskapshull som bør prioriteres. Behovet for forskning har vært påpekt i tidligere systematiske oversikter (17, 18), men vår oversikt viser at kunnskapshullet vedvarer.
Denne kartleggingsoversikten viser at kunnskapsgrunnlaget for å anbefale bruk av EWS utenfor sykehus er svakt.
Særlig mangler vi studier med robuste prospektive design for å vurdere effektene av å bruke EWS prehospitalt (17, 18), som er et premiss for å jobbe kunnskapsbasert (70). Likevel er det altså en generell økning i antall studier som er gjennomført utenfor sykehus, noe som kan reflektere interesse og behov for verktøyene.
Vi identifiserte hele 14 ulike verktøy, og det er et spørsmål hvilket av disse som er best egnet til å bruke på eldre utenfor sykehus. I Norge og England anbefaler nasjonale myndigheter gjennom retningslinjer og faglige råd å bruke NEWS2 (12, 15).
Studiene har ikke sammenliknet ulike EWS-verktøy
De inkluderte studiene har i liten grad sammenliknet de ulike EWS-verktøyene og bidrar dermed i liten grad med kunnskap om hvilket verktøy som er «det beste». Det er også utenfor en kartleggingsoversikts hensikt.
Antallet verktøy er en oppgang fra funn i tidligere systematiske oversikter (17, 18). Downey og Tahir (14) anbefaler at det samme verktøyet bør brukes for å skape et universelt språk på kryss av kontekster.
Samtidig er det viktig å vurdere om de samme verktøyene faktisk kan brukes på skrøpelige eldre med kompliserte sykdomsbilder og mange diagnoser utenfor sykehus og på yngre voksne på sykehus eller i andre kontekster.
EWS-verktøy har blitt kritisert for at de brukes i andre settinger og for andre populasjoner enn hva de var utviklet for (71). Dette er i liten grad vurdert i forskningslitteraturen.
EWS kan ikke erstatte helsepersonells kliniske vurdering
Fra den kvalitative delen av forskningen og fra implementeringsstudiene ser vi at helsepersonell uttrykker et behov for beslutningsstøtte i situasjoner som EWS skal avhjelpe med, og at slike verktøy er nyttige og relevante. Samtidig kommer det frem at EWS aldri kan erstatte helsepersonells kliniske vurderinger (23, 28, 36, 39, 67).
En av innvendingene mot EWS er nettopp at verktøyet kan oppfattes som erstatning for, og ikke støtte til, en helhetlig klinisk vurdering (71). Det bekreftes av Jeppestøl og Kirkevold (39), som løfter frem viktigheten av å kjenne pasientene når en bruker verktøyet.
Helsepersonell uttrykker et behov for beslutningsstøtte i situasjoner som EWS skal avhjelpe med.
Sykepleierne er en viktig ressurs, og kompetansen deres bør brukes riktig og heves der det er behov for det. Observasjonskompetanse er viktig for å vurdere somatiske utfordringer hos eldre med komplekse sykdomsbilder (2), og behovet for grunnleggende observasjonskompetanse er tidligere identifisert av Bing-Jonsson og medarbeidere (9).
Verktøyene kan gi god støtte, men fordrer rett bruk og rett kompetanse. Det er derfor viktig å ikke undervurdere implementeringen av slike verktøy (15). Det medfører en systematisk og planlagt prosess, der det også er nødvendig å fokusere på holdbarhet over tid (72).
Et stort behov for beslutningsstøtte synes å være dokumentert gjennom kartleggingsoversikten, samtidig som litteraturen viser utfordringer rundt kompetanse, opplæring og implementering av EWS-verktøy.
Implikasjoner
De kvalitative studiene i denne kartleggingsoversikten belyser fordeler ved å bruke EWS, og det er særlig positivt for beslutningsstøtte og kommunikasjon. Samtidig er målrettet opplæring viktig for rett anvendelse av verktøyene, noe som ofte er et sykepleieansvar i de kommunale helse- og omsorgstjenestene.
Det er en rekke kunnskapshull knyttet til bruken av EWS i sykehjem, i hjemmetjenesten og hos eldre generelt. Et av områdene hvor det foreligger grunnlag for oppdatering av og spissede systematiske oversikter, er i ambulansetjenesten.
Det er en rekke kunnskapshull knyttet til bruken av EWS i sykehjem, i hjemmetjenesten og hos eldre generelt.
Videre er det et markant behov for studier med prospektive forskningsdesign, som kan evaluere effekten av EWS rettet mot eldre pasienter i sykehjem og hjemmetjenesten. Det ville også vært nyttig å vite hvilket av de 14 verktøyene som egner seg best til tidlig oppdagelse av forverret tilstand hos eldre utenfor sykehus.
Metodiske styrker og begrensninger
Systematiske kartleggingsoversikter har til hensikt å identifisere det som eksisterer av forskning på et bestemt felt, i dette tilfellet verktøy for tidlig oppdagelse av forverret tilstand hos eldre utenfor sykehus. Metoden er denne oversiktens største styrke, nemlig at den gir et overblikk over det som eksisterer av forskning på feltet.
Det er likevel viktig å påpeke at det ligger utenfor en kartleggingsoversikts rammer å vurdere de inkluderte studienes metodiske kvalitet, herunder risikoen for systematiske skjevheter. Dette må det tas høyde for når resultatene fra denne kartleggingsoversikten tolkes og brukes.
En styrke ved kartleggingsoversikten er protokollen vi publiserte forut for oppstarten av oversikten, noe som reduserer risikoen for seleksjonsskjevhet i studien. En annen styrke er det brede og iterative litteratursøket som danner grunnlaget for datasamlingen, som også er kvalitetssikret av en universitetsbibliotekar.
Vi må likevel presisere at det alltid er en viss fare for at studier kan ha unnsluppet søket. Likeså er det en styrke at utvelgelsen av studier er gjort av to personer uavhengig av hverandre.
En svakhet ved metoden vår er at bare for 15 av de 45 inkluderte studiene var det to personer som uavhengig av hverandre trakk ut data fra artiklene. Imidlertid piloterte vi prosessen for å trekke ut data i forkant, siden vi fant godt samsvar da to personer gikk gjennom 15 artikler.
Konklusjon
Denne kartleggingsoversikten viser at forskning på verktøy for tidlig oppdagelse av forverret tilstand er i stor vekst både i Norge og internasjonalt. Trenden er imidlertid en annen når det gjelder bruk i typiske kommunale helsetjenestesettinger som hjemmetjeneste og sykehjem.
Vi vet fremdeles lite om hva verktøyene bidrar til i disse settingene, noe som er et paradoks tatt i betraktning at verktøyene inngår i nasjonale faglige råd. Flest studier om EWS blant eldre er fra ambulansetjenesten.
Den generelle økningen i forskning på EWS reflekterer trolig flere faktorer, hvor den viktigste kanskje er et reelt og stort behov for standardiserte verktøy som kan nyttes som beslutningsstøtte i situasjoner med komplekse vurderinger.
Fremtidig forskning på bruk av EWS hos eldre utenfor sykehus bør skje med mer robuste, prospektive og kontrollerte studiedesign som kan si oss noe om nytte for pasientgruppen og helsepersonell i kommunehelsetjenesten.
Studien er en del av IMPAKT-prosjektet, som er finansiert av Norges forskningsråd (256569) (73).
Studien er gjennomført som en masteroppgave ved master i kunnskapsbasert praksis i helsefag ved Høgskulen på Vestlandet. Takk til universitetets bibliotekar Gøril Tvedten Jorem for verdifull støtte i utforming og fagfellevurdering av litteratursøket.
Referanser
1. Wyller TB. Geriatri. En medisinsk lærebok. 3. utgave. Oslo: Gyldendal; 2020.
2. Nickel C, Bellou A, Conroy S. Geriatric emergency medicine. Cham: Springer International Publishing; 2017.
3. Forskrift 28.10.2016 nr. 1250 om ledelse og kvalitetsforbedring i helse- og omsorgstjenesten. Tilgjengelig fra: https://lovdata.no/dokument/LTI/forskrift/2016-10-28-1250 (nedlastet 03.02.2022).
4. Helsedirektoratet. Nasjonal handlingsplan for pasientsikkerhet og kvalitetsforbedring 2019–2023. Oslo: Helsedirektoratet; 2021. Tilgjengelig fra: https://www.helsedirektoratet.no/tema/pasientsikkerhet-og-kvalitetsforbedring (nedlastet 03.02.2022).
5. Helsedirektoratet. Pasientsikkerhetsprogrammet i trygge hender 24/7. Oslo: Helsedirektoratet; 2019. Tilgjengelig fra: https://www.itryggehender24-7.no/om-i-trygge-hender-24-7 (nedlastet 03.03.2021).
6. Flodgren G, Bidonde J, Berg RC. Konsekvenser av en høy andel ufaglærte på kvalitet og pasientsikkerhet i helse‐ og omsorgstjenestene: en systematisk oversikt. Oslo: Folkehelseinstituttet; 2017.
7. Stanyon MR, Goldberg SE, Astle A, Griffiths A, Gordon AL. The competencies of registered nurses working in care homes: a modified Delphi study. Age Ageing. 2017;46(4):582–8. DOI: 10.1093/ageing/afw2244
8. Preston RM, Flynn DJ. Observations in acute care: evidence-based approach to patient safety. Br J Nurs. 2010;19(7):442–7. DOI: 10.12968/bjon.2010.19.7.47446
9. Bing-Jonsson PC, Hofoss D, Kirkevold M, Bjørk IT, Foss C. Sufficient competence in community elderly care? Results from a competence measurement of nursing staff. BMC Nurs. 2016 Jan 14;15(1):5. DOI: 10.1186/s12912-016-0124-z
10. Hogan H, Healey F, Neale G, Thomson R, Vincent C, Black N. Preventable deaths due to problems in care in English acute hospitals: a retrospective case record review study. London: BMJ Publishing Group Ltd; 2012.
11. Helsedirektoratet. Kommunale helse- og omsorgstjenester 2019. Statistikk fra Kommunalt pasient- og brukerregister (IPLOS). Oslo: Helsedirektoratet; 2019.
12. Royal College of Physicians. National Early Warning Score (NEWS) 2. Standardising the assessment of acute-illness severity in the NHS. London: Royal College of Physicians; 2017.
13. Le Lagadec MD, Dwyer T. Scoping review: the use of early warning systems for the identification of in-hospital patients at risk of deterioration. Australian Critical Care. 2017;30(4):211–8. DOI: 10.1016/j.aucc.2016.10.003
14. Downey CL, Tahir W, Randell R, Brown JM, Jayne DG. Strengths and limitations of early warning scores: a systematic review and narrative synthesis. Int J Nurs Stud. 2017;76:106–19. DOI: 10.1016/j.ijnurstu.2017.09.003
15. Helsedirektoratet. Tidlig oppdagelse og rask respons ved forverret somatisk tilstand. Oslo: Helsedirektoratet; 2020. Tilgjengelig fra: https://www.helsedirektoratet.no/faglige-rad/tidlig-oppdagelse-og-rask-respons-ved-forverret-somatisk-tilstand#referere (nedlastet 01.06.2021).
16. National Institute for Health and Care Excellence (NICE). Sepsis: recognition, diagnosis and early management. NICE guideline [NG51]. London: NICE; 2016 [oppdatert 13.09.2017]. Tilgjengelig fra: https://www.nice.org.uk/guidance/NG51 (nedlastet 24.04.2021).
17. Williams TA, Tohira H, Finn J, Perkins GD, Ho KM. The ability of early warning scores (EWS) to detect critical illness in the prehospital setting: a systematic review. Resuscitation. 2016;102:35–43. DOI: 10.1016/j.resuscitation.2016.02.011
18. Patel R, Nugawela MD, Edwards HB, Richards A, Le Roux H, Pullyblank A, et al. Can early warning scores identify deteriorating patients in pre-hospital settings? A systematic review. Resuscitation. 2018;132:101–11. DOI: 10.1016/j.resuscitation.2018.08.028
19. Steinseide E, Graverholt B, Espehaug B, Ciliska D. The use of early warning scores (EWS) in older people in nonhospitalized settings. Protocol for a scoping review. Charlottesville: Center for Open Science; 2020. Tilgjengelig fra: https://osf.io/5rg78/ (nedlastet 17.08.2020).
20. Peters MDJ, Godfrey C, McInerney P, Munn Z, Tricco AC, Khalil, H. Chapter 11: Scoping Reviews [oppdatert 02.07.2020; sitert 10.02.2021]. I: Aromataris E, Munn Z, red. JBI Manual for Evidence Synthesis. Tilgjengelig fra: https://jbi-global-wiki.refined.site/space/MANUAL/3283910770/Chapter+11%3A+Scoping+reviews (nedlastet 10.02.2021).
21. Arksey H, O'Malley L. Scoping studies: towards a methodological framework. International Journal of Social Research Methodology. 2005;8(1):19–32. DOI: 10.1080/1364557032000119616
22. Graverholt B. Tailoring an intervention to the educational needs of healthcare professionals in nursing homes: does it have an impact on the use of an early warning score? Bergen: ISRCTN registry; 2020. Tilgjengelig fra: https://www.isrctn.com/ISRCTN12437773 (nedlastet 03.02.2022).
23. Steinsheim G, Malmedal W. Tidlig oppdagelse av forverret tilstand. Tidsskrift for omsorgsforskning. 2020;6(02):10–22. DOI: 10.18261/issn.2387-5984-2020-02-02
24. Mitsunaga T, Hasegawa I, Uzura M, Okuno K, Otani K, Ohtaki Y, et al. Comparison of the National Early Warning Score (NEWS) and the Modified Early Warning Score (MEWS) for predicting admission and in-hospital mortality in elderly patients in the pre-hospital setting and in the emergency department. Peerj. 2019;7:e6947. DOI: 10.7717/peerj.6947
25. Stow D, Barker R, Matthews F, Hanratty B. National Early Warning Scores and covid-19 deaths in care homes: an ecological time series study. Innovation in Aging. 2020;4(Suppl 1):962. DOI: 10.1136/bmjopen-2020-045579
26. Barker RO, Stocker R, Russell S, Roberts A, Kingston A, Adamson J, et al. Distribution of the National Early Warning Score (NEWS) in care home residents. Age Ageing. 2019;49(1):141–5. DOI: 10.1093/ageing/afz130
27. Camm CF, Hayward G, Elias TCN, Bowen JST, Hassanzadeh R, Fanshawe T, et al. Sepsis recognition tools in acute ambulatory care: associations with process of care and clinical outcomes in a service evaluation of an Emergency Multidisciplinary Unit in Oxfordshire. BMJ Open. 2018;8(4):e020497. DOI: 10.1136/bmjopen-2017-020497
28. Hodgson P, Cook G, Thompson J, Abbott-Brailey H. Assessment and clinical decision making of the acutely ill older care home resident: implementation of NEWS in Gateshead care homes. Final report. Newcastle: Northumbria University; 2017.
29. Ammitzboll O, Maarslet L. Early Warning Score in primary care in Denmark. Ugeskrift for laeger. 2014;176(41).
30. Bayer O, Schwarzkopf D, Stumme C, Stacke A, Hartog CS, Hohenstein C, et al. An early warning scoring system to identify septic patients in the prehospital setting: the PRESEP score. Academic Emergency Medicine. 2015;22(7):868–71. DOI: 10.1111/acem.12707
31. Jouffroy R, Saade A, Ellouze S, Carpentier A, Michaloux M, Carli P, et al. Prehospital triage of septic patients at the SAMU regulation: comparison of qSOFA, MRST, MEWS and PRESEP scores. Am J Emerg Med. 2018;36(5):820–4. DOI: 10.1016/j.ajem.2017.10.030
32. Pullyblank A, Tavare A, Little H, Redfern E, le Roux H, Inada-Kim M, et al. Implementation of the national early warning score in patients with suspicion of sepsis: evaluation of a system-wide quality improvement project. British Journal of General Practice. 2020;70(695):E381–8. DOI: 10.3399/bjgp20X709349
33. Lane DJ, Wunsch H, Saskin R, Cheskes S, Lin S, Morrison LJ, et al. Screening strategies to identify sepsis in the prehospital setting: a validation study. Cmaj. 2020;192(10):E230–9. DOI: 10.1503/cmaj.190966
34. Usul E, Korkut S, Kayipmaz AE, Halici A, Kavalci C. The role of the quick sequential organ failure assessment score (qSOFA) and modified early warning score (MEWS) in the pre-hospitalization prediction of sepsis prognosis. Am J Emerg Med. 2021;41:158–62. DOI: 10.1016/j.ajem.2020.09.049
35. Hargreaves DS, de Carvalho JLJ, Smith L, Picton G, Venn R, Hodgson LE. Persistently elevated early warning scores and lactate identifies patients at high risk of mortality in suspected sepsis. Eur J Emerg Med. 2020;27(2):125–31. DOI: 10.1097/MEJ.0000000000000630
36. Russell S, Stocker R, Barker RO, Liddle J, Adamson J, Hanratty B. Implementation of the National Early Warning Score in UK care homes: a qualitative evaluation. The British Journal of General Practice. 2020 okt. 29;70(700);e793–e800. DOI: 10.3399/bjgp20X713069
37. Scott LJ, Redmond NM, Garrett J, Whiting P, Northstone K, Pullyblank A. Distributions of the National Early Warning Score (NEWS) across a healthcare system following a large-scale roll-out. Emergency Medicine Journal. 2019;36(5):287–92. DOI: 10.1136/emermed-2018-208140
38. Hernes SK, Baste V, Krokmyrdal KA, Todnem SL, Ruths S, Johansen IH. Associations between characteristics of the patients at municipal acute bed unit admission and further transfer to hospital: a prospective observational study. BMC Health Services Research. 2020;20(1):963. DOI: 10.1186/s12913-020-05823-0
39. Jeppestøl K, Kirkevold M, Bragstad LK. Applying the Modified Early Warning Score (MEWS) to assess geriatric patients in home care settings: a qualitative study of nurses’ and general practitioners’ experiences. 2019 okt. DOI: 10.21203/rs.2.16666/v2
40. Brangan E, Banks J, Brant H, Pullyblank A, Le Roux H, Redwood S. Using the National Early Warning Score (NEWS) outside acute hospital settings: a qualitative study of staff experiences in the West of England. BMJ Open. 2018;8(10):e022528. DOI: 10.1136/bmjopen-2018-022528
41. Sletner A, Halvorsrud L. Opplæring i systematisk observasjon (ALERT) i kommunehelsetjenesten og betydningen for jobbtilfredshet. Sykepleien Forskning. 2020;15(80410):e-80410. DOI: 10.4220/Sykepleienf.2020.80410
42. Challen K, Walter D. Physiological scoring: an aid to emergency medical services transport decisions? Prehospital and Disaster Medicine. 2010;25(4):320–3. DOI: 10.1017/s1049023x00008268
43. Fullerton JN, Price CL, Silvey NE, Brace SJ, Perkins GD. Is the Modified Early Warning Score (MEWS) superior to clinician judgement in detecting critical illness in the pre-hospital environment? Resuscitation. 2012;83(5):557–62. DOI: 10.1016/j.resuscitation.2012.01.004
44. Gray JT, Challen K, Oughton L. Does the pandemic medical early warning score system correlate with disposition decisions made at patient contact by emergency care practitioners? Emerg Med J. 2010 des.;27(12):943–7. DOI: 10.1136/emj.2009.072959
45. Hoikka M, Lankimaki S, Silfvast T, Ala-Kokko TI. Medical priority dispatch codes-comparison with National Early Warning Score. Scand J Trauma Resusc Emerg Med. 2016;24(1):142. DOI: 10.1186/s13049-016-0336-y
46. Hoikka M, Silfvast T, Ala-Kokko TI. Does the prehospital National Early Warning Score predict the short-term mortality of unselected emergency patients? Scand J Trauma Resusc Emerg Med. 2018;26(1):48. DOI: 10.1186/s13049-018-0514-1
47. Kitahara O, Nishiyama K, Yamamoto B, Inoue S, Inokuchi S. The prehospital quick SOFA score is associated with in-hospital mortality in noninfected patients: a retrospective, cross-sectional study. PLoS ONE. 2018;13(8):e0202111. DOI: 10.1371/journal.pone.0202111
48. Leung SC, Leung LP, Fan KL, Yip WL. Can prehospital Modified Early Warning Score identify non-trauma patients requiring life-saving intervention in the emergency department? Emergency Medicine Australasia. 2016;28(1):84–9. DOI: 10.1111/1742-6723.12501
49. Magnusson C, Herlitz J, Axelsson C. Pre-hospital triage performance and emergency medical services nurse's field assessment in an unselected patient population attended to by the emergency medical services: a prospective observational study. Scandinavian Journal of Trauma, Resuscitation and Emergency Medicine. 2020;28(1):81. DOI: 10.1186/s13049-020-00766-1
50. Martín-Rodrígues F, López-Izqierdo R, Vegas CDP, Delgado-Benito JF, Perez CDP, Rodriguez VC, et al. A multicenter observational prospective cohort study of association of the prehospital national early warning score 2 and hospital triage with early mortality. Emerg Med Int. 2019 jul. 1;5147808. DOI: 10.1155/2019/5147808
51. Martín-Rodríguez F, López-Izquierdo R, Vegas CDP, Sanchez-Soberon I, Delgado-Benito JF, Martin-Conty JL, et al. Can the prehospital National Early Warning Score 2 identify patients at risk of in-hospital early mortality? A prospective, multicenter cohort study. Heart and Lung. 2020;49(5):585–91. DOI: 10.1016/j.hrtlng.2020.02.047
52. Martín-Rodríguez F, López-Izquierdo R, Vegas CDP, Delgado-Benito JF, Ibanez PDB, Mangas IM, et al. Predictive value of the prehospital NEWS2-L – National Early Warning Score 2 Lactate – for detecting early death after an emergency. Emergencias. 2019 jun.;31(3):173–9.
53. Martín-Rodríguez F, Vegas CDP, Mohedano-Moriano A, Polonio-Lopez B, Miquel CM, Vinuela A, et al. Role of biomarkers in the prediction of serious adverse events after syncope in prehospital assessment: a multi-center observational study. J Clin Med. 2020;9(3):651. DOI: 10.3390/jcm9030651
54. Martín-Rodríguez F, Lopez-Izquierdo R, Benito JFD, Sanz-Garcia A, Vegas CP, Villamor MAC, et al. Prehospital point-of-care lactate increases the prognostic accuracy of national early warning score 2 for early risk stratification of mortality: results of a multicenter, observational study. J Clin Med. 2020;9(4):1156. DOI: 10.3390/jcm9041156
55. Pirneskoski J, Kuisma M, Olkkola KT, Nurmi J. Prehospital National Early Warning Score predicts early mortality. Acta Anaesthesiol Scand. 2019;63(5):676–83. DOI: 10.1111/aas.13310
56. Silcock DJ, Corfield AR, Gowens PA, Rooney KD. Validation of the National Early Warning Score in the prehospital setting. Resuscitation. 2015;89:31–5. DOI: 10.1016/j.resuscitation.2014.12.029
57. Spangler D, Hermansson T, Smekal D, Blomberg H. A validation of machine learning-based risk scores in the prehospital setting. PLoS ONE. 2019;14(12):e0226518. DOI: 10.1371/journal.pone.0226518
58. Vihonen H, Laaperi M, Kuisma M, Pirneskoski J, Nurmi J. Glucose as an additional parameter to National Early Warning Score (NEWS) in prehospital setting enhances identification of patients at risk of death: an observational cohort study. Emergency Medicine Journal. 2020;37(5):286–92. DOI: 10.1136/emermed-2018-208309
59. Pirneskoski J, Laaperi M, Kuisma M, Olkkola KT, Nurmi J. Ability of prehospital NEWS to predict 1-day and 7-day mortality is reduced in the older adult patients. Emergency Medicine Journal. 2021;38(12):913–8. DOI: 10.1136/emermed-2019-209400
60. Martin-Rodriguez F, Sanz-Garcia A, Medina-Lozano E, Villamor MAC, Rodriguez VC, Vegas CDP, et al. The value of prehospital early warning scores to predict in – hospital clinical deterioration: a multicenter, observational base – ambulance study. Prehosp Emerg Care. 2020:25(5):597–606. DOI: 10.1080/10903127.2020.1813224
61. Ivic R, Kurland L, Vicente V, Castren M, Bohm K. Serious conditions among patients with nonspecific chief complaints in the pre-hospital setting. A retrospective cohort study. BMJ Open. 2019;9(Suppl 2):A2.2-A2. DOI: 10.1136/bmjopen-2019-EMS.5
62. Dillon K, Hook C, Coupland Z, Avery P, Taylor H, Lockyer A. Pre-hospital lowest recorded oxygen saturation independently predicts death in patients with COVID-19. British Paramedic Journal. 2020;5(3):59–65. DOI: 10.29045/14784726.2020.09.5.3.59
63. Ebrahimian A, Masoumi G, Jamshidi-Orak R, Seyedin H. Development and psychometric evaluation of the pre-hospital medical emergencies early warning scale. Indian Journal of Critical Care Medicine. 2017;21(4):205–12. DOI: 10.4103/ijccm.IJCCM_49_17
64. Essam N, Windle K, Mullineaux D, Knowles S, Gray J, Siriwardena AN. Modified Early Warning Scores (MEWS) to support ambulance clinicians’ decisions to transport or treat at home. Lincoln: University of Lincoln; 2014. Tilgjengelig fra: http://eprints.lincoln.ac.uk/id/eprint/13448/ (nedlastet 03.02.2022).
65. Martin-Rodriguez F, Castro-Villamor MA, Vegas CDP, Martin-Conty JL, Mayo-Iscar A, Benito JFD, et al. Analysis of the early warning score to detect critical or high-risk patients in the prehospital setting. Internal & Emergency Medicine. 2019;14(4):581–9. DOI: 10.1007/s11739-019-02026-2
66. Scott LJ, Redmond NM, Tavaré A, Little H, Srivastava S, Pullyblank A. Association between National Early Warning Scores in primary care and clinical outcomes: an observational study in UK primary and secondary care. British Journal of General Practice. 2020;70(695):e374–e80. DOI: 10.3399/bjgp20X709337
67. McClelland G, Haworth D. A qualitative investigation into paramedics' thoughts about the introduction of the National Early Warning Score. British Paramedic Journal. 2016;1(1):9–14. DOI: 10.1136/emermed-2016-206139.10
68. Alam N, Hobbelink EL, van Tienhoven A-J, van de Ven PM, Jansma EP, Nanayakkara PW. The impact of the use of the Early Warning Score (EWS) on patient outcomes: a systematic review. Resuscitation. 2014;85(5):587–94. DOI: 10.1016/j.resuscitation.2014.01.013
69. McGaughey J, O'Halloran P, Porter S, Blackwood B. Early warning systems and rapid response to the deteriorating patient in hospital: a systematic realist review. J Adv Nurs. 2017;73(12):2877-91. DOI: 10.1111/jan.13398
70. Polit DF, Beck CT. Nursing Research: generating and assessing evidence for nursing practice. 10. utg. Philadelphia: Wolters Kluwer; 2017.
71. Grant S, Crimmons K. Limitations of track and trigger systems and the National Early Warning Score. Part 2: sensitivity versus specificity. Br J Nurs. 2018;27(12):705–10. DOI: 10.12968/bjon.2018.27.11.624
72. Grol R. Improving patient care: the implementation of change in health care. 2. utg. Chichester: Wiley-Blackwell BMJ Books; 2013.
73. Graverholt B. IMPAKT – Implementation and action for knowledge translation. Oslo: Unit; 2016 [oppdatert 07.12.2021]. Tilgjengelig fra: https://app.cristin.no/projects/show.jsf?id=550905 (nedlastet 02.05.2021).
Henvisninger i teksten til figurene ble lagt til.























0 Kommentarer