Alle beboerne har MRSA: – Vi har smittevernet med oss hele tiden
Ved MRSA-posten på Ammerudlunden sykehjem er ingenting overlatt til tilfeldighetene når det kommer til smittevern.
Ved MRSA-posten på Ammerudlunden sykehjem er ingenting overlatt til tilfeldighetene når det kommer til smittevern.
I disse dager er det blitt stille på landets sykehjem. Det er en utfordring for sykepleiere som må balansere nødvendig smittevern med behovet for omsorg for mennesker i livets sluttfase.
Siden 2009 har Oslo-sykehusene Aker, Ullevål, Rikshospitalet og Radiumhospitalet vært fusjonert til ett stort sykehus, angivelig med èn dør inn. Meningen var at både pasienter og ansatte skulle få det bedre i tillegg til at man ville oppnå økonomisk gevinst. Fusjoneringen startet i 2005 da Rikshospitalet og Radiumhospitalet ble slått sammen. I 2009 ble alle de fire sykehusene samlet. Prosessen er derfor i full gang, og jeg vil i det følgende se nærmere på hva som egentlig skjer når man slår fire store sykehus sammen til ett. For at sammenslåingen skal lønne seg blir alle de fire sykehusene redusert til uforutsigbare størrelser, og Aker skal på sikt legges ned. Sengetallet og antall ansatte skal reduseres. Arealer skal omfordeles og man planlegger nye bygg. Ved Rikshospitalet er mulighetene for arealutvidelser svært begrenset. I tillegg er ansvaret for rundt 160 000 oslopasienter overført til omkringliggende sykehus. Alle disse grepene gjør det nærmest umulig å finne ut om den store omorganiseringen har noen som helst effekt – og i så fall, på hva?
Storsykehusets ansvarsområde som lokalsykehus, regionsykehus og
nasjonalsykehus er ennå noe usikkert, men man hevder det er mindre
enn tidligere, uten at det foreligger sikre tall. Beregningene for
Oslo og omegn, med en raskt økende befolkningsvekst og økt antall
eldre, vil trolig ikke holde mål da OUS vil få ansvar for et større
antall mennesker i nær framtid. I henhold til Statistisk
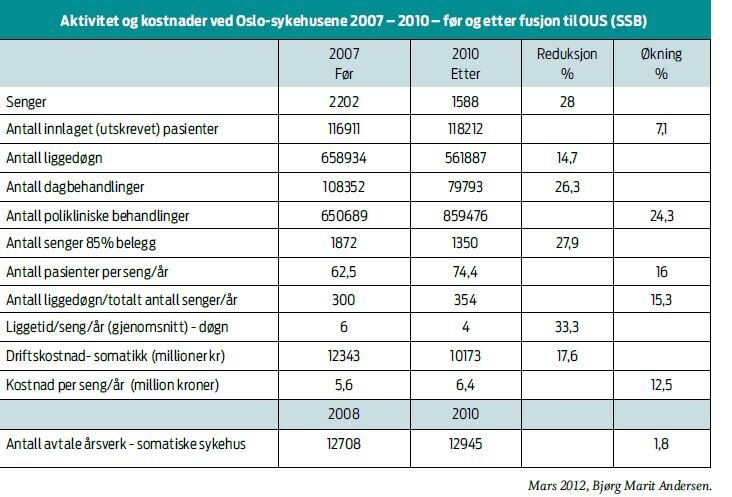
sentralbyrå (SSB) er antall somatiske senger ved OUS i rask
nedgang, og reduksjonen var allerede i gang før sammenslåingen
(Tabell 1).
Antallet senger i OUS er redusert med nesten en tredel, sammenliknet med Oslo-sykehusene i 2007. Antall senger som skal serve en voksende befolkning er derfor betydelig færre, og liggetiden er i snitt redusert fra seks til fire døgn. Man kan selvsagt veie opp dette ved at man øker antall innlagte pasienter slik trenden viser for Oslo-sykehusene og OUS i perioden 2002–2010. Men når flere pasienter skal inn på et sykehus med færre antall senger blir resultatet et sterkt overbelegg kombinert med færre liggedøgn per pasient. Hvilken effekt dette vil ha på kvalitet og pasientsikkerhet er ukjent. Antall somatiske dagbehandlinger er redusert med en fjerdedel i OUS, sammenliknet med Oslo-sykehusene, mens poliklinisk behandling er økt nesten tilsvarende i samme periode.
Det har vært en jevn økning av kostnader ved somatisk
sykehusbehandling ved Oslo-sykehusene. Før fusjonen synes økningen
å ha vært størst ved Rikshospitalet og seinere
Rikshospitalet/Radiumhospitalet. Fra 2009 tenderer
kostnadsutviklingen mot å være nedadgående. I 2010 er kostnaden for
somatisk drift ved OUS på nivå med det Oslo-sykehusene hadde til
sammen i 2005. Selv om de totale driftskostnadene for somatisk
tjeneste synes å være noe redusert i 2010, er kostnader per seng
økt fra 5,6 millioner på årsbasis i 2007 til 6,4 millioner i
2010.
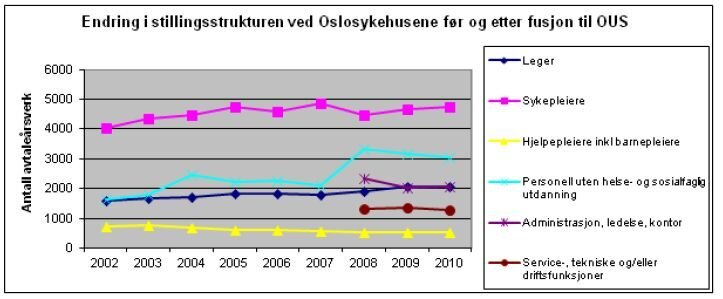
Totalt antall avtaleårsverk ved OUS var litt høyere i 2010 enn
i Oslo-sykehusene i 2008, det vil si ingen innsparing i årsverk
(Tabell 1). Avtaleårsverk ved Oslo-sykehusene har ligget på mellom
12 000 og 13 000 siden 2002. Men trykket på nedlegging av årsverk
økte i 2011. Dessverre foreligger det ikke tall for 2011 fra SSB
ennå. Siden 2002 har det vært en langsom økning i stillingsandeler
for sykepleiere og leger og denne økningen fortsetter i OUS (Figur
1). Annet helsepersonell som hjelpepleiere og barnepleiere
reduseres. Økningen av gruppen ”personell uten helse- og
sosialfaglig bakgrunn” økte kraftig ved Rikshospitalet i 2003–2004
og på nytt ved Rikshospitalet/Radiumhospitalet i 2007. Hva som
ligger i disse tallene er usikkert og bør granskes nærmere. SSB
slår sammen administrasjon, ledelse og kontor med intern service og
drift frem til 2008. Det er et tankekors at det er like mange i
administrasjon og kontor som det er leger ved sykehusene. Det er
også bekymringsfullt at antall årsverk i intern service og drift er
betydelig lavere en i administrasjonen og at dette ytterligere
reduseres i 2011 og 2012. Med økt aktivitet, kortere opphold,
større gjennomstrømming av pasienter og dårligere pasienter, vil
belastningen på personalet øke parallelt med at man reduserer
antall stillinger og belegger sengene nærmest 100 prosent hele
året. Dette kan føre til problemer med hygiene og smittevern siden
det er disse ”myke verdiene” som forsvinner først når man begynner
med innsparinger.
OUS er i ferd med å få en betydelig kapasitetsreduksjon av
senger, antall liggedøgn og antall dagbehandlinger per år
sammenliknet med tidligere. Dette til tross for en betydelig
befolkningsøkning i Oslo-området. Til gjengjeld er det en merkbar
økning av poliklinisk aktivitet som kanskje for en stor del er
generert av ventelistegarantien og som kanskje ikke i seg selv
fører til en grunnleggende behandling for pasienten. Dersom
beleggsprosenten skal ligge på det som helsetilsynet nasjonalt og
internasjonalt anbefaler som normalt – cirka 85 prosent, er
reduksjon av sengekapasitet nesten 30 prosent fra tidligere! Hver
seng benyttes i snitt av 75 pasienter hvert år. Dette er en økning
fra tidligere, og hver seng er i bruk nesten alle dager i året.
Dessuten koster sengen mer ved OUS enn det den gjorde ved de
tidligere Oslo-sykehusene. Det vil derfor være et betydelig press
på sengekapasiteten fremover. Men for å holde kapasiteten oppe
reduserer man liggetiden i gjennomsnitt med en tredel til fire døgn
per pasient.
Under slike forhold bør man diskutere hva som er akseptabel
minimum gjennomsnittlig liggetid for alvorlig syke pasienter ved
sykehus. Særlig fordi det mangler etablerte ”B-sykehus” for videre
behandling av alvorlig syke pasienter i Oslo-området. For kort
liggetid kan føre til for tidlig utskrivelse, for dårlig
diagnostikk og behandling, reinnleggelser og alvorlig forverring av
sykdommen. Samlet kan en slik utvikling bli svært fordyrende for
samfunnet. I tillegg vil presset på effektivitet og gjennomføring
for lege- og pleietjenesten, for medisinsk service og diagnostikk,
operasjonsavdelinger, intern service, renhold og vedlikehold øke.
Et ustrukturert sykehuskonglomerat med manglende oversikt,
kapasitet, ansatte, kompetanse, senger og areal vil helt klart gå
ut over sykehusets hygiene og smittevern. Det kan føre til risiko
for mer alvorlige sykehusinfeksjoner og spredning av resistente
bakterier. Dette har man ikke tatt hensyn til i det hele tatt ved
planleggingen av OUS. Hittil (2010-tall fra SSB) har ikke OUS vist
å fylle noen av de kravene som ble satt til innsparinger i årsverk
eller utgifter per seng. Og det er fremdeles mange dører inn i
systemet. Samtidig er kvaliteten på behandlingen truet av for stort
turnover, minkende kapasitet og kompetanse, og manglende opplegg
for de meget syke sykehuspasientene som er ”ferdigbehandlet” ved
OUS.
Sammenslåingen av Oslo-sykehus vil gi flere og dårligere pasienter samtidig som antallet stillinger kuttes.
Samarbeid om smittevern vil være høyest nødvendig for å begrense, og i beste fall isolere, koronaviruset. Men vi har også alle et ansvar om å ta vare på vår egen helse, skriver artikkelforfatteren.

Covid-19-pandemien, forårsaket av severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) har vært assosiert med infeksjoner og dødsfall blant helsepersonell, beboere på sykehjem og pasienter.
Det har vært motstridende anbefalinger om bruk av munnbind, ventilasjon og smitteverntiltak og uenighet om rollen dråper og aerosoler spiller i overføringen av koronaviruset. Mange diskusjoner om smitteverntiltak minner om situasjonen for rundt 30 år siden da man diskuterte luftsmitte og smitteverntiltak for tuberkulose (1, 2).
Denne oversikten er ikke en gjennomgang av litteraturen om bruk av munnbind, som flere allerede har gjort (3–6), men den er et forsøk på å belyse de medisinske og fysikalske grunnlagene for smitte via dråpene og aerosoler.
Hovedsmitteveien for SARS-CoV-2 er respiratorisk opptak av virusholdige væskepartikler som oppstår når man puster, snakker, hoster og nyser. Siden SARS-CoV-2 kan overføres noen dager før symptomene oppstår, vil presymptomatisk smitte bidra vesentlig til den totale covid-19-pandemien (7).
Oppfatningen om at dråpesmitte bare forekommer innen en til to meter, er basert på gamle påstander og eksperimenter. I 1910 publiserte Charles Chapin en bok som skulle bli førende innen smittevern. I The sources and modes of infection (8) prøver han å forklare hvorfor avstand reduserer smitte.
I kapitlet om luftbåren infeksjon konkluderer han med at man ikke kan utelukke smitte via aerosoler, men at det vil være helsepedagogisk vanskelig å formidle. Senere ble det et dogme innen smittevern, en påstand som ingen etterprøvde.
Oppfatningen om at dråpesmitte bare forekommer innen en til to meter, er basert på gamle påstander og eksperimenter.
Andre studier av hvordan dråper slippes ut under tale, hoste eller nysing, begynte på 1800-tallet, der forskere vanligvis samlet prøver på agarskåler (9). I 1897 foreslo Flugge en til to meter som trygg avstand basert på slike eksperimenter (10).
På 1940-tallet ble fotografisk dokumentasjon av dråpespredning mulig (11). Disse tidlige studiene hadde begrenset nøyaktighet, spesielt for lengre avstander. Likevel danner disse resultatene fortsatt grunnlaget for avstandsregelen om en til to meter.
Ifølge nyere funn kan dråper transporteres opptil åtte meter (12). I motsetning til aerosoler faller imidlertid større dråper til slutt på overflater og blir ikke i luften i flere timer, noe som kan ha en avgjørende innflytelse på eksponeringens varighet. Derfor er det ikke alltid tilstrekkelig å holde en avstand på to meter for å unngå en dråpeinfeksjon, for eksempel ved ukontrollert hoste eller nysing og ved turbulente luftstrømmer (12).
Større dråper og dråpekjerner spiller derfor en rolle også ut over «enmetersgrensen». I et miljø der luften «står stille», kan de mange små dråpene eller dråpekjernene som slippes ut når man snakker, tenkes som en usynlig «sky» som bare sakte legger seg (13).
Hvorvidt og hvor raskt dråper og aerosoler synker eller blir værende i luften, avhenger av størrelsen på partiklene og en rekke andre faktorer, inkludert temperatur, fuktighet (14) og luftbevegelse.
Avhengig av partikkelstørrelse skilles det mellom store dråper (større enn 5–10 μm) og mindre dråper eller dråpekjerner (15). Overgangen er flytende; såkalte dråpekjerner kan oppstå fra dråper når de tørker ut i luften (16).
Når dråpene har forlatt nesen eller munnen, fordamper vanninnholdet veldig raskt. Det som gjenstår, er de faste komponentene i form av mindre partikler som synker saktere. Ved 1 μm store dråper fordamper vannet på noen få millisekunder, mens 100 μm store dråper trenger nesten ett minutt på å fordampe vannet (16).
Mindre dråper holder seg betydelig lenger i luften.
Mindre dråper holder seg betydelig lenger i luften (13). Når det gjelder større dråper, spiller ikke dehydrering noen rolle – de er så tunge at de raskt faller på gulvet. En dråpe på 500 μm faller innen ett sekund fra en høyde på 1,6 meter. En liten dråpe (10 µm) trenger ni minutter (17).
På grunn av den lave vekten til dråpekjerner kan de flyte i luften i lang tid (aerosol). Hvis dråpekjerner blir inhalert, når de til de nedre luftveiene (14, 18, 19).
Aerosoler skilles ut når man puster og snakker, men enda mer når man skriker og synger. Hoste og nysing gir betydelig flere dråper (20, 21). Her er det viktig å minne om luftveienes fysiologi:
Ved dråpesmitte treffer dråpene typisk kontaktpersoner som en spray i øyne, nese og munn (12) og blir «fanget» der av slimhinnene (14). Denne smitteveien blir ansett som den viktigste for SARS-CoV-2.
De små dråpekjernene kan flyte i luften i lang tid (aerosol), distribuere seg i lukkede rom og sveve over ti meter (14). Derfor er det ut over tometersgrensen snakk om en «overføring via aerosoler (16).
Infeksjonsrisikoen er resultatet av et komplekst forhold mellom verten og et patogen. De fleste faktorene som påvirker infeksjonen og sykdommens alvorlighetsgrad, er relatert til verten. Egenskapene til mikroben er virulens, antall, eksponeringsvei og eksponeringstid (25).
Virulensen er ikke mulig å endre. Så lenge en effektiv vaksine ikke er tilgjengelig, kan immunforsvaret bare påvirkes i svært begrenset grad. Realistisk sett kan vi bare påvirke eksponeringen og dermed antallet patogener, altså smittedosen, for å unngå SARS-CoV-2-infeksjon.
Hvis minimumsavstanden opprettholdes, er det lav sannsynlighet for smitte utendørs på grunn av luftbevegelsen og UV-strålingen (26).
Situasjonen er annerledes innendørs: SARS-CoV-2 var i stand til å overleve i en eksperimentell studie i aerosoler i minst tre timer (27). En rekke risikofaktorer kan øke sannsynligheten for SARS-CoV-2-smitte gjennom mindre – og muligens større – dråper over en avstand på mer enn to meter.
SARS-CoV-2 var i stand til å overleve i en eksperimentell studie i aerosoler i minst tre timer.
Hvis rommet er dårlig ventilert og en eller flere personer som frigjør smittsomme dråper ut i romluften, er til stede i en viss periode, øker eksponeringen. Atferden påvirker frigjøringen av små dråper (16).
I tillegg spiller inneklimaet en viktig rolle, siden det kan oppstå en akkumulasjon av partikler. For eksempel har svært mange skoler i Norge et dårlig inneklima på grunn av manglende vedlikehold (28). Forfattere beskriver blant annet en høy finstøvforurensning i skolebygg, og finstøv kan øke rekkevidden til aerosoler (29).
Spesielt på kalde vinterdager synker den relative fuktigheten innendørs, noe som kan resultere i tørre slimhinner, som da igjen kan svekke immunforsvaret (30).
For andre smittsomme sykdommer er det kjent at en viss minimumsmengde av patogener må absorberes i kroppen før en infeksjon kan oppstå. Denne smittedosen er veldig lav for noen patogener, for eksempel norovirus. Den smittsomme dosen for SARS-CoV-2 er foreløpig ukjent. Når det gjelder SARS-CoV-1, anslås det til noen få hundre viruspartikler.
Det kan antas at langvarig eksponering fører til en akkumulering av små mengder virus, slik at smittedosen oppnås.
Direkte kontakt ansikt-til-ansikt fører til at den nødvendige smittedosen absorberes mye raskere enn hvis tilstrekkelig avstand opprettholdes, eller hvis en stor del av dråpene eller aerosolene holdes borte av et passende munnbind. Det kan antas at langvarig eksponering fører til en akkumulering av små mengder virus, slik at smittedosen oppnås (17).
Generelt fører opptak av respiratoriske patogener i lungene til et mer alvorlig klinisk bilde (31). Partikler ≤10 μm kan komme inn i nedre luftveier (ved <1–3 μm direkte i alveolene).
Partikler >10 μm når bare de øvre luftveiene ifølge gjeldende oppfatning (12, 31). Smitte via aerosoler er forbundet med mer alvorlige symptomer ved influensa (15).
Inntil mer detaljerte vitenskapelige funn tillater et mer differensiert syn, bør både dråper og aerosoler tas i betraktning når man bestemmer smitteverntiltak for å unngå SARS-CoV-2-infeksjon.
Ventilasjon kan effektivt redusere konsentrasjonen av smittsomme aerosoler innendørs. Derimot er det ennå ikke avklart hvor viktig ventilasjon er for å unngå typiske dråpeinfeksjoner. Også et vanlig munnbind er mest sannsynlig tilstrekkelig for å redusere risikoen for smitte via aerosoler under mange omstendigheter.
For SARS-CoV-2 er smitte via dråpekjernene i luften ut over to meter trolig ikke hovedveien, men en «opportunistisk», det vil si ytterligere, smittevei (32). For å kontrollere pandemien bør imidlertid alle smitteveiene avbrytes (14).
ALARA er et akronym for «As Low As Reasonably Achievable», på norsk «så lavt som rimelig oppnåelig». Det beskriver et prinsipp om strålevern.
Når det gjelder ioniserende stråling, krever ALARA-prinsippet at mennesker, dyr og materiale utsettes for så lave nivåer av stråling (til og med under grenseverdier) som det er praktisk mulig å gjennomføre, og ved å avveie fordeler og ulemper.
I analogi med føre var-tanken innen strålevern bør sannsynligheten for eksponering for SARS-CoV-2, antallet eksponerte personer og den individuelle dosen patogener som påvirker en person, holdes så lavt som det er rimelig oppnåelig.
1. Sepkowitz KA. How contagious is tuberculosis? Clin Infect Dis. 1996;23(5):954–62.
2. Fennelly KP. Personal respiratory protection against Mycobacterium tuberculosis. Clin Chest Med. 1997;18(1):1–17.
3. Li Y, Liang M, Gao L, Ahmed MA, Uy JP, Cheng C et al. Face masks to prevent transmission of COVID-19: a systematic review and meta-analysis. Am J Infect Control. 2020.
4. Chaabna K, Doraiswamy S, Mamtani R, Cheema S. Facemask use in community settings to prevent respiratory infection transmission: a rapid review and meta-analysis. Int J Infect Dis. 2020.
5. Chu DK, Akl EA, Duda S, Solo K, Yaacoub S, Schunemann HJ et al. Physical distancing, face masks, and eye protection to prevent person-to-person transmission of SARS-CoV-2 and COVID-19: a systematic review and meta-analysis. Lancet. 2020;395(10242):1973–87.
6. Brainard J, Jones NR, Lake IR, Hooper L, Hunter PR. Community use of face masks and similar barriers to prevent respiratory illness such as COVID-19: a rapid scoping review. Euro Surveill. 2020;25(49):2000725.
7. Buitrago-Garcia D, Egli-Gany D, Counotte MJ, Hossmann S, Imeri H, Ipekci AM et al. Occurrence and transmission potential of asymptomatic and presymptomatic SARS-CoV-2 infections: a living systematic review and meta-analysis. PLoS Med. 2020;17(9):e1003346.
8. Chapin CV. The sources and modes of infection. 1. utg. New York: J. Wiley & sons; 1910.
9. Papineni RS, Rosenthal FS. The size distribution of droplets in the exhaled breath of healthy human subjects. Journal of Aerosol Medicine. 1997;10(2):105–16.
10. Flügge C. Ueber luftinfection. Zeitschrift für Hygiene und Infektionskrankheiten. 1897;25(1):179–224.
11. Turner CE, Jennison MW, Edgerton HE. Public health applications of high-speed photography. Am J Public Health Nations Health. 1941;31(4):319–24.
12. Sommerstein R, Fux CA, Vuichard-Gysin D, Abbas M, Marschall J, Balmelli C et al. Risk of SARS-CoV-2 transmission by aerosols, the rational use of masks, and protection of healthcare workers from COVID-19. Antimicrob Resist Infect Control. 2020;9(1):100.
13. Stadnytskyi V, Bax CE, Bax A, Anfinrud P. The airborne lifetime of small speech droplets and their potential importance in SARS-CoV-2 transmission. Proc Natl Acad Sci USA. 2020;117(22):11875–7.
14. Morawska L, Cao J. Airborne transmission of SARS-CoV-2: the world should face the reality. Environ Int. 2020;139:105730.
15. Tellier R, Li Y, Cowling BJ, Tang JW. Recognition of aerosol transmission of infectious agents: a commentary. BMC Infect Dis. 2019;19(1):101.
16. Wei J, Li Y. Airborne spread of infectious agents in the indoor environment. Am J Infect Control. 2016;44(9 Suppl):S102–8.
17. Somsen GA, van Rijn C, Kooij S, Bem RA, Bonn D. Small droplet aerosols in poorly ventilated spaces and SARS-CoV-2 transmission. Lancet Respir Med. 2020;8(7):658–9.
18. Buonanno G, Morawska L, Stabile L. Quantitative assessment of the risk of airborne transmission of SARS-CoV-2 infection: Prospective and retrospective applications. Environ Int. 2020;145:106112.
19. Verdens helseorganisasjon (WHO). Transmission of SARS-CoV-2: implications for infection prevention precautions. Verdens helseorganisasjon; 2020. Tilgjengelig fra: https://www.who.int/news-room/commentaries/detail/transmission-of-sars-cov-2-implications-for-infection-prevention-precautions (nedlastet 26.01.2021).
20. Wilson NM, Norton A, Young FP, Collins DW. Airborne transmission of severe acute respiratory syndrome coronavirus-2 to healthcare workers: a narrative review. Anaesthesia. 2020;75(8):1086–95.
21. Gralton J, Tovey E, McLaws ML, Rawlinson WD. The role of particle size in aerosolised pathogen transmission: a review. J Infect. 2011;62(1):1–13.
22. Romano-Bertrand S, Aho-Glele LS, Grandbastien B, Gehanno JF, Lepelletier D. Sustainability of SARS-CoV-2 in aerosols: should we worry about airborne transmission? J Hosp Infect. 2020;105(4):601–3.
23. Bourouiba L. Turbulent gas clouds and respiratory pathogen emissions: potential implications for reducing transmission of COVID-19. JAMA. 2020;323(18):1837–8.
24. Xie X, Li Y, Chwang AT, Ho PL, Seto WH. How far droplets can move in indoor environments – revisiting the Wells evaporation-falling curve. Indoor Air. 2007;17(3):211–25.
25. Public Health Agency of Canada. Pathogen risk assessment. Canada: Government of Canada; 2018.
26. Sagripanti JL, Lytle CD. Estimated inactivation of coronaviruses by solar radiation with special reference to COVID-19. Photochem Photobiol. 2020;96(4):731–7.
27. van Doremalen N, Bushmaker T, Morris DH, Holbrook MG, Gamble A, Williamson BN et al. Aerosol and surface stability of SARS-CoV-2 as compared with SARS-CoV-1. N Engl J Med. 2020;382(16):1564–7.
28. Becher R, Bjerke M, Martinsen F, Vrevik J. Inneklima i skoler og barnehager: helsemessig betydning for barn og unge. Oslo: Folkehelseinstituttet; 2016.
29. Ahlawat A, Wiedensohler A, Mishra SK. An overview on the role of relative humidity in airborne transmission of SARS-CoV-2 in indoor environments. Aerosol and Air Quality Research. 2020;20(9):1856–61.
30. Kudo E, Song E, Yockey LJ, Rakib T, Wong PW, Homer RJ et al. Low ambient humidity impairs barrier function and innate resistance against influenza infection. Proc Natl Acad Sci USA. 2019;116(22):10905–10.
31. Thomas RJ. Particle size and pathogenicity in the respiratory tract. Virulence. 2013;4(8):847–58.
32. Klompas M, Baker MA, Rhee C. Airborne transmission of SARS-CoV-2: theoretical considerations and available evidence. JAMA. 2020;324(5):441–2.
Dråper, dråpekjerner og aerosoler kan smitte over større avstander enn antatt. Hvis vi skal få kontroll over pandemien, bør alle smitteveiene avbrytes.
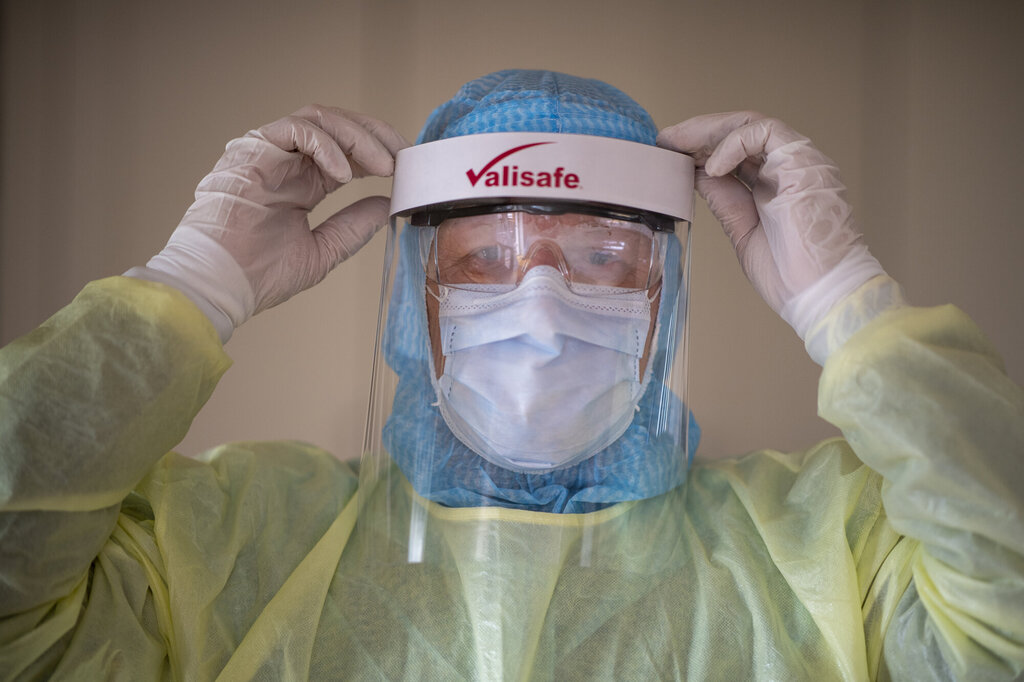
En covid-19-pasient skal akuttopereres. En anestesisykepleier og to anestesileger deltar ved intubasjonen. Det er varslet om mangel på smittevernutstyr, og kun den som utfører intubasjonen, har på seg åndedrettsvern – de andre har bare kirurgisk munnbind.
Etter vellykket intubasjon går akuttcallingen – det er hjertestans på lungeavdelingen. De blir enige om at anestesisykepleieren løper ut på denne. Pasienten som har hjertestans, er kjent lungesyk. Han ligger med ikke-invasiv ventilasjon (NIV) til vanlig og er innlagt på grunn av feber og økende respirasjonsbesvær. Etter denne hendelsen rekker anestesisykepleieren tilbake til pauserommet i operasjonsavdelingen for en pust i bakken.
Neste på programmet er en dame på 90 år som skal ha brukket lårhalsen, og må opereres. Anestesisykepleieren rekker også å gjennomføre anestesien til en 20 år gammel gutt som må operere et armbrudd, før arbeidsdagen er over.
Hjemme venter mann og tre barn. Privat følger de anbefalinger fra kommuneoverlegen, som tilsier at barn kan ha to, tre faste lekevenner. Etter ti dager begynner anestesisykepleieren å hoste …
Alle tiltak som har blitt iverksatt i forbindelse med SARS CoV-2-pandemien har vært rettet mot å begrense smitte. Dette har til nå vært svært vellykket. Den 7. mai kunne helsemyndighetene melde om et reproduksjonstall under 0,5 – noe som angir hvor mange nye smittede en gjennomsnittlig pasient gir opphav til i en befolkning uten immunitet og uten smitteverntiltak.
Sannsynligheten for en ny «bølge» av smittede er likevel stor. Folkehelseinstituttet anbefaler at kommuner og sykehus fortsatt planlegger for en epidemi som varer om lag et år og som på toppen medfører samtidig:
Folkehelseinstituttet regner med at minst 1 prosent av alle smittede vil ha behov for sykehusinnleggelse, og at rundt en firedel av disse vil ha behov for mekanisk pustehjelp.
Pasienter som er bærere av SARS CoV-2-viruset er smitteførende via dråpe- (2–4) eller luftsmitte (5, 6). Intubasjon er vist å innebære høy smitterisiko for den som intuberer (7–9).
Det er internasjonal konsensus om at antall personer til stede ved intubasjon skal begrenses, og at den som intuberer skal bruke fullt smittevernutstyr: åndedrettsvern, langermet frakk, hette, briller/visir og skotrekk (10, 11).
Likevel viser en kartlegging som Anestesisykepleierne Norsk Sykepleierforbund (NSF) har gjennomført i 34 anestesiavdelinger nasjonalt (12), at bruken av åndedrettsvern er varierende. I kartleggingen oppgir 11,8 prosent at den som assisterer ved intubasjon kun bruker kirurgisk munnbind, mens dette gjelder for 35,3 prosent av annet personell på operasjonsstuen under intubasjon.
2,9 prosent av alt personell bruker overtrekk over sko, og 58,8 prosent bruker egne smittesko. Intubatør og assistent bruker hette og briller eller visir i 100 prosent av tilfellene, mens annet personell på operasjonsstuen under intubasjon bruker dette i 88,2 prosent av tilfellene.
De radioaktive partiklene kunne registreres i hår, på udekket hud på halsen og ørene samt på skoene.
I en nylig publisert studie har man simulert en pasient med covid-19, ved hjelp av radioaktivt merket aerosol. Formålet var å kartlegge spredningen av virus ved hoste og under intubasjon.
Konklusjonen var at de radioaktive partiklene kunne registreres i hår, på udekket hud på halsen og ørene samt på skoene hos både intubatør og de to assistentene (13).
Folkehelseinstituttet var relativt tidlig ute med en kunnskapsoppsummering om aerosolgenererende prosedyrer som innebærer luftsmitte. Konsistente funn viser at det kan produseres aerosoler i forbindelse med intubering, trakeotomi, hjerte-lunge-redning og manuell ventilering.
Videre identifiserte de studier som tyder på at bronkoskopi, ikke-invasiv ventilering (NIV) og bruk av forstøver kan bidra til produksjon av aerosoler, men denne dokumentasjonen var svakere og mindre konsistent (14).
Ifølge en australsk konsensusrapport trekkes både hosting, nysing og forstøverbehandling frem som aerosolgenererende prosedyrer (10).
En studie av 202 pasienter med covid-19 som ble intubert i Wuhan, viste at ingen av de som intuberte ble smittet (15). Alle intubasjonene ble gjennomført av trente intubatører. Alle brukte åndedrettsvern (powered air-purifying respirator, PAPR), briller samt heldekkende beskyttelsesfrakker (inkludert hode og føtter) og doble hansker. De brukte N95/FFP3-masker med kirurgisk munnbind utenpå ved av- og påkledning av beskyttelsesutstyret. Av- og påkledning ble dobbeltkontrollert av en kollega.
Ifølge forfatterne råder det usikkerhet om hvorvidt en N95/FFP3 maske vil gi samme beskyttelse som PAPR. Videre påpeker de at risikoen for selv-smitte er stor ved avkledning av utstyr. Det anbefales derfor grundig opplæring og simulering i dette av spesialutdannet smittevernpersonell samt nøye overvåkning i prosessen (15).
Alt personell i rommetskal bruke aerosolbeskyttende utstyr.
På et tidlig tidspunkt tok Anestesisykepleierne NSF kontakt med Norsk anestesiologisk forening (NAF) for bistand til å utarbeide smittevernprosedyrer. NAF henviste da til den australske konsensusen (10), som også påpeker at alt personell i rommet både under og etter intubasjonen skal bruke aerosolbeskyttende utstyr.
Videre sier den australske konsensusen at ingen andre enn de som er involvert i intubasjonen skal være til stede når dette pågår, og at man skal tillate «tilstrekkelig tid» til at aerosolene har forduftet før annet personell kommer inn. Denne tiden avhenger av luftutvekslingen.
Munnbind beskytter mot sprut og dråpesmitte, ikke mot luftbåren smitte. For å beskytte seg mot luftbåren smitte må en derfor bruke åndedrettsvern. I de fleste situasjoner vil en filtrerende halvmaske gi god beskyttelse. Ved eksponering for luftbåren smitte skal det benyttes partikkelfilter klasse FFP3 (16).
I de fleste situasjoner vil en filtrerende halvmaske gi god beskyttelse.
Åndedrettsvern brukes til beskyttelse mot luftbåren smitte, enten med filtrerende halvmaske eller med krafttilført (motordrevet) filtrerende utstyr med hjelm eller hette.
Åndedrettsvern av typen filtrerende halvmaske kan ikke benyttes av personer med skjegg eller dem som er ubarberte, da dette kan hindre god kontakt mellom åndedrettsvernet og ansiktet, ifølge Regionalt kompetansesenter for smittevern i Helse Sør-Øst. Personer med skjegg og dem som er ubarberte, må bruke filtrerende utstyr med hjelm eller hette (16). Filtrerende ansiktsmasker finnes i tre klasser ut ifra grad av filtreringsevne/beskyttelse: FFP1, FFP2 og FFP3.
Filtrene deles i tre klasser: P1, P2 og P3, med krav til filtreringsevne og pustemotstand (NS-EN 143:2000/AC:2002).

Tilordnet beskyttelsesfaktor (APF – assigned protection factor) defineres som «den beskyttelsen som det er realistisk at man kan oppnå på arbeidsplassen hos 95 prosent av brukere som har fått adekvat opplæring, får veiledning og tilsyn, og som bruker et korrekt tilpasset åndedrettsvern».
Tilordnet beskyttelsesfaktor for filtrerende åndedrettsvern er som vist i tabell 2.

En oppsummering av forskning på masker viser at allmenn bruk av masker kan være hensiktsmessig, spesielt med tanke på asymptomatiske bærere av sykdommen. Helsepersonell anbefales her å bruke åndedrettsvern kontinuerlig på jobb, ved all kontakt med covid-19-pasienter (19).
En annen oppsummeringsartikkel har konkludert med manglende evidens for om munnbind og N95-åndedrettsvern gir samme virusbeskyttelse ved ikke-aerosolgenererende prosedyrer. Her konkluderer forfatterne med at det bør foretas en vurdering for å spare på N95-maskene til aerosolgenererende prosedyrer ved manglende tilgang (20).
Etter en henvendelse fra artikkelforfatteren til Folkehelseinstituttet oppgis følgende: «Det er bestemt å vurdere FFP2- og FFP3-masker som likestilte. Forskjellene er marginal, og riktig tilpasning er av mye større betydning. Vi har likevel valgt å nevne FFP3 før FFP2 i våre råd. Vi anbefaler i utgangspunktet ikke N95-masker, da disse ikke er godkjent i den europeiske standarden. Det er mulig de blir det, og de vil å så fall være tilsvarende FFP2-masker.»
Hele 70,6 prosent av respondentene i undersøkelsen til Anestesisykepleierne NSF oppga at smittevernprosedyrer hadde blitt endret med utgangspunkt i tilgang på smittevernutstyr og ikke basert på ny forskning eller nye nasjonale anbefalinger. Videre oppga 73,5 prosent at de har opplevd mangel på FFP3-masker, 29,4 prosent FFP2-masker, 50 prosent kirurgisk munnbind, 29,4 prosent smittefrakker, og 35,3 prosent desinfeksjonssprit.
Hele 70,6 prosent av respondentene i undersøkelsen oppga at smittevernprosedyrer hadde blitt endret.
Folkehelseinstituttet har kommet med egne anbefalinger for bruk av smittevernutstyr ved en mangelsituasjon samt råd for utvidet bruk og gjenbruk av utstyr (21). Her spesifiseres det for eksempel at det ikke er behov for å skifte munnbind, visir eller frakk mellom hver pasient ved prøvetaking av pasienter med mistanke om covid-19. Forutsetningen er at personellet ikke berører munnbind, øyebeskyttelse eller frakk og deretter berører pasienter, eller at frakken kommer i kontakt med pasienter under prøvetaking. Her anbefales også en gradvis «nedtrapping» av for eksempel maskebruk fra FFP3 til FFP2 til FFP1, når annet ikke er tilgjengelig, eller munnbind type I ved mangel på type II og III.
Enhver endring av smittevernprosedyrer med utgangspunkt i utstyrsmangel innebærer økt risiko for smitte.
I situasjonsbeskrivelsen innledningsvis vil anestesisykepleieren på grunn av utilstrekkelig beskyttelse kunne innebære smittefare. Hun kan ha dratt smitten med seg til lungeavdelingen og teamet rundt pasienten med hjertestans, til den gamle damen med hoftebrudd eller den unge mannen med armbrudd. Hun kan ha tatt viruset med seg hjem og medført risiko for sin familie, barnas venner og deres familie og venner igjen.
SARS-CoV-2 smitter også i inkubasjonstiden samt hos smittede uten symptomer.
SARS-CoV-2 smitter også i inkubasjonstiden samt hos smittede uten symptomer (22–29). Forskning har vist til inkubasjonstider på fra 4 til 5,2 dager (23, 30, 31). Dette samsvarer med Verdens helseorganisasjon (WHO) som rapporterer 2 til 10 dager (32). Smittepotensialet ved ikke-påvist sykdom er stort.
Helsepersonell er i situasjoner med kjent smitte, de håndterer pasienter med påvist covid-19. I slike situasjoner er det viktig med nasjonale, evidensbaserte høyrisikoprosedyrer og at det legges en plan ved eventuell utstyrsknapphet. Prosedyrene må ikke endres på grunn av mangel på utstyr! Videre må helsepersonell sikres at de ikke kan pålegges å gjennomføre slike prosedyrer uten nødvendig beskyttelsesutstyr.
1. Folkehelseinstituttet. Ny risiko- og responsrapport om covid-19-epidemien 2020. Tilgjengelig fra: https://www.fhi.no/nyheter/2020/ny-risiko--og-responsrapport-om-covid-19-epidemien2/ (nedlastet 13.05.2020).
2. Zhonghua L, Xing B, Xue Z. The epidemiological characteristics of an outbreak of 2019 novel coronavirus diseases (COVID-19) in China. Novel Coronavirus Pneumonia Emergency Response Epidemilogy Team; 2020. Tilgjengelig fra: https://pubmed.ncbi.nlm.nih.gov/32064853/ (nedlastet 13.05.2020).
3. Yang W, Cao Q, Quin L. Clinical characteristics and imaging manifestations of the 2019 novel coronavirus disease (COVID-19): a multi-center study in Wenzhou city, Zhejiand, China. J Infect. 2020;80:388–93.
4. Tian S, Hu W, Niu L, Liu H, Xu S, Xiao S. Pulmonary pathology of early-phase 2019 novel coronavirus (COVID-19) pneumonia in two patients with lung cancer. J Thorac Oncol. 2020.
5. van Doremalen N, Bushmaker T, Morris D. Aerosol and surface stability of SARS-CoV-2 as compared with SARS-CoV-1. N Eng J Med. 2020.
6. Bourouiba L. Turbulent gas clouds and respiratory pathogen emissions: potential implications for reducing transmission of COVID-19. JAMA. 2020.
7. Zhonghua J, Hu H, Zhi X. Expert consensus on preventing nosocomial transmission during respiratory care for critically ill patients infected by 2019 novel coronavirus pneumonia. Respiratory Care Committee of Chinese Thoracic Society; 2020. Tilgjengelig fra: https://pubmed.ncbi.nlm.nih.gov/32077661/ (nedlastet 12.05.2020).
8. Zuo M, Huang Y, Ma W. Expert recommendations for tracheal intubation in critically ill patients with novel coronavirus disease 2019. Chin Med Sci. 2020.
9. Wax R, Christian M. Practical recommendations for critical care and anesthesiology teams for caring for novel coronavirus (2019-nCov) patients. Can J Anaesth. 2020.
10. Brewster D, Chrimes N, Thy B, et al. Consensus statement: Safe Airway Society principles of airway management and tracheal intubation specific to the COVID-19 adult patient group. Med J Austr. 2020.
11. SIIARTI Airway Research Group and the European Airway Management Society. Airway management. 2020. Tilgjengelig fra: https://www.esahq.org/esa-news/covid-19-airway-management/ (nedlastet 13.05.2020).
12. Leonardsen A. COVID-19 – en forvirringstilstand. Dagens Medisin. 2020. Tilgjengelig fra: https://www.dagensmedisin.no/artikler/2020/05/08/covid-19--en-forvirringstilstand2/ (nedlastet 13.05.2020).
13. Feldman O, Meir M, Shavit D, Idelman R, Shavit I. Exposure to a surrogate measure of contamination from simulated patients by emergency department personnel wearing personal protective equipment. JAMA. 2020;e-pub ahead of print.
14. Norwegian Institute of Public Health. COVID-19 epidemic: Aerosol generating procedures in health care, and COVID-19. 2020. Tilgjengelig fra: https://www.fhi.no/globalassets/dokumenterfiler/rapporter/2020/aerosol-generating-procedures-in-health-care-and-covid19-rapport-2020.pdf (nedlastet 13.05.2020).
15. Wenlong Y, Wang T, Jiang B, Gao F, Wang L, Zheng H, et al. Emergency tracheal intubation in 202 patients with COVID-19 in Wuhan, China: lessons learnt and international expert recommendations. BJA. 2020.
16. Regionalt Kompetansesenter for smittevern Helse Sør-Øst. Bruk av åndedrettsvern 2020. Tilgjengelig fra: https://www.infeksjonskontroll.no/forebygging/5779 (nedlastet 13.05.2020).
17. Oslo universitetssykehus. Bruk av åndedrettsvern ved luftsmitte 2020. Tilgjengelig fra: https://ehandboken.ous-hf.no/document/21564/fields/23 (nedlastet 13.05.2020).
18. Standard Norge. NS-EN 149:2001+A1:2009 Åndedrettsvern – Filtrerende halvmasker til beskyttelse mot partikler – Krav, prøving, merking. 2009. Tilgjengelig fra: https://www.standard.no/no/Nettbutikk/produktkatalogen/Produktpresentasjon/?ProductID=388527 (nedlastet 13.05.2020).
19. MacIntyre C, Chughtai A. A rapid systematic review of the efficacy of face masks and respirators against coronaviruses and other respiratory transmissible viruses for the community, healthcare workers and sick patients. In J Nurs Stud. 2020.
20. Bartoszko J, Farooqi M, Alhazzani W, Loeb M. Medical masks vs N95 respirators for preventing COVID-19 in healthcare workers: a systematic review and meta-analysis of randomized trials. Influenza and other respiratory viruses. 2020.
21. Folkehelseinstituttet. Personlig beskyttelsesutstyr ved covid-19 ved en mangelsituasjon, inkludert råd om utvidet bruk og gjenbruk 2020. Tilgjengelig fra: https://www.fhi.no/nettpub/coronavirus/helsepersonell/personlig-beskyttelsesutstyr/#tiltak-for-aa-redusere-behov-for-beskyttelsesutstyr (nedlastet 13.05.2020).
22. Phan LT, Nguyen TV, Luong QC, Nguyen TV, Nguyen HT, Le HQ, et al. Importation and Human-to-Human Transmission of a Novel Coronavirus in Vietnam. N Engl J Med. 2020;382(9): 872–4.
23. Li Q, Guan X, Wu P, Wang X, Zhou L, Tong Y, et al. Early Transmission Dynamics in Wuhan, China, of Novel Coronavirus-Infected Pneumonia. N Engl J Med. 2020;382 (13): 1199–207.
24. Yu P, Zhu J, Zhang Z, Han Y. A Familial Cluster of Infection Associated With the 2019 Novel Coronavirus Indicating Possible Person-to-Person Transmission During the Incubation Period. J Infect Dis. 2020.
25. Hu Z, Song C, Xu C, Jin G, Chen Y, Xu X, et al. Clinical characteristics of 24 asymptomatic infections with COVID-19 screened among close contacts in Nanjing, China. Sci China Life Sci. 2020.
26. Bai Y, Yao L, Wei T, Tian F, Jin DY, Chen L, et al. Presumed asymptomatic carrier transmission of COVID-19. JAMA. 2020.
27. Chan JF, Yuan S, Kok KH, To KK, Chu H, Yang J, et al. A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster. Lancet. 2020;395 (10223): 514–23.
28. Rothe C, Schunk M, Sothmann P, Bretzel G, Froeschl G, Wallrauch C, et al. Transmission of 2019-nCoV Infection from an Asymptomatic Contact in Germany. N Engl J Med. 2020;382 (10): 970–1.
29. Ki M. Epidemiologic characteristics of early cases with 2019 novel coronavirus (2019-nCoV) disease in Korea. Epidemiol Health. 2020;42(0): e2020007-0.
30. Pung R, Chiew CJ, Young BE, Chin S, Chen MI, Clapham HE, et al. Investigation of three clusters of COVID-19 in Singapore: implications for surveillance and response measures. Lancet. 2020.
31. Lauer SA, Grantz KH, Bi Q, Jones FK, Zheng Q, Meredith HR, et al. The Incubation Period of Coronavirus Disease 2019 (COVID-19) From Publicly Reported Confirmed Cases: Estimation and Application. Ann Intern Med. 2020.
32. WHO. Novel Coronavirus (2019-nCoV) situation report – 7. WHO. 2020. Tilgjengelig fra: https://www.who.int/emergencies/diseases/novel-coronavirus-2019/situation-reports (nedlastet 13.05.2020).
Når smittevernprosedyrer blir endret på grunn av mangel på utstyr, øker faren for at helsepersonell og pasienter blir smittet av SARS CoV-2-viruset. Likevel har prosedyrer blitt endret under pandemien.
De fleste av oss tilbringer mye tid innendørs, der vi deler luften vi puster. Den utåndede luften blandes med resten av romluften og blir delvis innåndet igjen av de tilstedeværende. Hva er da betydningen av dråper og aerosoler som ikke overholder «enmetersgrensen»?
Streng rasjonering på smittevernutstyr. Trange skyllerom. Pasienter med tilgang til felleskjøkken, oppvask og mat. Frykt for økt tvang ved smitte. Sykepleierne i kommunene er bekymret for dårlig smittevern.
Afrikanske musikere sprer smittevern og håp gjennom musikk.

Jeg går litt tilbake i tid, til midten av februar 2021, når vi er i starten av tredje bølge av pandemien. Det er fredag ettermiddag, og jeg er på seinvakt ved en av landets største intensivavdelinger. Vi er allerede på bristepunktet av hva vi kan håndtere.
Jeg tar imot rapport om pasienten jeg skal ha ansvaret for. Pasienten, en mann i 60-årene, har akkurat ankommet, han ventet i det lengste før han tok kontakt med helsevesenet. Kanskje var det kona som ringte 113?
Da ambulansen hentet ham, var han knapt ved bevissthet. Nå legges han i kunstig koma. Han får neppe med seg ordene mine: «Du er på sykehus, vi tar vare på deg.» Det legges inn venekateter, arteriekateter, urinkateter, det tas blodprøver og røntgen. Vi jobber i dyp konsentrasjon, vi redder liv.
Under normale omstendigheter er ivaretakelse av pårørende en viktig del av gjøremålene våre. Denne ettermiddagen skulle noen ha sittet på pårørenderommet nederst i korridoren, ventende på å få komme inn.
Kanskje har de tatt med bilder av pasienten de skal besøke. Bilder som forteller en historie, som sier oss noe om hvem pasienten i senga er, siden han selv ikke er i stand til det. Kanskje har de med tegninger fra barn eller barnebarn – som forankrer pasienten til verdenen utenfor sykerommet.
Kona til pasienten jeg har ansvaret for, skulle også vært blant dem som venter på pårørenderommet. Jeg skulle ha gått inn til henne, informert om behandlingen mannen hennes får, forberedt henne på hva som møter henne når hun kommer inn på rommet: respirator, tube i munnen, intravenøsslanger, ledninger og alarmer. Det blir bare en samtale på telefonen, hun får ikke komme på besøk. Hun er i karantene, og det er besøksrestriksjoner.
Det blir en kort natt, og lørdag morgen er jeg tilbake hos pasienten som kom inn i går. Han skal legges over i mageleie for å ventilere alle delene av lungene, det er mye som skal ordnes og organiseres.
Sykepleieren hos pasienten ved siden av får beskjed om å gjøre sin pasient klar for overflytting til en annen intensivavdeling ved et annet sykehus. Pasienten, en dame på min alder, måtte tilkoples respirator etter noen dager med maskebehandling.
Hun ville helst ikke, hun var redd, og hun var tapper, ville så gjerne komme seg gjennom uten respiratorbehandling. Nå ligger hun i kunstig koma, tilkoplet respirator, snart på vei til et annet sykehus. Vi må skaffe ledig plass. Ikke fordi noen venter på tur, men for å ha kapasitet til den neste som måtte trenge respirator.
Følelsen av mismot når meg idet jeg trasker ned trappene til garderoben.
Å organisere og klargjøre for intensivtransport tar tid, det er mange som er involvert i prosessen. Når neste pasient er på vei opp fra akuttmottaket, er det for sent å organisere transport. Det blir en travel vakt, vi må holde fokus, vi jobber intensivt med begge pasientene.
Følelsen av mismot når meg idet jeg trasker ned trappene til garderoben. Er det god behandling å transportere alvorlig syke pasienter?
Historien min fra en helg på intensiv i februar 2021 viser noen av de etiske utfordringene sykepleiere har stått i gjennom pandemien. Knappe ressurser, lav bemanning og liten eller ingen tid til faglig og etisk refleksjon fører til at mange sykepleiere går på akkord med det de mener vil være god omsorg og forsvarlig helsehjelp.
Intensivsykepleier Rita Paulsen ved intensivavdelingen i Tromsø forteller at det høye arbeidspresset gjør at de ikke får snudd respiratorpasientene så ofte som de burde (1).
Mange sykepleiere har måttet håndheve regler som ikke tar individuelle hensyn.
Mange sykepleiere har måttet håndheve regler som ikke tar individuelle hensyn, og særlig utfordrende har det vært med besøksstans og sosial isolering. Rådet for sykepleieetikk har fått flere henvendelser både fra pårørende og sykepleiere med fortellinger om hvor vanskelig det har vært å følge restriksjonene. Det har også blitt stilt spørsmål om hvorvidt reglene har vært for strenge.
Frisk eller syk – vi ønsker alle å være sammen med dem som står oss nærmest, kanskje særlig i krisetider. De som gir oss trygghet og forankrer oss til livet. For noen har kanskje ensomhet og isolasjon bidratt til sykdom eller forverring av sykdom.
Dette er et eksempel på helsepersonellets skvis i pandemien: Vi skal følge strenge smittevernregler, samtidig som vi skal gi faglig forsvarlig og omsorgsfull hjelp. Det er en vanskelig balansegang, for vi har også en plikt til å ta vare på de mest sårbare – de av oss som trenger ekstra beskyttelse.
Høstens smitteutbrudd på sykehjem og sykehusavdelinger, til tross for at mange er vaksinerte, er en påminnelse om den utryggheten vi fortsatt befinner oss i.
Våre yrkesetiske retningslinjer sier følgende: «Sykepleieren ivaretar den enkelte pasients verdighet og integritet, herunder retten til faglig forsvarlig og omsorgsfull hjelp, retten til å være medbestemmende og retten til ikke å bli krenket»(2).
Vi vet at vi må ha beredskap for de neste syke som kommer. Vi gjør vår plikt.
Vi som jobbet sammen på intensivavdelingen «min» lørdagen i februar, visste hva som var denne respiratorpasientens beste. Det var ikke transport til et annet sykehus. Men hva var alternativet?
Magefølelsen settes til side, vi jobber samvittighetsfullt på alle kanter, tar vare på dem som allerede ligger her, dem som skal transporteres til et annet sykehus, og vi gjør klart til neste pasient. Vi vet at vi må ha beredskap for de neste syke som kommer. Vi gjør vår plikt.
Min fortelling er preget av pandemien. Mange sykepleiere opplever arbeidsdager i konstant skvis, også når hverdagen er normal.
Nå kommer det flere fortellinger fra sykepleiere i kjølvannet av pandemien, men det som beskrives, er en normaltilstand. Maria Fallsen skriver i et innlegg i Aftenposten at hun er sliten av å beklage for alt hun ikke får gjort. Hun forteller om en vakt der hun bidro til å redde liv, men hadde dårlig samvittighet for alt det andre hun ikke fikk gjort (3).
At kapasiteten i helsevesenet er for liten, er ikke noe nytt. Pandemien kommer på toppen av et allerede presset helsevesen. Vi mangler sykepleiere og helsefagarbeidere med fagkunnskaper, skriver Isachsen-Hagen og Lillebø i en kronikk i Adresseavisen. (4).
Tiden med pandemi har tydeliggjort hvordan knapphet på menneskelige ressurser utfordrer etikken generelt i helsevesenet. Det håper jeg sykepleiere fortsetter å snakke høyt om.
1. NTB. Stort press på intensivavdelingen på UNN. Nettavisen.. 13.11.2021. Tilgjengelig fra: https://www.nettavisen.no/nyheter/innenriks/stort-press-pa-intensivavdelingen-pa-unn/s/12-95-3424204969 (nedlastet 02.12.2021).
2. Norsk Sykepleierforbund (NSF). Yrkesetiske retningslinjer. Oslo: NSF; u.å. Tilgjengelig fra: https://www.nsf.no/sykepleiefaget/yrkesetiske-retningslinjer (nedlastet 02.12.2021).
3. Fallsen M. Jeg er sykepleier, og jeg er sliten. Av å beklage. Aftenposten. 02.11.2021. Tilgjengelig fra: https://www.aftenposten.no/meninger/debatt/i/5GWkem/jeg-er-sykepleier-og-jeg-er-sliten-av-aa-beklage (nedlastet 02.12.2021).
4. Isachsen-Hagen M, Lillebø G. Vi har deg, men alt har en grense. Adresseavisen. 12.11.2021. Tilgjengelig fra: https://www.midtnorskdebatt.no/meninger/kronikker/2021/11/12/Vi-har-deg-men-alt-har-en-grense-24802595.ece (nedlastet 02.12.2021).
Sykepleiere har arbeidsdager i konstant skvis mellom smittevern og forsvarlig helsehjelp. Det er en vanskelig balansegang.

Etter et og et halvt år med et liv og et samfunn «på vent» er vi endelig på vei tilbake til det normale. Selv om pandemien ikke er over ennå, kan vi se tilbake på hva vi har lært, og hva vi kan ta med oss videre.
Når det gjelder etikk og etiske utfordringer, har vi lært noe om hvilke verdier som utfordres under en pandemi. I etikkspalten våren 2020 skrev jeg om hvilke verdier som vi opplevde ble satt på prøve i starten av pandemien (1).
De utfordringene vi trodde ble de største, ble ikke så store som vi hadde fryktet.
I den første fasen ble spesielt prioriteringsutfordringer tydelige. Det handlet om alt fra prioritering av utstyr til prioritering av helsehjelp. En studie som ble gjennomført ved sykehus i Norge våren 2020, bekreftet disse utfordringene (2).
Etter hvert oppsto andre utfordringer som var knyttet til smittevern og besøk på sykehjem, behandling av sykehjemsbeboere og døende samt fordeling av vaksiner (3, 4). Det som er interessant, er at de utfordringene vi trodde ble de største, slik som press på intensivplasser og mangel på respiratorer, ikke ble så store som vi hadde fryktet.
I ettertid kan vi spørre oss om ikke håndteringen og prioriteringene i starten av pandemien var panikk- og fryktdrevet, slik at ressursfordelingen dermed ble feil. Fikk oppmerksomheten på intensivplasser og sykehuskapasitet for stor plass, slik at kommunehelsetjenesten fikk lide? Vi var flere som var bekymret for dette (3, 5). Samtidig må vi ta i betraktning at covid-19 var en helt ny sykdom, som vi hadde lite kunnskap om og få erfaringer å bygge på.
En annen ting vi bør spørre oss om, er om vi i for stor grad vektla smittevern, spesielt på sykehjem. Når vi står overfor etiske utfordringer, er det ofte ulike verdier som kommer i konflikt. Og da må vi velge hvilke verdier vi vil prioritere.
Under pandemien kunne det se ut som om verdien av liv og helse trumfet verdier knyttet til de psykososiale behovene. En slik prioritering er ikke ny. Forskning har også vist tidligere at medisinske og fysiske behov ofte blir prioritert fremfor de psykososiale behovene (6, 7).
Når vi står overfor etiske utfordringer, er det ofte ulike verdier som kommer i konflikt.
Vi kan jo spørre oss om de eldste på sykehjem ville hatt det bedre hvis de hadde fått mer besøk, og vi hadde lagt mindre vekt på smittevern? Samtidig har det vært ekstra utfordrende på sykehjem når hensynet til den enkelte beboerens behov for sosial kontakt ble satt opp mot fellesskapets behov for smittevern.
Selv om en beboer på et sykehjem kanskje ville vært mer opptatt av å få besøk av sine nærmeste enn å beskytte seg selv mot smitte, måtte man likevel ta hensyn til fellesskapet og de som var redd for å bli smittet. Hensynet til den enkelte veid opp mot hensynet til de andre har vært et etisk dilemma gjennom hele pandemien.
Under pandemien har vi lært mye om hvordan vi både kan legge til rette for besøk samt ivareta smittevern. Vi måtte være kreative og finne nye løsninger, med digitale møteplasser og fysiske møteplasser utenfor institusjonene. Denne lærdommen kan vi ta med oss videre.
En problemstilling det ikke har vært snakket så mye om, er de ansatte i helsetjenesten med tanke på det de har ofret, og den risikoen de har tatt. Mange har kjent på en frykt for å ta med seg smitte til pasienter, men også for å ta med seg smitte hjem.
Vi vet lite om hvordan denne redselen har påvirket de ansatte, og hvilke konsekvenser den har fått i etterkant. Vi vet lite om hvilket moralsk stress de ansatte har opplevd, og om dette stresset kan ha ført til større utskiftning av ansatte. Her trengs det forskning.
Vi vet lite om hvilket moralsk stress de ansatte har opplevd.
Utfordringene som er beskrevet over, er ikke nye. Slike utfordringer står vi overfor i helsetjenesten hver dag. Men vi har sett at utfordringene har blitt forsterket under pandemien, og de har hatt større konsekvenser både for pasienter og ansatte.
Nå må vi ikke slutte å sette søkelyset på problemstillingene, selv om de er mindre dramatiske enn de har vært under pandemien. Vi må fortsette å spørre oss om vi prioriterer riktig, og vi må fortsette å stille spørsmål om vi ivaretar døende på en verdig måte. Vi må ta de ansattes moralske stress på alvor, uavhengig av om vi står i en pandemi eller ikke.
1. Heggestad AKT. I krevende tider blir verdiene våre satt på prøve. Sykepleien. 2020;108(80878):(e-20878). DOI: 10.4220/Sykepleiens.2020.80878
2. Miljeteig I, Forthun I, Hufthammer KO, Engelund IE, Schanche E, Husøy OK. Priority-setting dilemmas, moral distress and support experienced by nurses and physicians in the early phase of the COVID-19 pandemic in Norway. Nurs Ethics. 2021;28(1):66–81. DOI: 10.1177/0969733020981748
3. Myrstad M, Ranhoff AH. Akutt syke eldre i koronaens tid. Tidsskr Nor Legeforen. 25.03.2020. DOI: 10.4045/tidsskr.20.0227
4. Eriksen S, Grov EK, Lichtwarck B, Holmefoss I, Bøhn K, Myrstad C, et al. Behandling, omsorg og pleie for døende sykehjemspasienter med covid-19. Tidsskr Nor Legeforen. 23.04.2020. DOI: 10.4045/tidsskr.20.0306.
5. Heggestad AKT, Førde R, Pedersen R, Magelssen M. Prioriteringsutfordringer i helse- og omsorgstjenesten i kommunene under covid-19-pandemien. Tidsskrift for omsorgsforskning. 2020;6(01):1–4. DOI: 10.18261/issn.2387-5984-2020-01-11
6. Pedersen R, Nortvedt P, Nordhaug M, Slettebø Å, Grøthe KH, Brinchmann BS, et al. In quest of justice? Clinical prioritisation in healthcare for the aged. J Med Ethics. 2008;34(4):230–5. DOI: 10.1136/jme.2006.018531
7. Heggestad AKT, Nortvedt P, Slettebø Å. Dignity and care for people with dementia living in nursing homes. Dementia. 2015;14(6):825–41. DOI: 10.1177/1471301213512840
Under hele pandemien har hensynet til den enkelte blitt veid opp mot hensynet til fellesskapet. Har prioriteringene vært riktige, eller har de vært drevet av frykt?
– Sykepleieren har en sentral rolle i kampen mot antibiotikaresistens. Det gjenspeiles ikke i handlingsplanene, skriver NSF-lederen.